Descrição
Princípios da imunologia e sua aplicação na identificação de grupos sanguíneos e doenças relacionadas.
Propósito
Compreender os principais sistemas eritrocitários e como o nosso sistema imunológico atua na defesa do organismo. Esse conhecimento facilitará o entendimento dos testes imuno-hematológicos e das doenças correlacionadas.
OBJETIVOS
Módulo 1
Descrever os componentes e as funções das respostas imunes inata
e adquirida e a interação
antígeno-anticorpo
Módulo 2
Identificar os principais sistemas eritrocitários humanos e as doenças associadas
Módulo 3
Reconhecer métodos imuno-hematológicos para classificação sanguínea e diagnóstico de doenças relacionadas
Introdução
Ao longo desta jornada, vamos estudar a organização estrutural do sistema imunológico e entender como seus componentes celulares e moleculares interagem entre si para garantir a geração de respostas imunológicas eficazes, bem como as características da interação entre antígenos e anticorpos.
Além disso, vamos desvendar os principais sistemas de classificação eritrocitários e relacionar os grupos ABO e Rh às doenças geradas por incompatibilidade sanguínea, identificando os princípios dos testes imuno-hematológicos e sua importância diagnóstica. Você sabe qual tipo sanguíneo um paciente AB positivo pode receber? E um paciente O negativo? Vamos descobrir?
MÓDULO 1
Descrever os componentes e as funções das respostas imunes inata e adquirida e a interação antígeno-anticorpo
Sistema imunológico
Nosso sistema imunológico é um conjunto de tecidos, células e moléculas que atuam de forma coordenada para nos defender de microrganismos que podem nos causar infecções ou doenças.
Além disso, o sistema imunológico é capaz de reconhecer e eliminar do nosso organismo células tumorais ou que sofreram algum dano que prejudique sua função normal. Em casos de transplante de órgãos, de tecidos e nas transfusões sanguíneas, o sistema imunológico também pode reconhecer esses elementos como não próprios e desencadear a resposta imune.
Os mecanismos de defesa do hospedeiro seguem uma sequência coordenada de etapas, sendo que, em cada uma delas, as propriedades específicas dos componentes do sistema imune desempenham papel fundamental. Dessa forma, é essencial entender a organização do sistema imunológico para a geração de respostas eficazes.
Assim, temos o rápido direcionamento das células efetoras da imunidade inata para os locais de infecção, permitindo que linfócitos reconheçam e respondam de forma específica a determinado antígeno, independentemente do local em que ele é introduzido no organismo.
Órgãos linfoides e células do sistema imune
O sistema imunológico é composto por diferentes órgãos, que são classificados como órgãos geradores ou primários e órgãos periféricos ou secundários. A medula óssea é um órgão gerador, no qual há produção de todos os elementos figurados do sangue a partir da célula hematopoiética pluripotente, observados na figura a seguir.
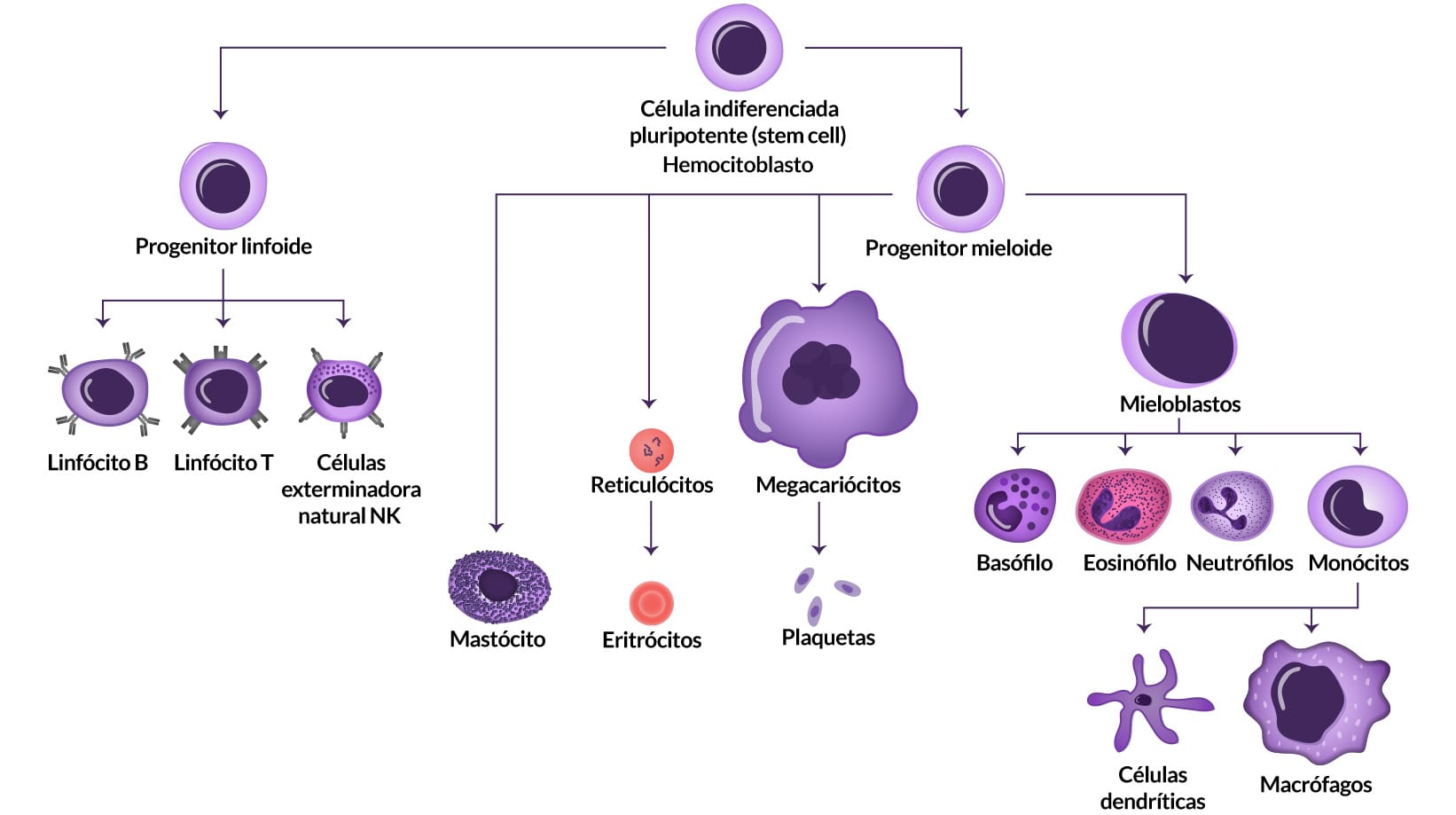
- No timo, outro órgão gerador, ocorre a maturação de linfócitos T.
- Nos órgãos linfoides periféricos, ocorre a apresentação de antígenos aos linfócitos, possibilitando o início da resposta imune adquirida. Nos linfonodos, os linfócitos B e T encontram os antígenos coletados pela linfa dos tecidos periféricos e, no baço, os antígenos capturados no sangue encontram os linfócitos.
- Além de formarem aglomerados que dão origem a órgãos linfoides, as células das imunidades inata e adquirida encontram-se como células circulantes no sangue e na linfa. As células do sistema imunológico que circulam no sangue pertencem à série leucocitária e compreendem os linfócitos, granulócitos e monócitos.
- Os leucócitos permanecem temporariamente no sangue e migram para o tecido conjuntivo através das paredes dos capilares e vênulas, processo conhecido como diapedese ou transmigração. Uma vez nos tecidos, essas células desempenharão funções específicas.
- Os leucócitos são agrupados em granulócitos e agranulócitos de acordo com suas características morfológicas. Os granulócitos são os neutrófilos, eosinófilos e basófilos, e os agranulócitos são os monócitos e linfócitos. Vamos, agora, conhecer um pouco mais sobre a série granulocítica?
Série granulocítica
Os basófilos contêm grânulos com enzimas hidrolíticas, fatores quimiotáticos, heparina e histamina em seu citoplasma e receptores de imunoglobulina em sua superfície, desempenhando papel importante, principalmente nas reações alérgicas (hipersensibilidade do tipo I) e anafiláticas.
Número de células anormalmente aumentado no sangue.
Colite ulcerativa, asma, sinusite e rinite, artrite, insuficiência renal crônica, anemia hemolítica, leucemia mieloide crônica, quimioterapia, remoção do baço.
Número de células anormalmente diminuído no sangue.
Urticária, hipertireoidismo, síndrome de Cushing, uso de corticosteroides, ovulação ou gestação, estresse.
Os eosinófilos apresentam grânulos que contêm enzimas hidrolíticas (peroxidase, histaminase, arilsulfatase) e outras proteínas. Essas células migram do sangue para os tecidos periféricos, sendo encontradas especialmente no revestimento de mucosas dos tratos respiratório, gastrointestinal e genitourinário, podendo aumentar em número sob condições inflamatórias.
Além disso, os eosinófilos estão envolvidos no combate a infecções parasitárias causadas por helmintos e na produção de citocinas que modulam respostas inflamatórias nas reações alérgicas.
Doenças parasitárias, alergias (asma e eczemas).
Síndrome de Cushing, uso de corticosteroides, estresse.
Os neutrófilos constituem a população mais numerosa de leucócitos no sangue e compõem a primeira linha de defesa do hospedeiro, destacando-se sua grande capacidade fagocítica. O acúmulo de neutrófilos mortos e bactérias degradadas no sítio de infecção forma o pus.
Infecções bacterianas, apendicite, gestação, estresse.
Câncer, esplenomegalia, doenças autoimunes, quimioterapia, radioterapia, deficiência de vitamina B12 ou folato.
Série agranulocítica
Os monócitos são as maiores células observadas em esfregaços sanguíneos. Esses tipos celulares podem ser recrutados rapidamente da corrente sanguínea para os sítios de inflamação, e, ao entrar nos tecidos, os monócitos diferenciam-se em macrófagos. Desempenham funções tanto na imunidade inata, como a fagocitose e morte de microrganismos por meio da produção de espécies reativas de oxigênio e digestão proteolítica, como na adquirida, pois apresentam antígenos aos linfócitos.
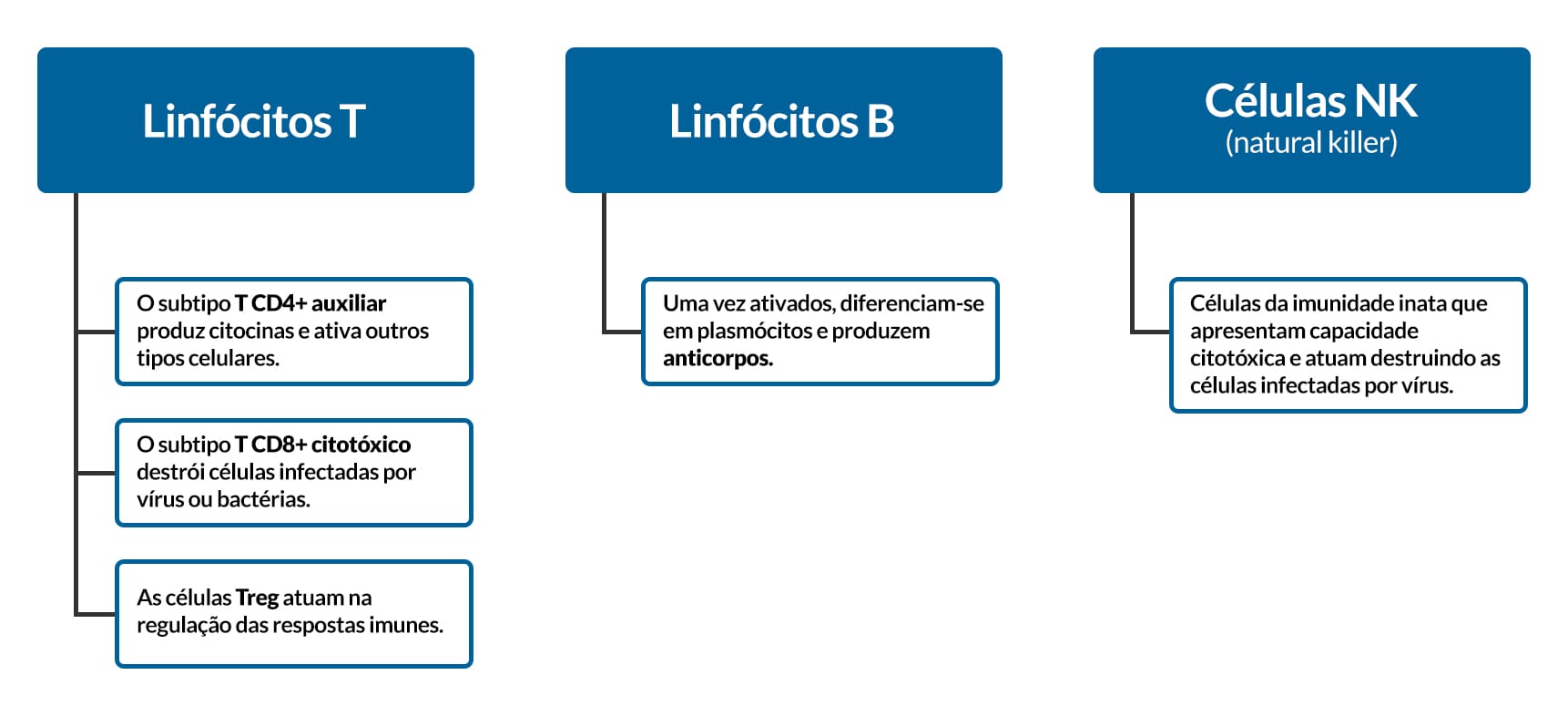
Os linfócitos são células geralmente pequenas, classificadas em diversos tipos, os quais diferem nas funções e em seus produtos proteicos. As principais populações são:
Este vídeo apresenta um aprofundamento sobre diapedese, suas causas, seu processo e seus efeitos.
Resposta imune inata e adquirida
As respostas imunes compõem um sistema integrado de defesa do hospedeiro, no qual diversas células e moléculas atuam em cooperação. Nossa primeira linha de defesa é constituída pela imunidade inata ou natural, composta por barreiras naturais (pele, mucosas, enzimas), células fagocíticas, em especial neutrófilos e macrófagos, e proteínas de fase aguda, como a proteína C reativa (PCR) e os componentes do sistema complemento.
As proteínas de fase aguda podem ser úteis como biomarcadores de condições patológicas. Sintetizada pelos hepatócitos em resposta a citocinas inflamatórias como a IL-6, a PCR tem sido utilizada como marcador de resposta de fase aguda, uma vez que seus níveis séricos aumentam rapidamente após lesão e/ou necrose tecidual, infecção ou outros processos inflamatórios.
Biomarcadores
Biomarcadores ou marcadores biológicos são utilizados na prática clínica para diagnóstico ou identificação de riscos de ocorrência de determinada doença.
A PCR tem especial utilidade na investigação e no acompanhamento de isquemia ou infarto agudo do miocárdio, queimaduras, doenças renais, hematológicas e reumatológicas.
A imunidade adquirida ou adaptativa desenvolve-se posteriormente à ação da imunidade inata, e seus componentes celulares são capazes de reconhecer antígenos de forma específica.
Com o antígeno reconhecido, uma resposta pode ser desencadeada por meio da produção de anticorpos, por exemplo.
Esse tipo de resposta confere memória protetora contra o mesmo antígeno, isto é, durante uma segunda exposição, frequentemente a resposta é mais rápida do que na infecção primária.
A imunidade adquirida celular ou mediada por células tem como seus principais componentes os diversos subtipos de linfócitos T, classificados de acordo com seu modo de ação. Por sua vez, a imunidade adquirida humoral é mediada por anticorpos produzidos pelos plasmócitos.
Antígenos e anticorpos
Antígenos são definidos como moléculas ou partículas que, uma vez reconhecidas por células do nosso sistema imunológico, podem desencadear ou não uma resposta imunológica. Um antígeno capaz de ativar uma resposta imunológica é chamado de imunógeno. Cada antígeno possui sítios de reconhecimento aos quais os anticorpos ou receptores de linfócitos B se ligam. Os antígenos podem ser moléculas simples ou complexas, como:
- Metabólitos intermediários de carboidratos, lipídeos e hormônios.
- Macromoléculas, como carboidratos complexos, fosfolipídeos, ácidos nucleicos e proteínas.
As imunoglobulinas, popularmente conhecidas como anticorpos, caracterizam-se por serem moléculas proteicas que atuam como receptores de membrana dos linfócitos B (BCR) ou podem se apresentar em sua forma solúvel, sendo sintetizadas por plasmócitos (linfócitos B diferenciados).
Os anticorpos são produzidos em resposta a determinado antígeno, sendo capazes de se ligar a ele de forma altamente específica, formando os chamados imunocomplexos. Os anticorpos podem atuar em diferentes processos, tais como:
- Neutralização de microrganismos ou toxinas.
- Opsonização de patógenos, possibilitando o aumento da fagocitose e da toxicidade mediada por células dependentes de anticorpos.
- Ativação do sistema complemento.
- Ativação de mastócitos nas infecções por helmintos.
Opsonização
A opsonização consiste na fixação de moléculas como anticorpos à superfície de patógenos. Dessa forma, os fagócitos têm a sua ação otimizada.
No nosso organismo, temos cinco tipos de imunoglobulinas. Você sabe como elas são classificadas?
Cada uma dessas classes está envolvida em um tipo específico de proteção. Clique nas setas e conheça cada classificação.
As classes e a quantidade de anticorpos podem variar de acordo com o tipo de resposta imunológica. A IgM é denominada “anticorpo frio”, pois sua fixação ao antígeno é máxima em baixas temperaturas e praticamente nula a 37 °C; é sintetizada de forma mais rápida e em maior quantidade na resposta primária. Por sua vez, a IgG é denominada “anticorpo quente”, pois sua fixação é ótima a 37 °C, sendo produzida de forma tardia e em menor quantidade.
Na interpretação de exames imunológicos, a detecção de IgM indica infecção aguda ou recente, enquanto a detecção de IgG indica que houve contato com o antígeno há algum tempo. De forma geral, os anticorpos da classe IgM podem permanecer de três a seis meses no organismo, e os anticorpos IgG resistem por tempo mais prolongado ou permanecem durante toda a vida.
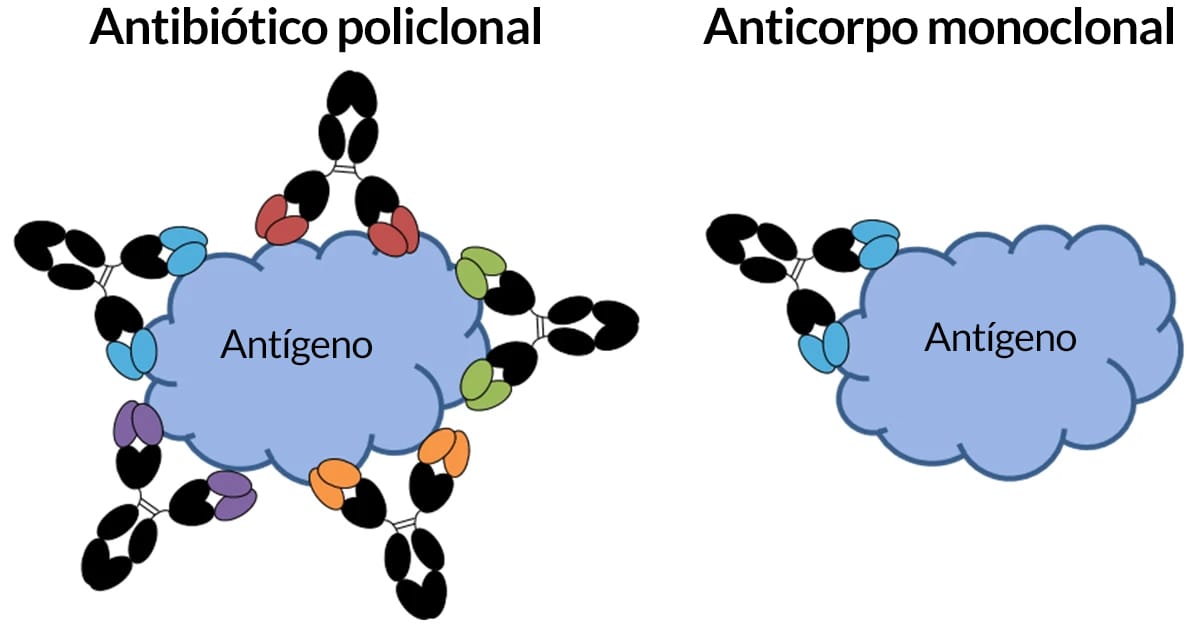
No plasma sanguíneo, encontramos muitos anticorpos diferentes, sendo cada um deles derivado de um clone de linfócito B. Quando temos ativação de diversos clones de linfócitos B e estes, diferenciados em plasmócitos, produzem anticorpos, denominamos anticorpos policlonais, uma vez que são produtos de clones diferentes e cada um desses clones produz anticorpos de especificidade única.
Os anticorpos monoclonais ou mAbs são produzidos a partir de um único clone de linfócito B, que passa a produzir sempre os mesmos anticorpos em resposta a um antígeno. Saiba mais sobre eles clicando a seguir:
Podem ser produzidos em grande quantidade em laboratório a partir de linfócitos B gerados por camundongos cujo sistema imunológico tenha sido estimulado por antígenos de interesse.
As novas gerações de mAbs quiméricos e humanizados usam camundongos geneticamente modificados para produzir uma molécula híbrida, o que diminui a probabilidade de reação do sistema imunológico humano contra proteínas do camundongo.
Quiméricos
Um anticorpo quimérico é constituído por uma combinação de uma região do anticorpo de camundongo e outra região do anticorpo humano.
Os mAbs são utilizados como ferramentas diagnósticas e terapêuticas. Como exemplos, temos: infliximab ou entanercept para o controle da inflamação na artrite reumatoide e doença de Crohn; trastuzumab para tratamento de câncer de mama; muromonab-CD3 para diminuição da rejeição de transplante renal, entre outros.
Interação antígeno-anticorpo
A ligação do anticorpo ao antígeno ocorre em um sítio específico, denominado epítopo ou determinante antigênico. Uma macromolécula que apresenta muitos epítopos iguais é chamada de antígeno polivalente. Os epítopos podem ser classificados de acordo com sua estrutura em:
- Determinantes lineares: formados com aproximadamente seis aminoácidos em sequência linear.
- Determinantes conformacionais: formados por aminoácidos que não estão em sequência, sendo encontrados na forma de proteína dobrada.
A interação antígeno-anticorpo (Ag-Ac) é semelhante à interação de enzimas com seus substratos (modelo chave e fechadura) ou de hormônios com seus receptores, mas com algumas diferenças. Você imagina quais?
O anticorpo não provoca alteração química irreversível na molécula do antígeno; assim, o produto formado (Ag-Ac) pode se dissociar em dois componentes, ficando cada um deles livre em solução. Além disso, os antígenos apresentam estruturas químicas que favorecem a complementaridade com o anticorpo por meio de ligações não covalentes reversíveis.
Não covalentes reversíveis
Essas ligações podem ser rompidas após o contato com altas concentrações de sal, pH extremo, detergentes e também por competição com elevadas concentrações do próprio epítopo puro.
A associação antígeno e anticorpo apresenta diferentes peculiaridades; um anticorpo pode apresentar distintas afinidades, avidez e especificidade a uma gama de moléculas.
Porém, o que são afinidade, avidez e especificidade? Clique nas abas para conhecer cada uma delas.
É determinada pela força de ligação resultante entre um anticorpo e um único epítopo do antígeno e depende da complementariedade entre as duas moléculas. Anticorpos com alta afinidade apresentam grande similaridade ao antígeno, interagindo por meio de ligações fortes e duradouras; anticorpos com baixa afinidade dissociam-se rapidamente, pois estabelecem ligações mais fracas.
É determinada pela força resultante de interações múltiplas entre uma molécula de anticorpo e os epítopos de um antígeno complexo. Assim, quanto maior a avidez, melhor o efeito biológico final do anticorpo, porém a afinidade será menor. A baixa afinidade de um anticorpo pode ser compensada por uma avidez elevada, como acontece em uma molécula de IgM, que, por ser pentamérica, apresenta diferentes sítios de ligação.
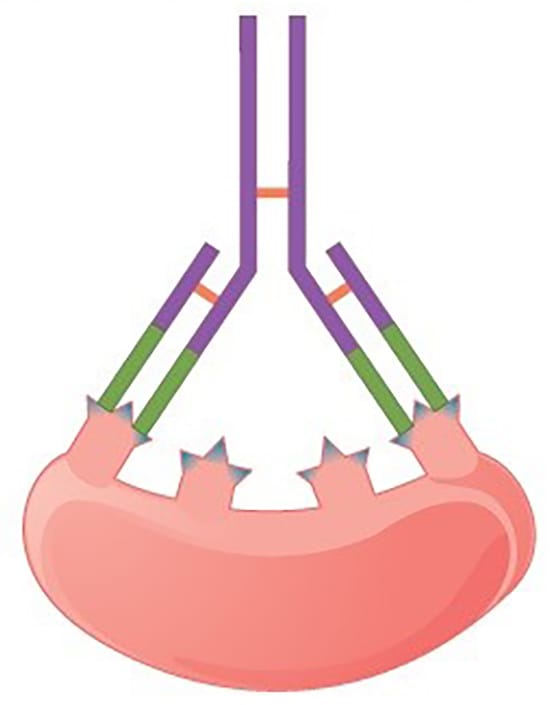
Afinidade se refere à força da interação antígeno-anticorpo único. Na figura vemos a interação entre IgG e o antígeno. Cada sítio de ligação do anticorpo IgG normalmente tem alta afinidade para seu sítio de ligação.
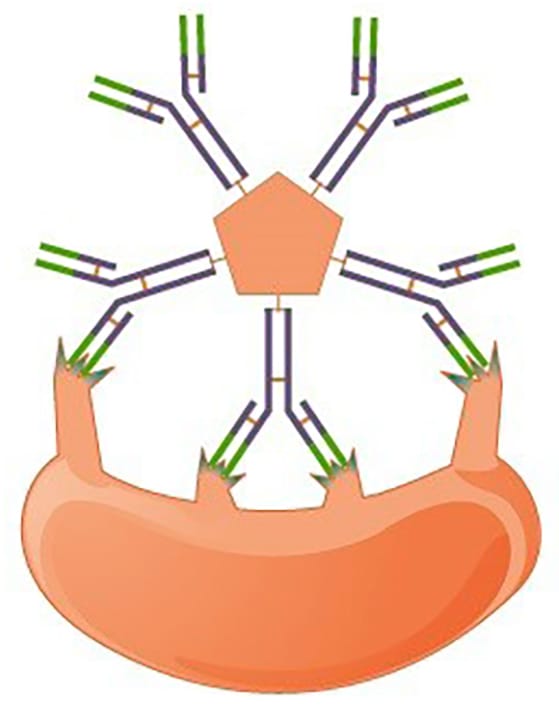
Avidez refere-se à força de todas as interações combinadas. Na figura vemos a interação de IgM com um antígeno, que tem locais de ligação ao antígeno de baixa afinidade, mas, como é uma estrutura pentamérica, há dez sítios de ligação, assim a avidez é alta.
Consiste na habilidade do anticorpo de distinguir seu imunógeno de outros antígenos.
A relação Ag-Ac é influenciada por diversos fatores. Assim, reações entre antígenos e anticorpos polivalentes são mais estáveis, sendo detectadas mais facilmente. Caso o antígeno seja particulado, geralmente é observada a aglutinação do antígeno pelo anticorpo. No entanto, se o antígeno estiver na forma solúvel, geralmente é observada a precipitação de um antígeno após a produção de grandes complexos Ag-Ac insolúveis. A formação dos complexos Ag-Ac é influenciada pela temperatura e pelo tempo de reação. Já o tamanho desses complexos está relacionado à concentração do antígeno e do anticorpo.
Particulado
Antígenos particulados constituem a estrutura de bactérias, fungos, vírus e alguns tipos celulares, como hemácias. Geralmente, são mais imunogênicos que antígenos solúveis.
Reatividade cruzada
Alguns anticorpos podem ter habilidade de interagir com mais de um epítopo com propriedades químicas similares. Assim, é possível que ocorram ligações mais fracas com regiões semelhantes, mas não idênticas, do antígeno que o induziu. Esse tipo de ligação é chamado de reação cruzada. Observe a seguir:
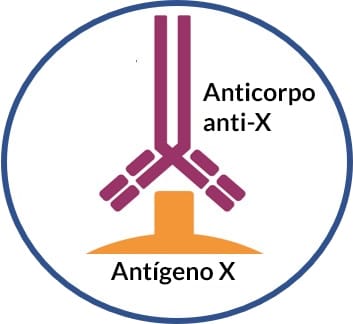

Epítopo similar

Epítopo compartilhado
Muitos vírus e diversas bactérias podem apresentar epítopos idênticos ou similares a componentes normais da célula hospedeira. Os antígenos microbianos estimulam anticorpos que reagem de maneira cruzada com os componentes da célula hospedeira e resultam em uma reação autoimune que lesiona o tecido.
Exemplo
Um exemplo é a bactéria Streptococcus pyogenes, que expressa proteínas na parede celular (antígenos M). Os anticorpos produzidos contra antígenos M reagem de forma cruzada com várias proteínas do miocárdio e do músculo esquelético, causando lesões cardíacas e renais que levam ao desenvolvimento da febre reumática.
Além disso, sabe-se que algumas bactérias intestinais têm substâncias quimicamente semelhantes que apresentam reatividade antigênica cruzada com antígenos A e/ou B expressos na superfície dos eritrócitos.
Verificando o aprendizado
ATENÇÃO!
Para desbloquear o próximo módulo, é necessário que você responda corretamente a uma das seguintes questões:
O conteúdo ainda não acabou.
Clique aqui e retorne para saber como desbloquear.
MÓDULO 2
Identificar os principais sistemas eritrocitários humanos e as doenças associadas
Antígenos Eritrocitários
Nossas hemácias têm diferentes antígenos de superfície em suas membranas. Dentre os antígenos presentes, temos o sistema ABO e Rh, que possibilitam a determinação do tipo sanguíneo de cada indivíduo. Você sabe qual é seu grupo sanguíneo? Sabe qual tipo sanguíneo você pode receber em uma transfusão? Faz ideia de como são realizados os exames pré-transfusionais?
Os grupos sanguíneos têm grande importância no contexto da transfusão de sangue, pois, se indivíduos que não apresentam determinado antígeno eritrocitário (exemplo o antígeno Rh) entrarem em contato com esse antígeno (Rh positivo) durante uma transfusão sanguínea, produzirão anticorpos contra esse antígeno (anticorpo anti-Rh), o que pode causar uma reação transfusional, com hemólise, podendo até levar o paciente ao óbito.
Assim, a determinação do tipo sanguíneo de um indivíduo é uma das etapas essenciais para possibilitar uma transfusão sanguínea segura. Apesar de serem descritos centenas de tipos de antígenos eritrocitários, os mais importantes e complexos pertencem aos grupos ABO e Rh. Esses são os dois sistemas com maior relevância no contexto de compatibilidade sanguínea.
Sistema ABO
O sistema ABO foi o primeiro sistema de classificação sanguínea a ser descrito em 1900. Na ocasião, o cientista austríaco Karl Landsteiner observou aglutinação após misturar diferentes amostras de sangue.
Posteriormente, Landsteiner descobriu que a aglutinação era causada por uma reação imunológica que ocorre quando anticorpos são produzidos contra células do sangue de um doador. Essa resposta imune é induzida porque existe grande variação dos antígenos localizados na superfície dos eritrócitos entre as pessoas.
Esses antígenos estão presentes nas hemácias e na maioria das células epiteliais e endoteliais, linfócitos e plaquetas. Além disso, apresentam-se na forma solúvel em secreções como saliva, lágrima, leite, urina e líquido amniótico. Por esse motivo, o sistema ABO é considerado um sistema de histocompatibilidade.
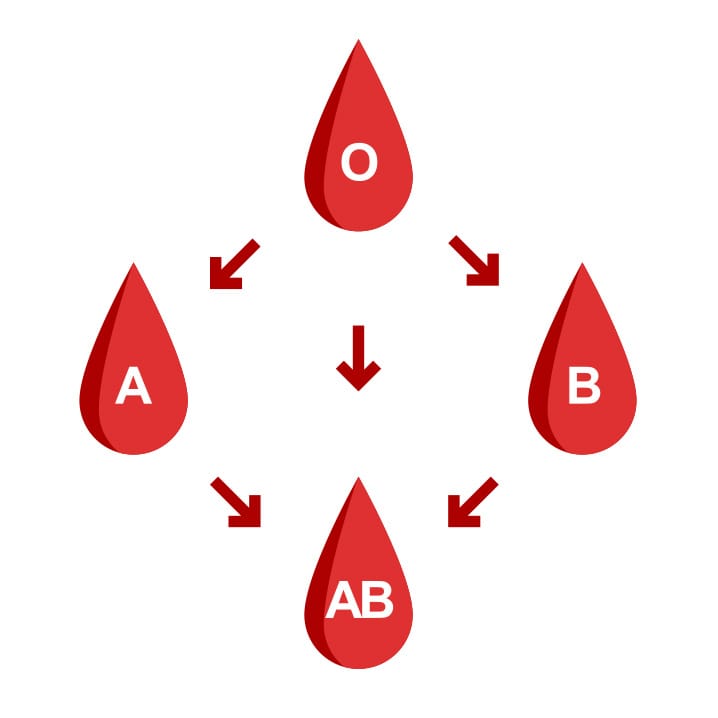
Os antígenos do sistema ABO são definidos por uma proteína codificada por um gene único, para o qual há três alelos: A, B e O. Observa-se uma relação de dominância dos alelos A e B sobre o alelo O e uma codominância entre os alelos A e B, o que nos dá a possibilidade de quatro tipos sanguíneos: A, B, AB ou O.
Exemplo
Dessa forma, se um indivíduo com tipo sanguíneo A, por exemplo, recebe sangue de um indivíduo de um tipo sanguíneo diferente (como tipo B), o sistema imunológico desse receptor não reconhecerá os antígenos B nas células do sangue do doador e, portanto, considerará que eles são estranhos à sua composição.
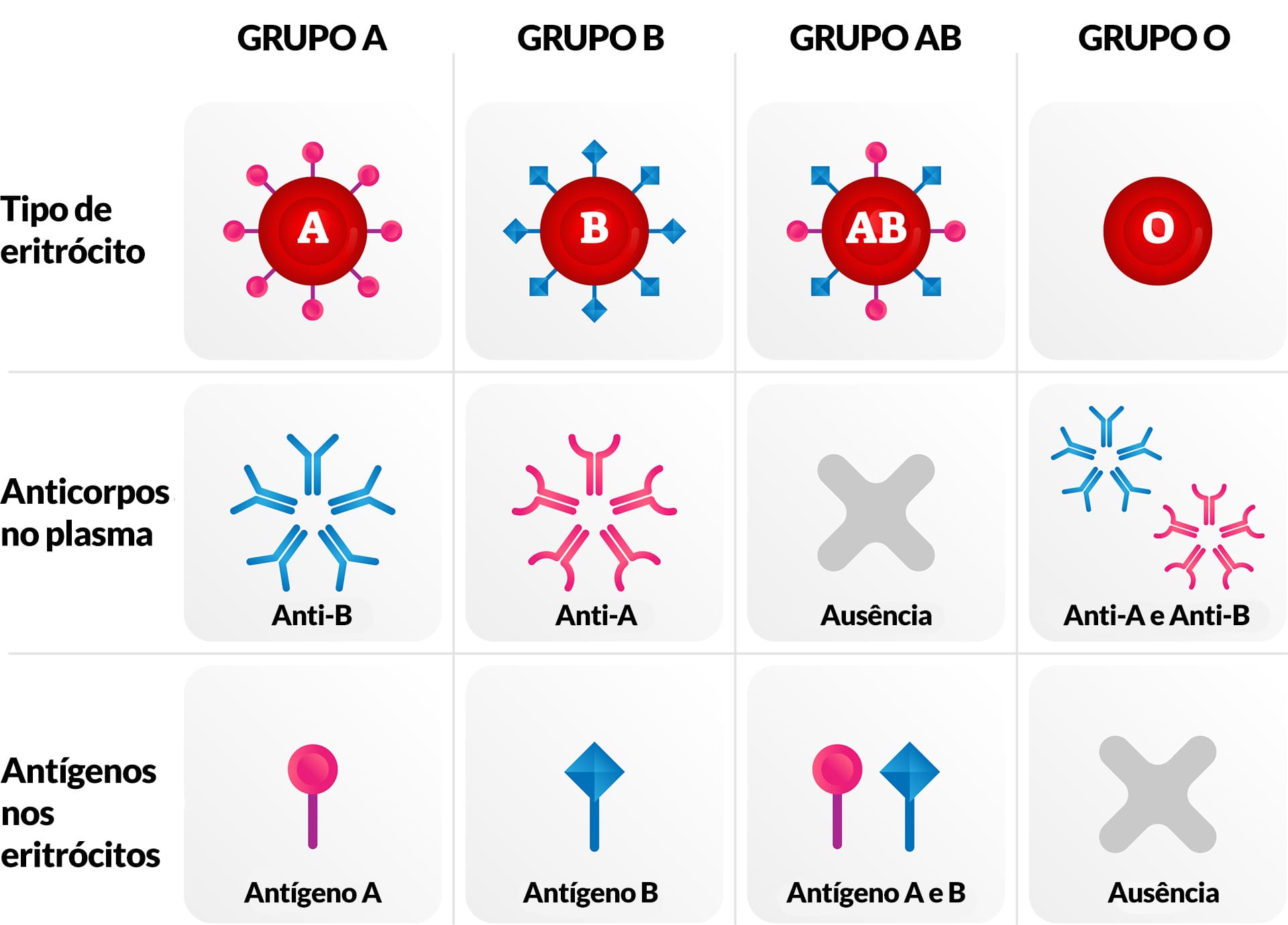
Durante nossa vida, já escutamos muito os termos doador e receptor universal. Vamos entender o que é isso?
A identificação dos antígenos eritrocitários do sistema ABO e dos anticorpos produzidos possibilita entender a compatibilidade entre os grupos sanguíneos (Figura 9). A ausência de antígenos nas hemácias do grupo O possibilita que os grupo A, B e AB recebam sangue do tipo O, por isso esse tipo sanguíneo é definido como doador universal. O grupo AB é considerado o receptor universal, uma vez que não produz anticorpos anti-A e anti-B, podendo, assim, receber sangue de qualquer grupo sanguíneo.
A expressão dos genes ABO depende da ação do gene H, que se apresenta em 99% da população sob a forma homozigota HH ou heterozigota Hh. A forma hh é rara e caracteriza o fenótipo Bombaim, que compreende indivíduos que não apresentam antígenos ABO e H nem nos eritrócitos nem em substâncias solúveis: são os chamados “falsos O”.
Os anticorpos contra antígenos A e/ou B são encontrados no plasma de indivíduos com eritrócitos que não apresentam o antígeno correspondente. Portanto, diferem dos demais por terem ocorrência natural, mesmo em indivíduos que não receberam transfusão ou tiveram gestação prévia.
Os anticorpos mais importantes são anti-A e anti-B. Em geral, são anticorpos da classe IgM, e a reação com os antígenos correspondentes é ótima em temperaturas baixas (4 °C), sendo chamados de anticorpos frios, apesar de também serem reativos à temperatura corporal, em torno de 37 °C.
| Aglutinógenos e Aglutininas contidos no sangue - Sistema ABO | ||
|---|---|---|
| Tipos | Aglutinógenos | Aglutininas |
| O Bombay* | Não contém | Anti-A1, Anti-A2, Anti-B e Anti-H |
| O | H | Anti-A1, Anti-A2 e Anti-B |
| A1 | A1 | Anti-B (Anti-A2*) |
| A2 | A2 | Anti-B (Anti-A1*) |
| B | B | Anti-A1, Anti-A2 |
| A1B | A1, B, H | (Anti-A2*) |
| A2B | A2, B, H | (Anti-A1*) |
| Onde se encontram | Hemácias | Plasma |
Aglutinógeno: Aglutinógeno ou aglutinogênio é a substância antigênica que estimula a formação de uma aglutinina específica.
Aglutinina: Substância que pode provocar a aglutinação de células quando identificadas como antígeno.
Saiba mais
Os anticorpos naturais ABO estão ausentes no nascimento; entre 3 e 6 meses de vida, começam a aparecer e atingem títulos máximo entre 5 e 10 anos, permanecendo elevados até a fase adulta. Esses anticorpos apresentam grande relevância do ponto de vista transfusional, estando relacionados à reação transfusional grave e em casos de DHRN de forma clínica moderada, causando icterícia leve.
Sistema Rh
Com mais de 50 diferentes antígenos caracterizados, o sistema Rh é o maior de todos os sistemas sanguíneos.
O antígeno RhD foi descoberto em 1939 pelos cientistas Philip Levine e Rufus Stetson, quando estudaram o caso de uma mãe que necessitou de transfusão após o nascimento de seu bebê natimorto. Apesar de ambos serem do tipo O, a mulher apresentou reação hemolítica transfusional ao receber sangue do marido.
Os cientistas levantaram a hipótese de que o pai do bebê (o doador das hemácias que a mãe recebeu) tinha um "fator" (antígeno) que faltava à mãe e que o bebê havia herdado do pai. Em gestações anteriores, a mãe havia sido imunizada por exposição às hemácias de seus outros bebês, que também tinham esse fator.
O fator ou anticorpo que causou a morte do bebê foi atribuído ao sistema Rh (remetendo ao modelo experimental utilizado – macaco do gênero Rhesus) e nomeado de anti-D.
Os antígenos do sistema RH são encontrados apenas nas hemácias. Esse antígeno é codificado por um par de genes homólogos RHD e RHCE, que codifica a produção do antígeno RhD, e de dois pares de antígenos antitéticos: C, c, E, e, respectivamente. Quando falamos em pacientes RH positivo ou negativo, isso corresponde à presença ou à ausência na hemácia do antígeno D, mas ambos apresentam os antígenos Cc e Ee .
Diferentemente dos anticorpos ABO, os anticorpos Rh raramente ocorrem de forma natural, sendo considerados anticorpos imunes. Isso significa dizer que anticorpos Rh resultam de sensibilização que ocorre por transfusão sanguínea prévia ou gestação anterior. O anticorpo anti-D é responsável pela maior parte das implicações clínicas associadas ao sistema Rh.
A classificação simples dos indivíduos em Rh D+ e Rh D –, usando soro anti-D, geralmente se mostra suficiente para fins clínicos. Anti-C, anti-c, anti-E e anti-e são vistos ocasionalmente e podem causar tanto reações transfusionais como doença hemolítica do recém-nascido (DHRN).
Sistemas Lewis, Kell, Duffy e outros sistemas eritrocitários
Além dos sistemas ABO e Rh, outras classificações de antígenos eritrocitários são propostas, entre elas os sistemas Lewis, MNS, P, I, Kell e Duffy. Embora a ocorrência natural de anticorpos dos sistemas Lewis, P e MNS não seja incomum, eles geralmente reagem apenas a baixas temperaturas e, por isso, não acarretam consequências clínicas.
A frequência de detecção de anticorpos imunes contra antígenos desses sistemas é pequena. Muitos antígenos apresentam baixa antigenicidade, e outros, embora imunogênicos, apresentam frequência relativamente baixa.
O sistema Lewis fundamenta-se na classificação do sangue humano com base na expressão de glicoproteínas chamadas antígenos de Lewis (Le), na superfície dos eritrócitos ou nos fluidos corporais, ou em ambos. Esse sistema está bioquimicamente associado ao sistema de grupo sanguíneo ABO, embora os loci genéticos não estejam ligados entre si.
O sistema consiste em dois alelos, chamados de Le (dominante) e le (recessivo). A presença de Le especifica a formação do antígeno Lea, um antígeno solúvel em água identificado em 1946. Um segundo antígeno, Leb, identificado em 1948, ocorre apenas quando os alelos Le e H (do sistema de grupo sanguíneo ABO) interagem e é encontrado em indivíduos secretores que expressam fenótipo eritrocitário Le (a-b+).
O sistema Kell foi descrito em 1946 e é composto por mais de 20 antígenos, sendo alguns deles mais importantes que outros.
Esses antígenos são produtos do gene KEL e expressos na glicoproteína transmembrana N-glicosilada Kell e começam a ser expressos logo no início da vida; a partir da décima semana, podem ser detectados nas células do feto. Ao nascimento, estão bem desenvolvidos e são encontrados principalmente na linhagem eritroide, nos testículos e, em menor nível, no cérebro, nos tecidos linfoides e no tecido muscular, estando ausentes em plaquetas, linfócitos, granulócitos ou monócitos.
Geralmente, os anticorpos anti-Kell pertencem à classe IgG e apresentam maior imunogenicidade do que os dos sistemas ABO e Rh. Sendo assim, podem causar reações transfusionais e estão implicados na DHRN.
O sistema Duffy é composto por seis antígenos, sendo Fya e Fyb os mais importantes. Esses dois antígenos são produtos de alelos codominantes expressos na glicoproteína gpD, que é um receptor de citocinas na superfície das hemácias. Os antígenos do sistema Duffy são expressos nas hemácias e em tecidos como rim, coração, cérebro, pulmão, pâncreas, placenta, tireoide, entre outros. Eles não são expressos em linfócitos, monócitos e plaquetas.
Os quatro fenótipos no sistema Duffy são:
- Fy (a+b+)
- Fy (a+b-)
- Fy (a-b+)
- Fy (a-b-)
O fenótipo Fy (a-b-), raro em caucasianos e mais comum na população africana, é resultante de uma mutação que leva à ausência da expressão proteica nas hemácias. Esse fenótipo tem relevância clínica, pois confere resistência à malária.
Sabe-se que anticorpos anti-Fy são moderadamente imunogênicos. Assim, anti-Fya podem causar DHRN moderada e reações transfusionais. Por sua vez, anticorpos anti-Fyb são incomuns.
O sistema MN foi o segundo sistema de grupos sanguíneos a ser descrito, em 1927, por Landsteiner e Levine, quando encontraram anticorpos anti-M e anti-N no soro dos coelhos imunizados. Posteriormente, o antígeno S foi relatado por Walsh e Montgomery e, em 1951, foi descrito o alelo s.
Assim, o sistema MN transformou-se em MNSs e, atualmente, sabe-se que esse sistema é formado por 43 antígenos associados a sialoglicoproteínas de membrana e restritos à linhagem eritroide. São antígenos bem desenvolvidos ao nascimento.
A produção de anticorpos anti-M ou anti-N ocorre somente após sensibilização; assim, não haverá reação de incompatibilidade se um indivíduo que não tenha o antígeno M (M-) receber um sangue de um doador com antígeno M (M+), a não ser que ele esteja sensibilizado por transfusões anteriores e apresente o anticorpo anti-M.
O anticorpo anti-N é mais raro que o anti-M, estando raramente associado a DHRN e reações transfusionais. O anticorpo anti-S é mais comum do que o anti-s, mas ambos podem desencadear reações transfusionais hemolíticas moderadas a graves, assim como DHRN.
Além dos sistemas que já estudamos, existem ainda outros antígenos eritrocitários, como o sistema P, cuja expressão dos antígenos é influenciada por genes do sistema ABO, e o sistema I, presente em quase todos os adultos e o único expresso no sangue do cordão umbilical.
Esses antígenos não estão comumente envolvidos em reações transfusionais, mas podem causar hemólise se pacientes sensibilizados (que têm anticorpo contra o sistema P ou I) forem transfundidos com hemácias que apresentem esse antígeno.
Saiba mais
Nem todos os bancos de sangues têm os materiais necessários para conhecer os antígenos eritrocitários. Assim, no momento da seleção de bolsas de sangue para a transfusão, é feita a classificação sanguínea (sistema ABO e Rh) e Kell dos doadores e receptores para os pacientes imunodeprimidos (como os pacientes que recebem tratamento para câncer). Nos pacientes imunocompetentes (como pacientes com anemia falciforme), também é verificado o sistema Duffy, para garantir que os receptores tenham antígenos eritrocitários compatíveis.
Doença hemolítica do RN (DHRN/DHPN) por Rh ou ABO
A doença hemolítica perinatal (DHPN), ou doença hemolítica do recém-nascido (DHRN), compreende patologias que resultam da destruição ou diminuição da sobrevida dos eritrócitos do feto e/ou recém-nascido. Essa condição pode ser classificada em três categorias: DHRN por incompatibilidade sanguínea materno-fetal aos antígenos do sistema Rh, do sistema ABO e contra antígenos de outros sistemas eritrocitários.
A DHRN por anticorpo anti-D é grave na maioria dos casos, caracterizando-se por destruição acentuada das hemácias do feto. Essa condição é evidenciada por hiperbilirrubinemia, anemia profunda e hidropsia fetal, que muitas vezes evolui para o óbito.
Hiperbilirrubinemia
A hiperbilirrubinemia do recém-nascido é uma condição causada pelo acúmulo de bilirrubina no sangue, deixando a pele do bebê amarelada.
Atenção
É importante ressaltar que a incidência de DHRN por anticorpo anti-D tem diminuído graças ao acompanhamento pré-natal e à utilização da imunoglobulina humana anti-D nas mães não sensibilizadas.
Quando a gestante é Rh negativa e o feto é Rh positivo, eritrócitos fetais entram na circulação materna geralmente durante o parto e podem sensibilizar a mãe, que passa a produzir anticorpos anti-D. A mãe também pode ser sensibilizada anteriormente por transfusão de sangue, aborto prévio ou amniocentese, produzindo anticorpos anti-D. Uma vez sensibilizada, em uma nova gestação de filho Rh positivo, seus anticorpos anti-D poderão destruir as hemácias do bebê.
A principal forma de manejo é prevenir a formação de anticorpo anti-D em mulheres Rh negativas por meio da administração de anticorpos anti-D, que levam à remoção rápida dos eritrócitos fetais Rh positivos da circulação, antes que eles possam sensibilizar o sistema imunológico da mãe e ela comece a produzir anti-D. Quando realizada até 72 horas após o nascimento, a imunoprofilaxia com IgRh promove proteção de 98% a 99% contra a formação de anticorpos anti-D.
A classificação da DHRN como grave está relacionada à morte intrauterina por hidropsia fetal. Já na doença moderada, o bebê nasce com anemia e icterícia, podendo apresentar palidez, edema e hepatoesplenomegalia. Se o nível de bilirrubina não conjugada não for controlado, a deposição de pigmento biliar nos gânglios da base cerebral pode causar dano ao sistema nervoso central, com possibilidade de levar à deficiência intelectual, surdez e epilepsia. Na DHRN leve, o bebê apresenta anemia leve com ou sem icterícia.
A investigação laboratorial pode mostrar:
- Anemia variável com alta contagem de reticulócitos.
- A classificação sanguínea revela que o bebê é Rh positivo e a mãe negativa, o teste direto de antiglobulina (chamado de Coombs direto) é positivo e a bilirrubina está elevada.
- Em casos moderados e graves, são vistos eritoblastos abundantes no hemograma.
Coombs
Teste que detecta a presença de anticorpos ligados a antígenos eritrocitários.
Embora o anticorpo anti-D seja responsável pela maioria dos casos graves de DHRN, anticorpos anti-c, anti-E e anti-K também podem estar envolvidos. Além disso, sabe-se que anticorpos relacionados ao sistema ABO são a causa mais frequente de DHRN, mas a doença costuma ser leve.
A doença hemolítica por incompatibilidade do sistema ABO pode ocorrer em qualquer gestação (incluindo a primeira), podendo não afetar as gestações subsequentes, e se restringe aos recém-nascidos com tipo sanguíneo A ou B de mães do tipo O. Geralmente, a doença se apresenta com intensidade mais branda, com anemia leve e de fácil manejo.
O diagnóstico laboratorial da DHRN por incompatibilidade do sistema ABO compreende anemia, reticulócitos e hiperbirrubinemia indireta precoce. O diagnóstico sorológico pode ser confirmado por meio do teste de Coombs direto positivo nos eritrócitos do recém-nascido e incompatibilidade sanguínea materno-fetal.
A baixa gravidade da DHRN do sistema ABO pode ser explicada pela falta de desenvolvimento total dos antígenos A e B ao nascimento e pela neutralização parcial dos anticorpos IgG maternos pelos antígenos A e B em outras células, no plasma e nos fluidos dos tecidos.
Recomendação
Cabe ressaltar que todas as gestantes devem fazer tipagem dos sistemas ABO e Rh. A pesquisa de anticorpos irregulares deve ser feita ao menos duas vezes durante todas as gestações por meio do teste de Coombs.
Este vídeo apresenta as características dos sistemas Kidd e Diego, respectivos tipos de antígenos e anticorpos.
Verificando o aprendizado
ATENÇÃO!
Para desbloquear o próximo módulo, é necessário que você responda corretamente a uma das seguintes questões:
O conteúdo ainda não acabou.
Clique aqui e retorne para saber como desbloquear.
MÓDULO 3
Reconhecer métodos imuno-hematológicos para classificação sanguínea e diagnóstico de doenças relacionadas
Técnicas imunológicas
Diversas técnicas imunológicas são utilizadas no diagnóstico clínico de doenças infectocontagiosas e no monitoramento de tratamento por quimioterapia e radioterapia. São úteis, ainda, para a determinação do grupo sanguíneo de um indivíduo.
Essas técnicas possibilitam a detecção ou quantificação de anticorpos, antígenos e outras moléculas provenientes da interação Ag-Ac em amostras biológicas. Os testes utilizados para a detecção de anticorpos ou antígenos podem ser primários ou secundários.
Vamos conhecer um pouco mais sobre cada teste.
Verificam a interação direta entre Ag-Ac.
Exemplos: radioimunoensaio, imunofluorescência, ELISA.
Detectam as consequências da interação entre Ag-Ac ou mudanças no estado físico do antígeno.
Exemplos: imunodifusão, aglutinação, precipitação, fixação de complemento.
Além de possuir diversas aplicações, de forma geral, o imunodiagnóstico apresenta vantagens como:
- Rapidez
- Possibilidade de automação
- Kits comerciais padronizados
- Custo operacional relativamente baixo
A imuno-hematologia é uma das áreas que utiliza técnicas de imunodiagnóstico para estudar e classificar os grupos sanguíneos por meio de reações imunológicas entre aglutinógenos e anticorpos.
Os testes imuno-hematológicos pré-transfusionais realizados no sangue do doador e receptor são fundamentais e críticos para a realização de uma transfusão segura. Além disso, os testes imuno-hematológicos são rotineiramente empregados para verificar a compatibilidade sanguínea entre mãe e filho.
As metodologias mais utilizadas na imuno-hematologia são as técnicas em tubo, microplacas e gel teste.
A condução dos testes imuno-hematológicos no laboratório deve ser criteriosa e seguir as normas de biossegurança, o procedimento operacional padrão e todas as indicações das bulas dos fabricantes dos reagentes. Diversos fatores podem influenciar a qualidade dos ensaios imuno-hematológicos.
Saiba mais
- O sangue deve ser coletado de forma adequada em tubo apropriado.
- Devem ser utilizadas vidrarias limpas e sem resíduos de detergente, pois a presença de interferentes pode favorecer a formação de aglutinatos, levando a resultados falso-positivos.
- Deve ser utilizada a técnica adequada para separação do soro.
- As suspensões de hemácias com Salina (NaCl 0,9%) devem ser preparadas corretamente, uma vez que concentrações muito abaixo ou acima da ideal podem levar a resultados falsos negativos.
- É essencial verificar a qualidade dos reagentes e equipamentos empregados.
- Devem ser utilizados ensaios técnicos padronizados.
Práticas imuno-hematológicas: classificação do sistema ABO
Para conhecermos a classificação sanguínea em relação ao sistema ABO, é obrigatória a realização de duas provas, chamadas de prova direta e reversa. Para conhecê-las, clique a seguir.
Na prova direta, ou teste de Beth-Vincent, faz-se a pesquisa de antígenos fixados nas hemácias do indivíduo. Para isso, são utilizados soros (anticorpos anti-A, anti-B e anti-A, B) que apresentam a capacidade de reconhecer e ligar-se aos antígenos eritrocitários, permitindo a definição dos grupos sanguíneos: A, B, AB, O.
Na prova reversa, ou teste de Simonin, faz-se a pesquisa do anticorpo presente no soro (ou plasma) do indivíduo. Esse teste deve ser feito com hemácias com o tipo sanguíneo A e B conhecido. Essa prova é uma contraprova essencial para a conclusão da tipagem sanguínea, devendo ser sempre realizada, exceto em bebês com idade inferior a quatro meses de idade, isto porque os anticorpos do sistema ABO estão ausentes ao nascimento, sendo detectados após os primeiros meses de vida.
| Soro Anti-A | Soro Anti-B | Soro Anti-A+B | Hemácia A | Hemácia B | |
|---|---|---|---|---|---|
| Grupo A | |||||
| Grupo B | |||||
| Grupo AB | |||||
| Grupo O | |||||
| Ausência de aglutinação | Presença de aglutinação | ||||
É importante ressaltar que o anticorpo B geralmente apresenta título mais fraco que os demais anticorpos. As provas direta e reversa são complementares entre si. É possível ocorrerem discrepâncias por alterações nos antígenos, no soro/plasma ou devido a erros laboratoriais. Antes de o laudo laboratorial ser liberado, os resultados discrepantes devem ser esclarecidos.
Saiba mais
Em bebês com menos de quatro meses de idade, podemos observar a presença de anticorpos maternos durante a classificação sanguínea. Em pacientes imunodeprimidos, durante a prova reversa, podemos não observar os anticorpos devido à sua baixa produção nesses pacientes.
Atenção
Além dos quatro tipos sanguíneos conhecidos (A, B, AB, O), existem alguns subgrupos dos grupos A, B e AB. Os subgrupos do antígeno A e B apresentam algumas mutações no gene que codifica essas moléculas, o que leva a uma menor expressão e presença desses antígenos na membrana dos eritrócitos. Durante a classificação direta em pacientes com esses subgrupos, a baixa expressão desses antígenos gera uma reação fraca nos testes imunológicos, gerando discrepâncias entre a prova direta e a reversa.
Em bancos de sangue, a distinção entre os subgrupos A e B não apresenta relevância, pois normalmente a transfusão desses sorogrupos não leva a uma reação transfusional.
Práticas imuno-hematológicas: classificação do sistema RhD e pesquisa de D fraco
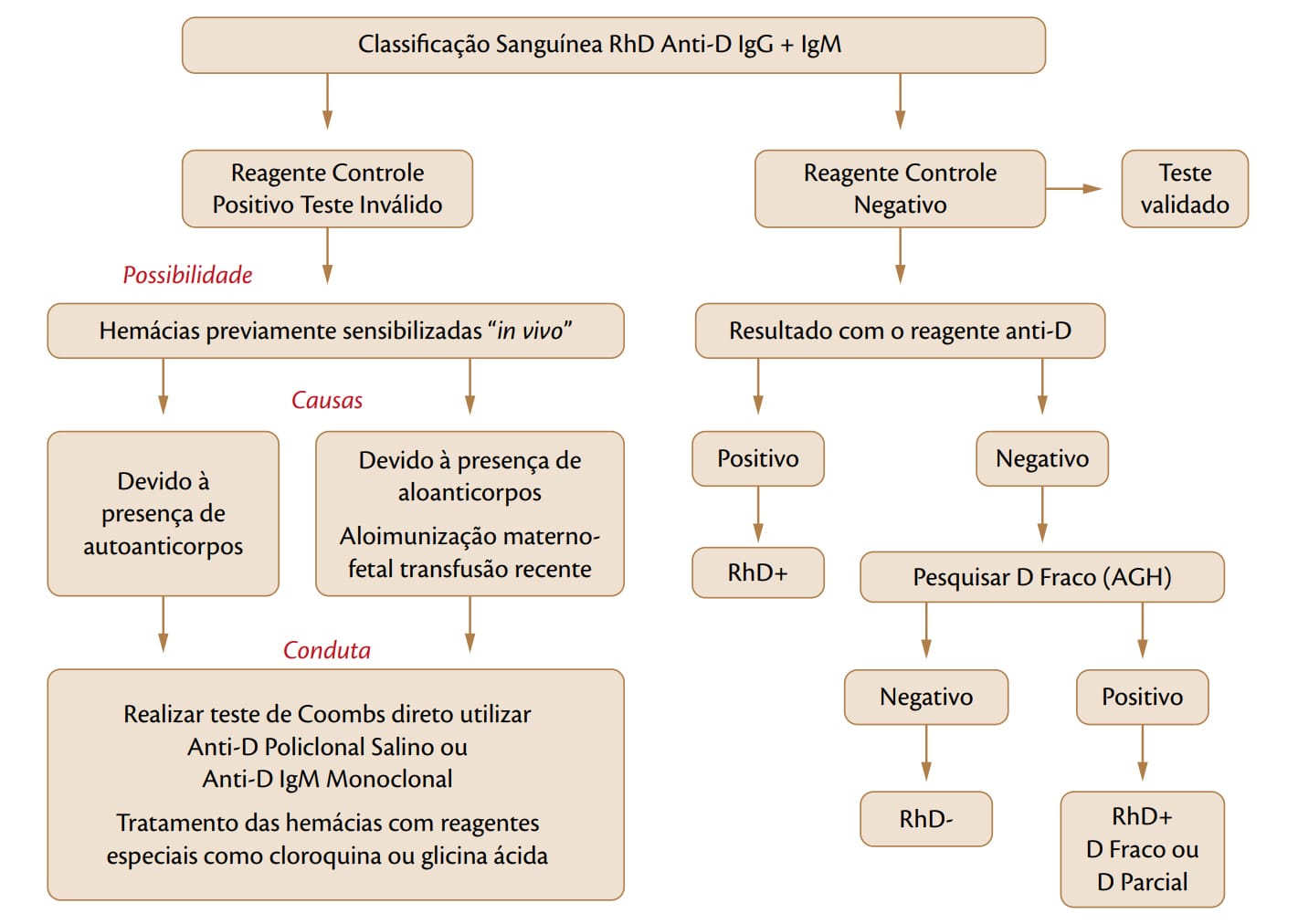
Diferentemente da tipagem do sistema ABO, a classificação do RhD refere‑se somente à presença ou ausência do antígeno RhD, não existindo prova reversa, pois os indivíduos não apresentam anticorpos naturais contra o antígeno Rh.
A classificação do Rh é feita pela tipagem direta, com a utilização de soros comerciais contendo anticorpos anti-D monoclonais ou policlonais, que identificam a presença de antígenos na superfície dos eritrócitos, classificando os indivíduos como RhD positivo (aglutinação direta) e RhD negativo (ausência de aglutinação).
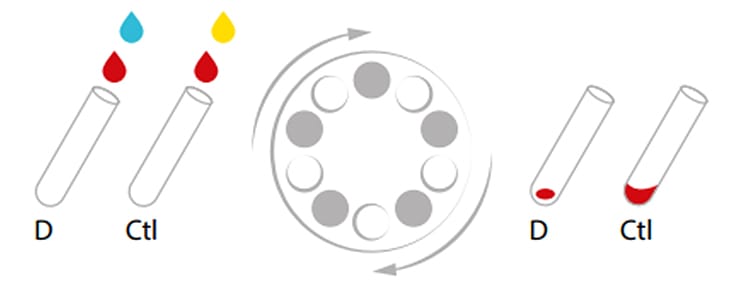
A pesquisa de D fraco deve ser feita sempre que a classificação do RhD for negativa, isto é, quando não houver aglutinação. A classificação correta do sistema RhD e de suas variantes tem grande relevância, uma vez que esse antígeno é o mais imunogênico quando comparado aos demais antígenos eritrocitários conhecidos até o momento.
Assista ao vídeo a seguir, em que o especialista apresenta os testes Beth-Vincent (prova direta) e Simonin (prova reversa), demonstrando como se complementam.
Práticas imuno-hematológicas: teste de Coombs
O teste da antiglobulina humana ou teste de Coombs foi descoberto em 1945 e destina-se à pesquisa de anticorpos e proteínas do sistema complemento. O sistema imunológico pode produzir anticorpos contra eritrócitos nos seguintes casos:
- Anemia hemolítica
- Leucemia linfocítica crônica
- DHRN
- Mononucleose infecciosa
- Sífilis
- Lúpus eritematoso sistêmico
- Reação transfusional
Vamos conhecer um pouco mais sobre os testes.
O teste de Coombs direto ou teste da antiglobulina direto (TAD) é um teste que detecta anticorpos (gamaglobulinas) do tipo IgG ou fração do sistema complemento que estão ligados às hemácias. Esses anticorpos podem ser produzidos pelo próprio organismo ou recebidos durante uma transfusão de sangue.
O TAD é realizado com suspensão a 5% de eritrócitos do paciente em soro fisiológico e adição do soro de Coombs (anticorpo anti-Ig humano, que reconhece uma região do IgG). Posteriormente, a mistura é centrifugada para a verificação da aglutinação. A presença de aglutinação (TAD positivo) indica sensibilização (anticorpos ligados a hemácias).
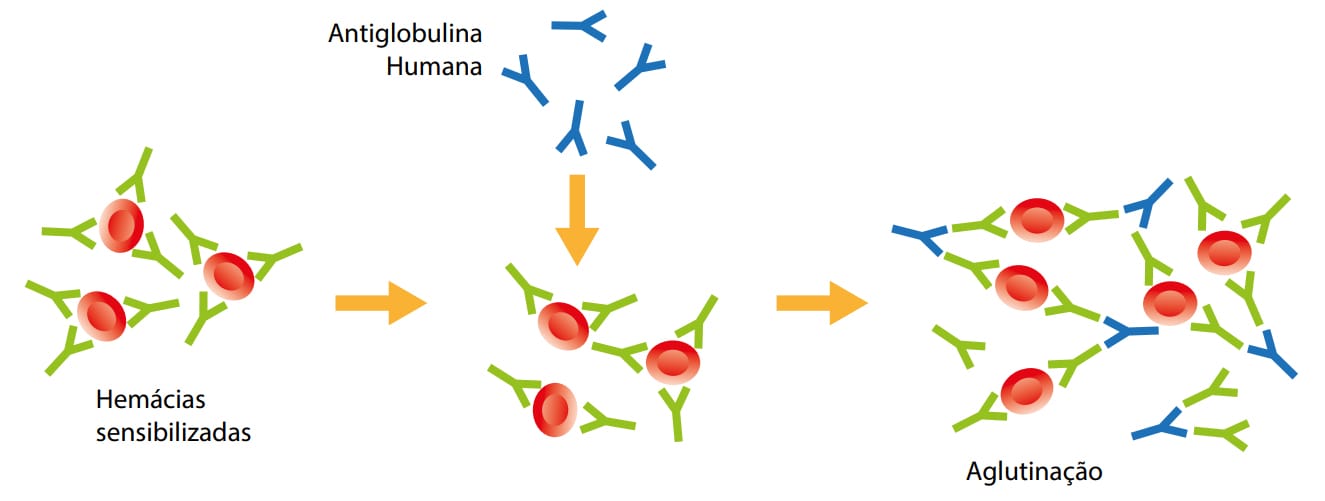
Uma das maiores aplicações do teste de Coombs direto é na pesquisa da DHRN. Nas mães com o fator Rh negativo com o recém-nascido com fator Rh positivo, a realização do TAD permite verificar se a mãe produziu anticorpos anti-Rh e se estes atingiram o bebê, podendo levar ao desenvolvimento da doença.
Além de casos de DHRN, a realização do TAD é indicada em casos de anemia hemolítica autoimune, anemia induzida por medicamentos e na reação transfusional. O TAD positivo não significa que o paciente necessariamente apresenta anemia hemolítica autoimune e o teste negativo não exclui hemólise imune. Assim, todo paciente com TAD positivo deve ser submetido a uma avaliação clínica criteriosa e a testes adicionais.
O teste de Coombs indireto ou teste da antiglobulina indireto (TAI) é frequentemente utilizado na identificação e detecção de anticorpos presentes no soro. Esses anticorpos podem atacar os eritrócitos, mas não estão ligados a eles, sendo chamados de anticorpos irregulares, incompletos ou não aglutinantes.
Normalmente, realiza-se este teste para detectar a presença de anticorpos no sangue de um receptor ou doador antes de uma transfusão. Além disso, tem utilidade no acompanhamento pré-natal, sendo possível proteger os bebês no início da gestação, caso a mãe tenha sangue Rh negativo.
O teste é realizado incubando-se o soro ou plasma do paciente com hemácias reagentes de triagem e, após incubação a 37 °C com potencializadores, como albumina, o soro de Coombs é adicionado, misturado e centrifugado para a verificação da aglutinação.
Esse teste é utilizado como uma triagem para pesquisa de anticorpos irregulares; caso o TAI apresente resultado negativo, isso indica que a amostra testada não tem anticorpos livres (irregulares), que reagiriam, assim, com eritrócitos. De forma diferente, TAI positivo indica a presença desses anticorpos, sendo necessários testes adicionais para identificar qual anticorpo foi formado, pesquisando-se, assim, os diferentes tipos de antígenos eritrocitários (sistemas Rh, Duffy, Lewis, Kell, MNS, dentre outros).
Na gestante ou na mulher Rh negativa que esteja planejando engravidar, o teste de triagem positivo pode ser indicativo da presença de um anticorpo anti-Rh, ou seja, sugere que a mãe foi sensibilizada, e deve ser realizada a testagem sanguínea no feto e o acompanhamento médico para evitar riscos ao bebê. Caso o teste seja negativo, isso indica que a mãe não foi sensibilizada. Durante o pré-natal, esse teste é sempre solicitado.
Agora, como fazemos a compatibilidade entre doadores e receptores de sangue?
Durante os exames transfusionais para transfusões de concentrados de hemácias (CH), devemos fazer a classificação sanguínea (ABO e Rh) e a pesquisa de anticorpos irregulares (TAI) no receptor e no doador.
Além disso, deve-se fazer a prova cruzada, que consiste em verificar se o receptor tem anticorpos contra algum antígeno eritrocitário do doador, o que pode levar a uma reação transfusional.
Para isso, é realizada a testagem do soro ou plasma do paciente (receptor) com as hemácias do possível doador e é verificada a presença de aglutinação. Caso haja aglutinação, o receptor não pode receber aquela bolsa de CH e o sangue de outros doadores deve ser compatibilizados.
Atenção
Caso a pesquisa de anticorpos irregulares (TAI) no paciente (receptor) seja positiva, mostrando a presença de anticorpos irregulares, e a prova cruzada, negativa, o paciente pode receber o sangue, pois, como não ocorreu aglutinação na prova cruzada, o doador não apresenta antígenos eritrocitários que interajam com o anticorpo irregular produzido pelo paciente. No entanto, devemos realizar testes adicionais para descobrir qual anticorpo irregular o paciente desenvolveu.
Fala, mestre!
No vídeo apresentado por Mariele de Jesus sobre biomédica, o tema abordado é o mapa de risco e seu objetivo. O vídeo ensina como identificar diferentes tipos de risco no laboratório, tais como risco químico, risco físico, risco biológico, risco ergonômico e risco de acidentes, bem como a importância dos Equipamentos de Proteção Individual (EPIs) e Equipamentos de Proteção Coletiva (EPCs). Cada tipo de risco é associado a uma cor específica e exemplos práticos são fornecidos para ilustrar cada um. Também é destacada a importância do uso adequado dos EPIs para minimizar riscos de acidentes e questões ergonômicas no ambiente de trabalho. Por fim, os alunos são incentivados a identificar os riscos em seus próprios laboratórios e desenvolver um mapa de risco.
Fala, mestre!
No vídeo apresentado pela biomédica Mariele de Jesus, o objetivo é ensinar sobre vidrarias e equipamentos de laboratório, enfatizando a identificação de vidrarias e a correta utilização dos equipamentos. A aula aborda a higienização das mãos e o uso de luvas, seguidos de tutoriais sobre como realizar a pesagem de substâncias na balança, preparar soluções utilizando um agitador magnético, e medir volumes com uma bureta. Marielle também demonstra como utilizar diferentes tipos de pipetas (graduada e automática) para medir e transferir líquidos com precisão. O vídeo fornece orientações passo a passo para garantir o manuseio seguro e correto dos equipamentos laboratoriais.
Verificando o aprendizado
ATENÇÃO!
Para desbloquear a conclusão, é necessário que você responda corretamente a uma das seguintes questões:
O conteúdo ainda não acabou.
Clique aqui e retorne para saber como desbloquear.
Conclusão
Considerações Finais
Ao longo desta jornada, apreendemos como o sistema imunológico está ordenado para defender o organismo contra patógenos invasores por meio da imunidade inata e adquirida. Entendemos a importância dos anticorpos e como se dá a interação específica com os diversos antígenos a que estamos expostos diariamente.
Visitamos os antígenos eritrocitários e vimos como podem ser classificados esses antígenos em diferentes sistemas, sendo que os sistemas ABO e Rh apresentam maior relevância clínica, uma vez que estão envolvidos em reações transfusionais e na doença hemolítica do recém-nascido. Entretanto, o sistema Rh é capaz de causar as formas mais graves dessa doença.
Além disso, entendemos os princípios dos métodos imuno-hematológicos utilizados na rotina laboratorial para a determinação dos tipos sanguíneos e detecção de anticorpos produzidos contra eritrócitos, identificando sua importância na prática clínica.
Podcast
CONQUISTAS
Você atingiu os seguintes objetivos:
Descreveu os componentes e as funções das respostas imunes inata e adquirida e a interação antígeno-anticorpo
Identificou os principais sistemas eritrocitários humanos e as doenças associadas
• Reconheceu métodos imuno-hematológicos para classificação sanguínea e diagnóstico de doenças relacionadas















As imunoglobulinas podem ser classificadas em cinco diferentes isotipos: IgA, IgD, IgE, IgG e IgM.