Apresentação
Você vai estudar o papel da fisiologia cardiovascular no controle da homeostase corporal. Conhecer a organização do sistema cardiovascular, o controle do ritmo cardíaco e a regulação da hemodinâmica é essencial para entender o débito cardíaco, o retorno venoso, a distribuição do fluxo sanguíneo e o controle da pressão arterial em diversas situações fisiológicas. Esse conhecimento é crucial para profissionais que desejam atuar na área da saúde.
OBJETIVOS
Módulo 1
Descrever a organização do sistema cardiovascular
Módulo 2
Compreender os mecanismos responsáveis pelo controle do ritmo cardíaco
Módulo 3
Reconhecer os fenômenos associados à função miocárdica e seu papel na manutenção do débito cardíaco e retorno venoso
Módulo 4
Comparar as respostas hemodinâmicas relacionadas à redistribuição do fluxo sanguíneo e à manutenção da pressão arterial
MÓDULO 1
Descrever a organização do sistema cardiovascular
Visão geral do sistema cardiovascular
Visão geral do sistema cardiovascular
Neste vídeo, você conhecerá a estrutura e a função do sistema cardiovascular na manutenção da homeostase corporal. Assista!
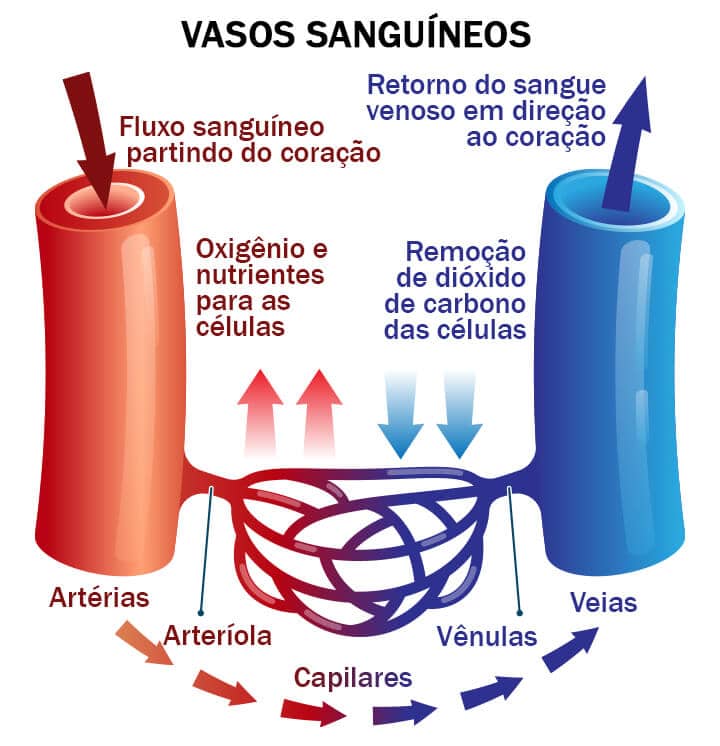
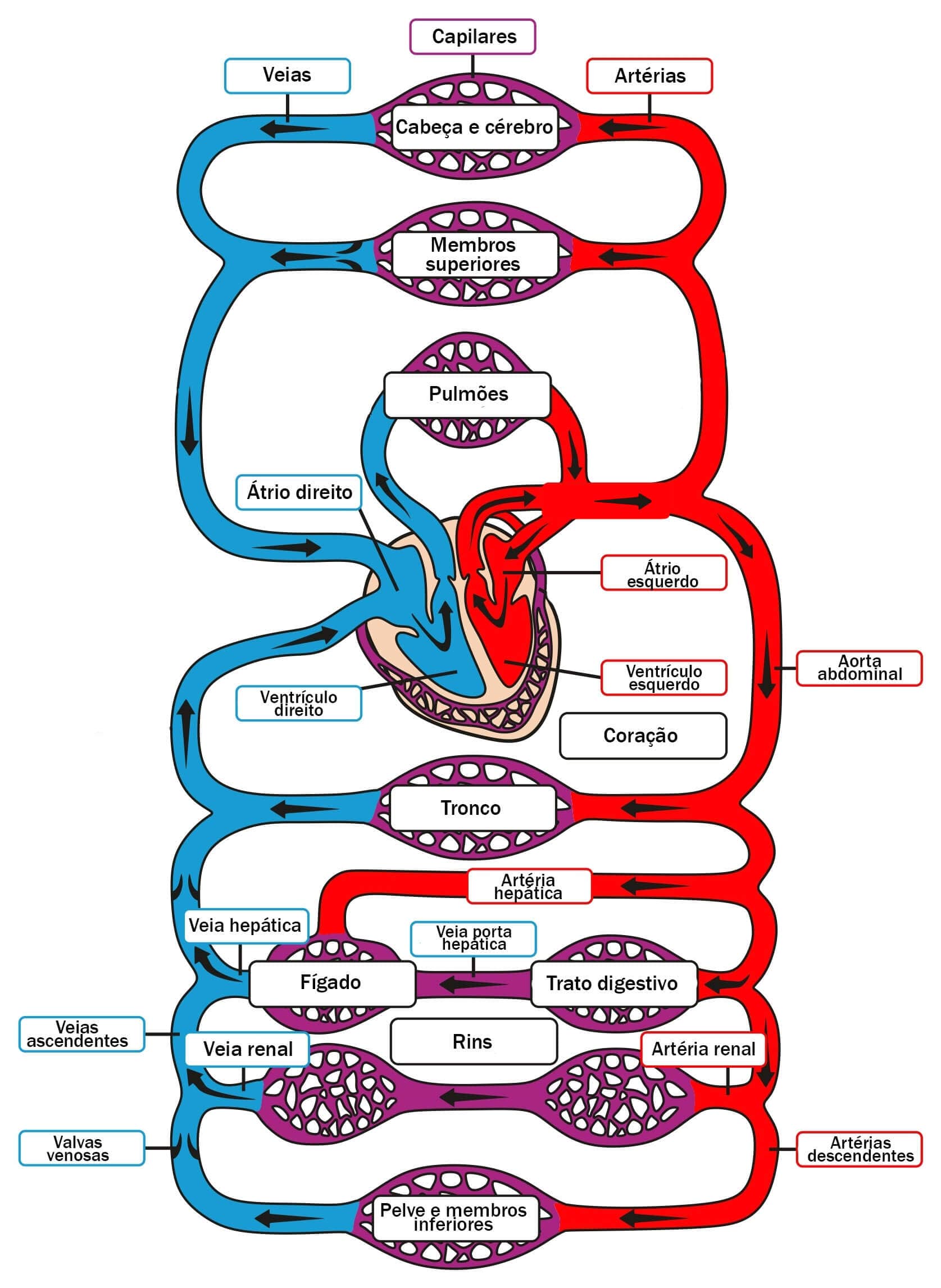
A partir de agora você vai começar a estudar a organização do sistema cardiovascular. Ele é dividido em arterial e venoso, por isso é denominado “sistema duplo e fechado”. O órgão principal, o coração, é reconhecido como uma bomba capaz de impulsionar quantidades relevantes de sangue para a periferia. Além do coração, o sistema cardiovascular compreende uma rede de vasos de distribuição de sangue e de coleta de resíduos metabólicos que são as artérias e veias, respectivamente.
À medida que o sangue flui para as estruturas vasculares distantes do coração, os grandes vasos se ramificam em uma extensa rede de microvasos, denominados arteríolas e capilares, responsáveis pela realização das trocas de nutrientes e oxigênio com os tecidos.
Os vasos arteriais e venosos apresentam diversidade estrutural e funcional. Veja o significado de cada um deles:
Sistema arterial
Pode ser considerado como um sistema de alta resistência e pressão e de baixo volume – por isso que um sangramento arterial é em forma de jato de sangue de coloração vermelho vivo.
Sistema venoso
Compreende um sistema de baixa resistência e pressão e de alto volume – por isso, quando ocorre um sangramento venoso, observamos um comportamento em forma de escorrimento e cianótico (vermelho escuro).
Atividade 1
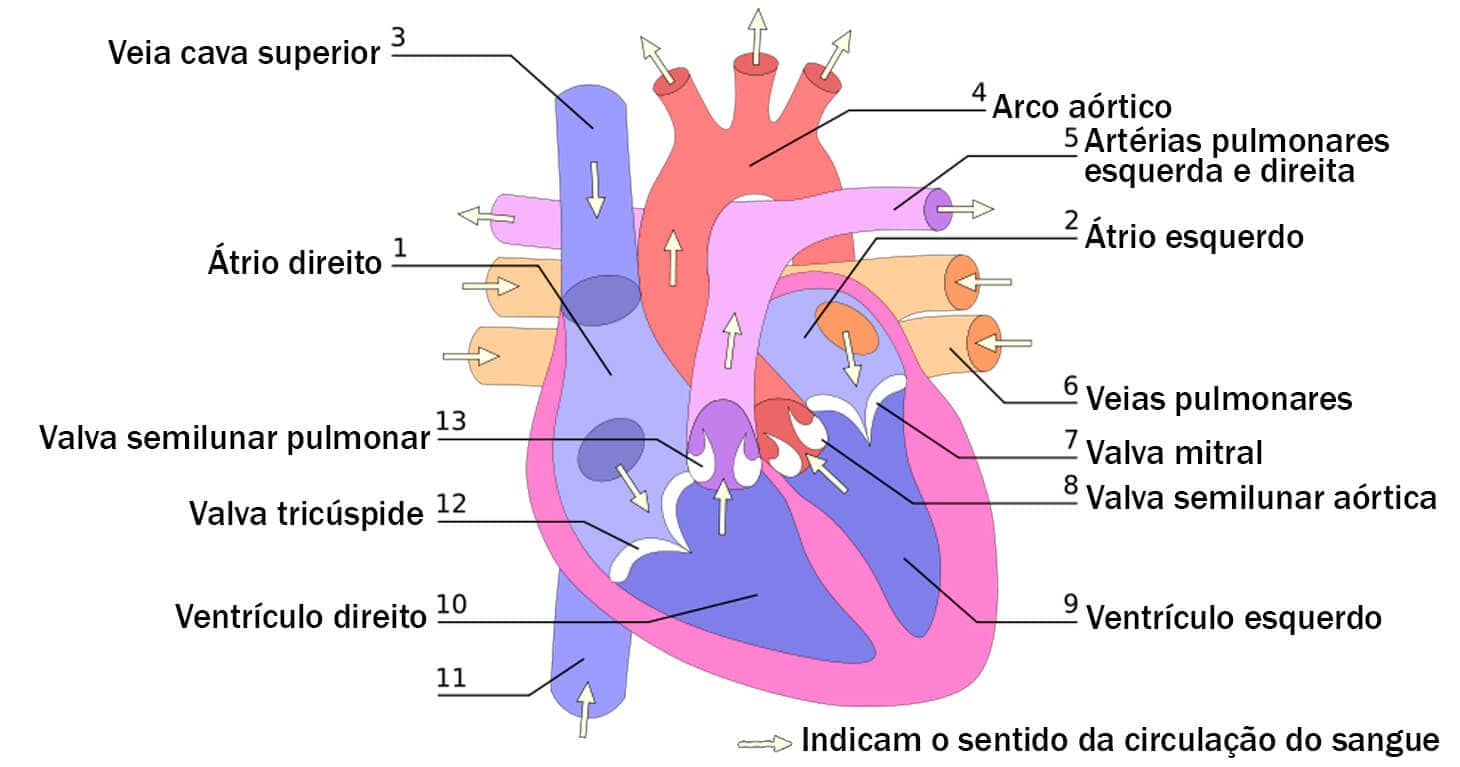
O principal responsável pelo direcionamento de sangue para os tecidos é o coração. Este órgão pode ser analisado estrutural e funcionalmente através das diferenças em suas câmaras dos dois lados (direito e esquerdo), organizadas da seguinte maneira:
Pelo lado direito, o sangue flui através do átrio para o ventrículo direito e daí para os pulmões (a pequena circulação ou pulmonar).
Em seguida, o sangue agora arterializado retorna ao coração para o átrio esquerdo, deste para o ventrículo esquerdo, e depois para a circulação sistêmica (a grande circulação ou sistêmica).
No coração de uma pessoa saudável, as características observadas no diâmetro interno da cavidade, bem como em relação às espessuras de cada câmara do coração, diferem consideravelmente. Isso se dá pelo fato de existir uma relação muito importante com a função de cada uma delas, por exemplo, os átrios, durante a contração (também chamada de sístole atrial), desenvolvem baixas pressões e por este motivo apresentam paredes relativamente finas.
Já os ventrículos direito e esquerdo, que precisam bombear o sangue através das artérias pulmonares e aórtica, respectivamente, com pressões relativamente elevadas, apresentam paredes muito mais espessas quando comparadas aos átrios.
As principais diferenças observadas nas estruturas dos ventrículos direito e esquerdo podem ser assim resumidas:
O ventrículo esquerdo apresenta a espessura de sua parede maior que aquela do ventrículo direito e trabalha em uma condição de alta pressão para efetivar o bombeamento de sangue para a circulação sistêmica.
Já o ventrículo direito apresenta tanto uma dimensão interna quanto a espessura de parede reduzida, se comparado ao ventrículo esquerdo. Isto ocorre pelo fato de o ventrículo direito não precisar de pressão tão elevada para bombear o sangue em direção aos pulmões.
Na divisão dos átrios e ventrículos, observamos estruturas fibrocartilaginosas responsáveis por garantir o fluxo de sangue dos átrios para os ventrículos – são denominadas como valvas atrioventriculares.
Atenção
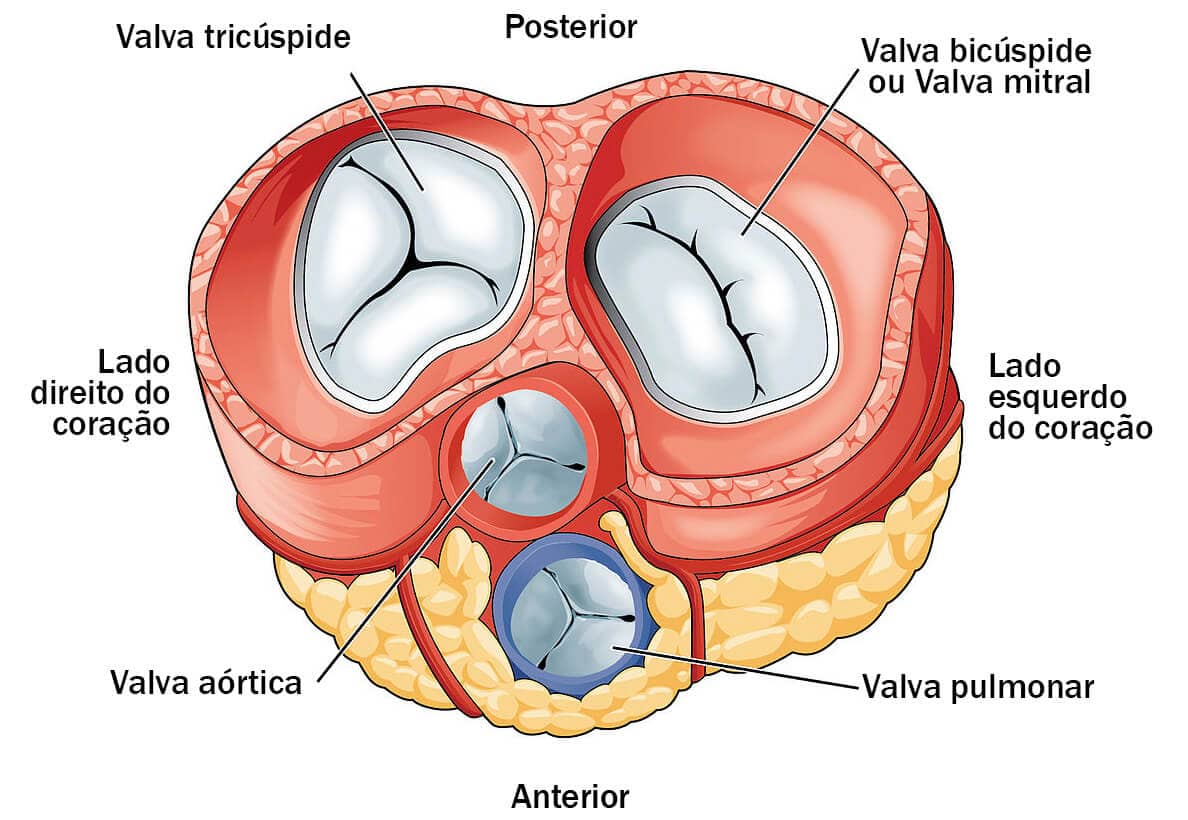
É possível notar a presença de quatro valvas cardíacas: além das duas atrioventriculares, existem outras duas responsáveis pela saída de sangue dos ventrículos em direção às artérias pulmonares e aórtica, respectivamente, essas valvas são denominadas como semilunares pulmonar e aórtica.
A abertura das valvas atrioventriculares permite que o sangue seja direcionado dos átrios em direção aos dois ventrículos (mais adiante, no ciclo cardíaco, visualizaremos que isso ocorre durante a fase de diástole ou relaxamento ventricular). Após o fechamento das valvas atrioventriculares, o sangue é transportado para as artérias pulmonares (lado direito) e aorta (lado esquerdo, durante a contração dos dois ventrículos, a sístole ventricular). Veja na imagem a seguir.
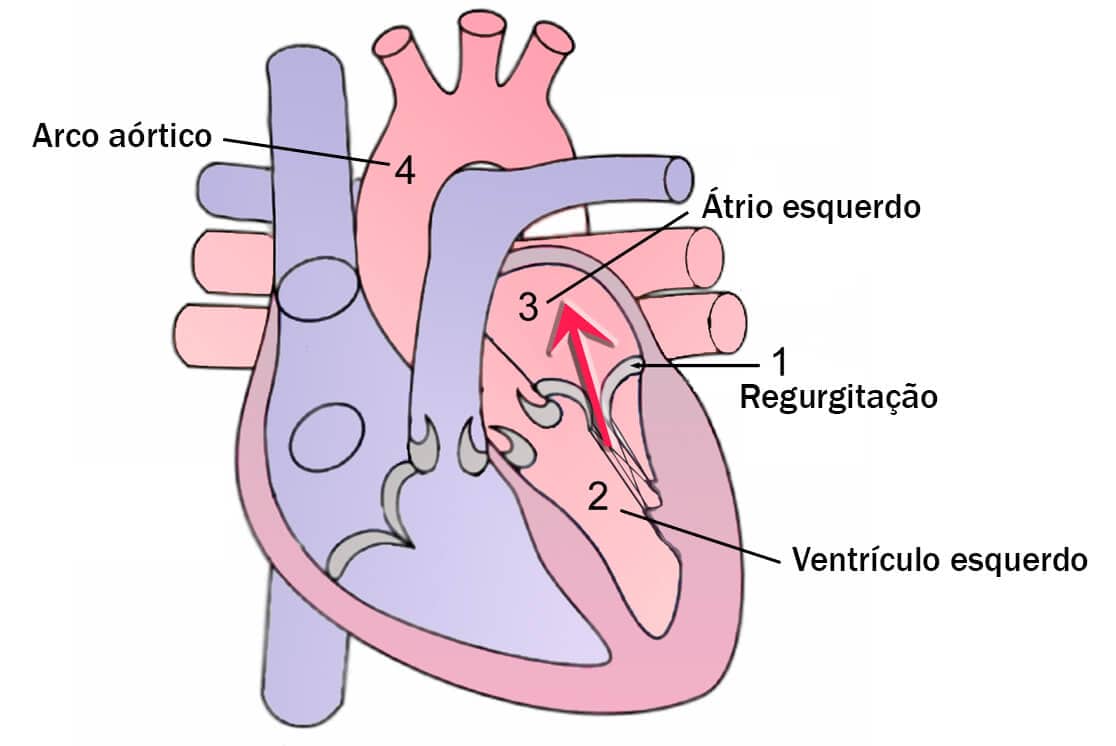
O correto fechamento destas valvas depende dos músculos papilares, estruturas localizadas na parede interna dos ventrículos que, por sua vez, são conectadas as essas valvas pelas cordas tendíneas. Quando ocorre a sístole ventricular, as cordas tendíneas são responsáveis por realizar a tração dos folhetos dessas valvas, mantendo-as fechadas e impedindo que o sangue seja direcionado de volta aos átrios, fenômeno denominado regurgitação.
À medida que o sangue é direcionado dos ventrículos para as artérias aorta e pulmonares, ele passa por valvas com denominação semelhante a estas estruturas, valvas semilunares aórtica e pulmonar, respectivamente, constituídas cada uma por três folhetos. A organização estrutural dessas valvas permite que o sangue ejetado pelo ventrículo flua para as artérias correspondentes, impedindo assim seu retorno durante a fase de relaxamento (diástole) (AIRES, 2018, p. 381).
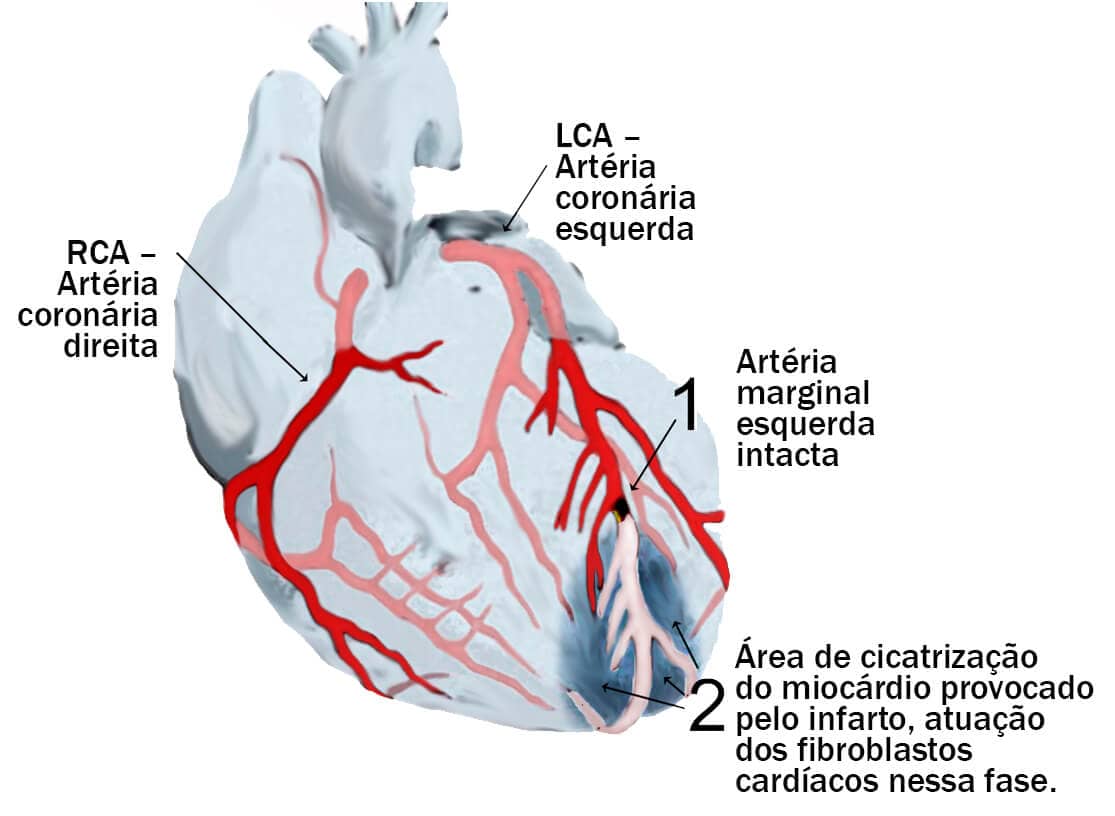
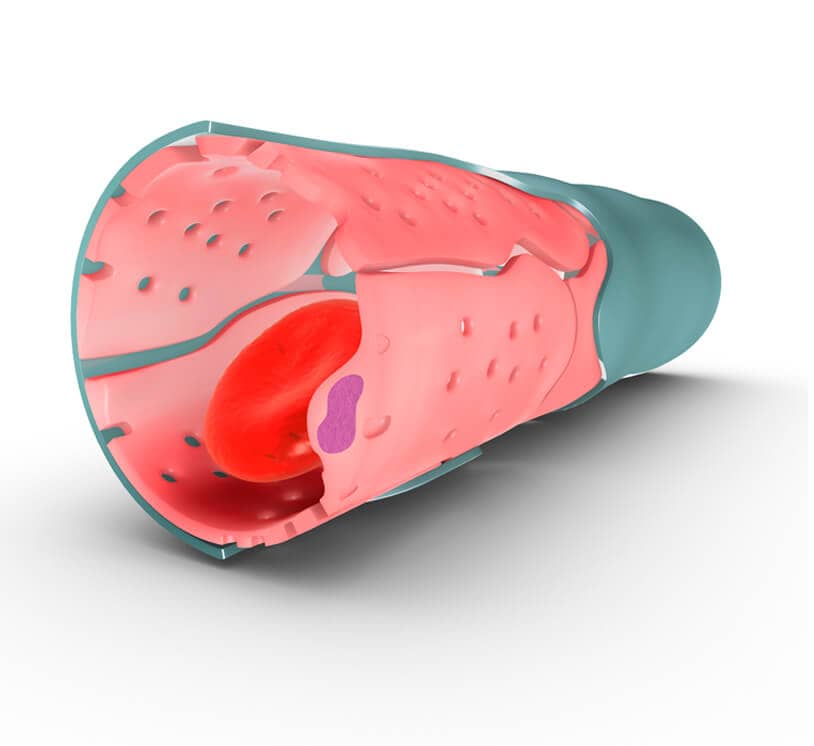
Além dos miócitos atriais e ventriculares, o tecido cardíaco é repleto fibroblastos cardíacos, responsáveis pela produção da matriz extracelular que é composta por colágeno do tipo I e III, capazes de desempenhar o processo de remodelamento miocárdico (também denominado como cicatrização do miocárdio durante o infarto, veja a imagem).
Devido à presença dessas células, durante o infarto do miocárdio os fibroblastos cardíacos migram para a região da lesão e promovem a deposição do colágeno (I e III). Como resultado teremos a cicatrização do coração (área escura na imagem, representada pelo número 2).
Atividade 2
ESTRUTURA DOS VASOS SANGUÍNEOS
O sistema vascular é formado pelos sistemas arterial e venoso, constituídos por uma rede de tubos, compreendendo uma extensão total de 50.000 km, que transportam cerca de 10.000 litros de sangue diariamente. Em relação aos seus aspectos estruturais e funcionais, as artérias e veias apresentam diferenças em seu conteúdo proteico (colágeno e elastina em suas camadas).
Essas diferenças impactam na resistência e na capacitância desses vasos.
Em relação às suas estruturas, observam-se três camadas denominadas túnicas diferentes, modificadas conforme a função do vaso:
A camada mais externa do vaso é chamada de adventícia;
A intermediária é a camada média onde encontra-se o músculo liso;
E a camada mais interna é a íntima, composta pelas células endoteliais.
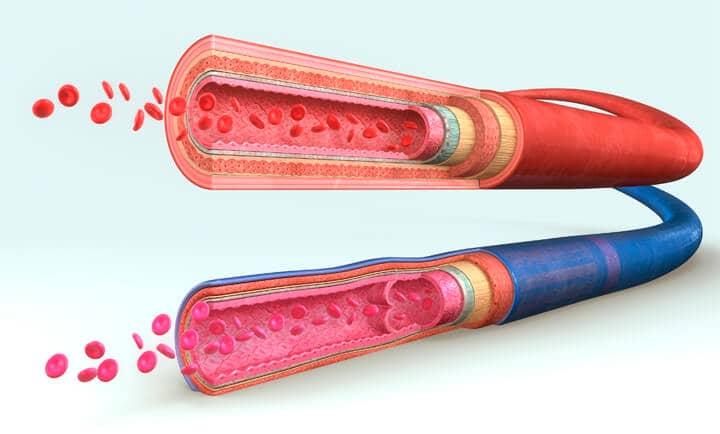
Quanto à espessura da parede desses vasos, notamos que ela possui relação direta com a pressão gerada no sistema, que é característico de cada região. Por exemplo, a espessura das artérias é muito maior do que a espessura das veias. Esta característica está relacionada com a composição das três camadas em cada artéria ou veia, como se vê na imagem a seguir.
Aspectos morfofuncionais do sistema vascular
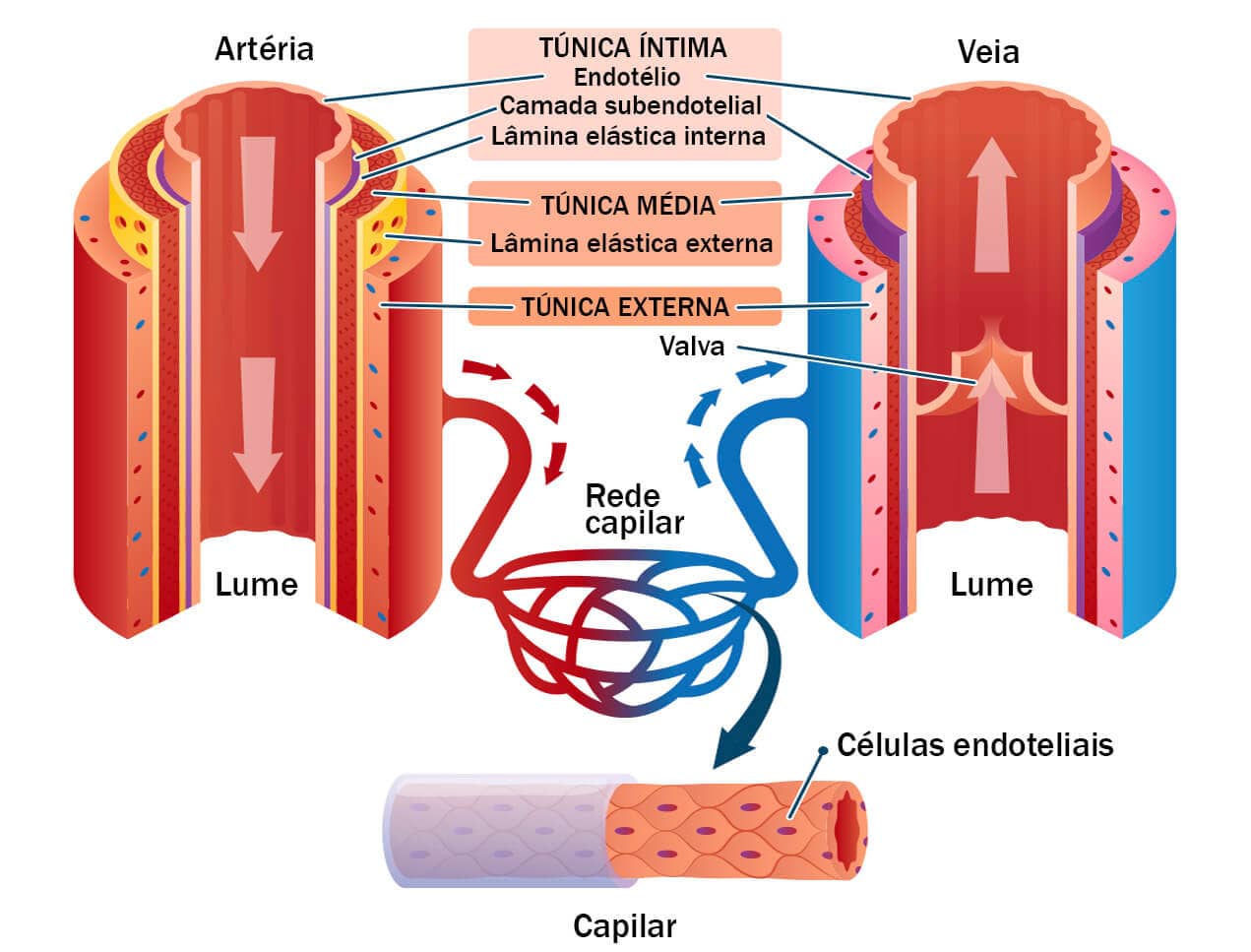
Basicamente, as artérias e as veias apresentam três camadas.
A túnica íntima (mais interna) é constituída por uma camada única de células endoteliais, recobertas por uma lâmina subendotelial. Na camada subendotelial, além da presença de fibras colágenas (matriz extracelular), nota-se a presença de células musculares lisas, além de fibrócitos e macrófagos. É dividida da túnica média por uma estrutura denominada camada elástica interna. A estrutura da túnica média sofre variação de acordo com sua capacidade contrátil e elástica; em função disso, os dois principais componentes da túnica média são as células musculares lisas e as lâminas elásticas presentes entre estas células. Externamente, a túnica média é cercada por uma lâmina elástica, reconhecida como camada elástica externa, que a separa da túnica adventícia.
Já a túnica adventícia é constituída predominantemente por tecido conjuntivo frouxo, contendo grande quantidade de fibrócitos, fibras elásticas e colágeno.
Atenção
Quando comparamos as diferenças de fluxo nos sistemas arterial e venoso, notamos que este parâmetro é drasticamente reduzido nas artérias de pequeno calibre assim como nas arteríolas. Nas metarteríolas (porções finais das arteríolas), devido ao seu pequeno diâmetro (cerca de 10 e 40 mm) e pelo fato de serem pouco inervadas, a camada muscular é incompleta, mas complementada pela presença de um forte esfíncter muscular pré-capilar.
Na rede arterial, os valores pressóricos são maiores que em qualquer outra região do sistema vascular, no entanto, quando o sangue atinge as arteríolas, ocorre uma queda acentuada na pressão do sistema. O motivo principal para que ocorra essa grande variação hemodinâmica é o aumento da resistência ao fluxo criada por esses pequenos vasos.
Desse modo, a partir dos capilares sanguíneos, a pressão e o fluxo sanguíneo serão bastante reduzidos. Como o sistema arterial é considerado um sistema de alta pressão e baixo fluxo, a quantidade total de sangue presente neste sistema é cerca de 20%, enquanto nos capilares é de 5% por causa de seu tamanho reduzido. Nas veias é de cerca de 75%, denotando sua função como reservatório de volume.
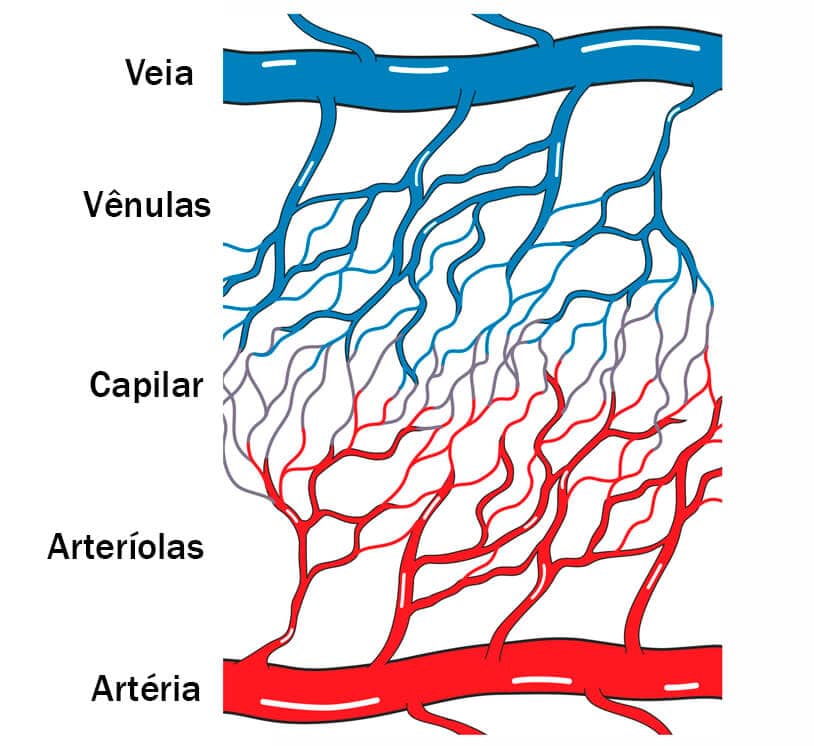
A microcirculação possui vasos terminais, com grande capacidade para realização de trocas de substâncias, e é constituída por pequenas artérias, arteríolas, capilares e vênulas. Nos capilares, sua parede é constituída por uma única camada de células endoteliais. Tal fato favorece o transporte satisfatório de nutrientes e oxigênio dos capilares para os tecidos e destes para a remoção de metabólitos.
Atenção
Independentemente da ausência de células musculares lisas nestes pequenos vasos, as variações em seus diâmetros são controladas por células que fazem parte de sua estrutura externa (uma espécie de adventícia) denominadas pericitos. Eles possuem alta habilidade em controlar o diâmetro dos vasos, atuando no controle do fluxo sanguíneo. Além dos capilares, as trocas de metabólitos também podem ocorrer através das paredes de pequenas arteríolas, antes mesmo de o sangue alcançar a região.
A função principal do sistema venoso é transportar o sangue de todas as veias em direção ao coração. Neste sentido, o sangue, ao trafegar pelos capilares, será transportado para as vênulas, seguindo para as veias de pequeno, médio e grande calibre.
Contudo, ao contrário do sistema arterial, o venoso é considerado um sistema de baixa pressão. Pelo fato de as veias serem maiores em número e tamanho que as artérias, elas conseguem apresentar maior capacidade de acomodação de sangue, motivo pelo qual são considerados vasos de capacitância.
Assim, o sistema venoso é responsável em estocar uma proporção muito elevada de sangue (cerca de 75% do total). Por ser um sistema de baixa pressão e alto volume, o sangue é impedido de fluir no sentido contrário ao coração pela presença das valvas venosas, possibilitando o fluxo de sangue pelas veias ocorrer sempre no sentido unidirecional, em direção ao coração.
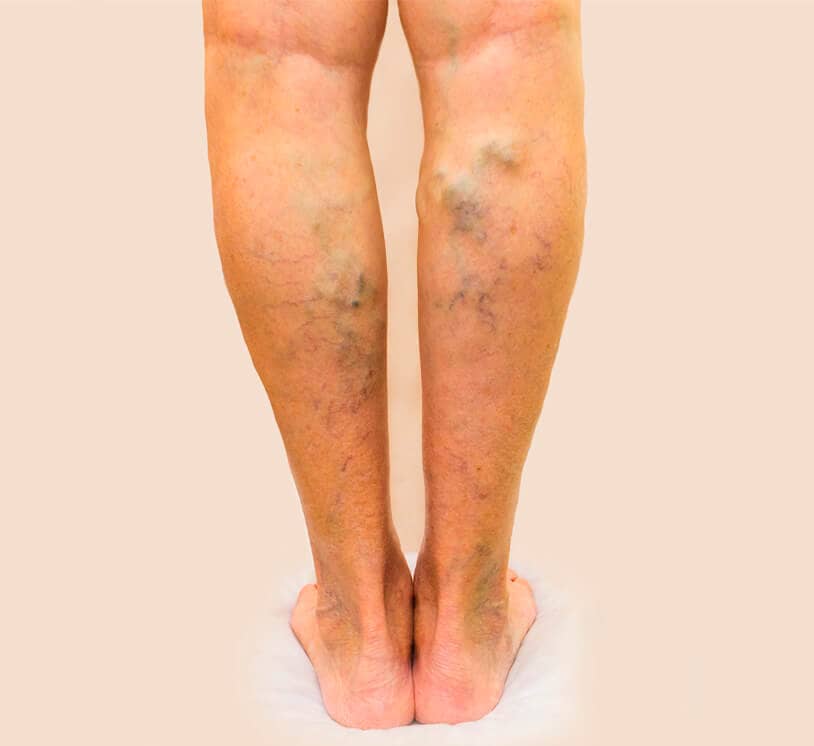
Certamente você já ouviu falar em varizes ou veias varicosas, mas o que isso de fato representa?
Aplicação prática
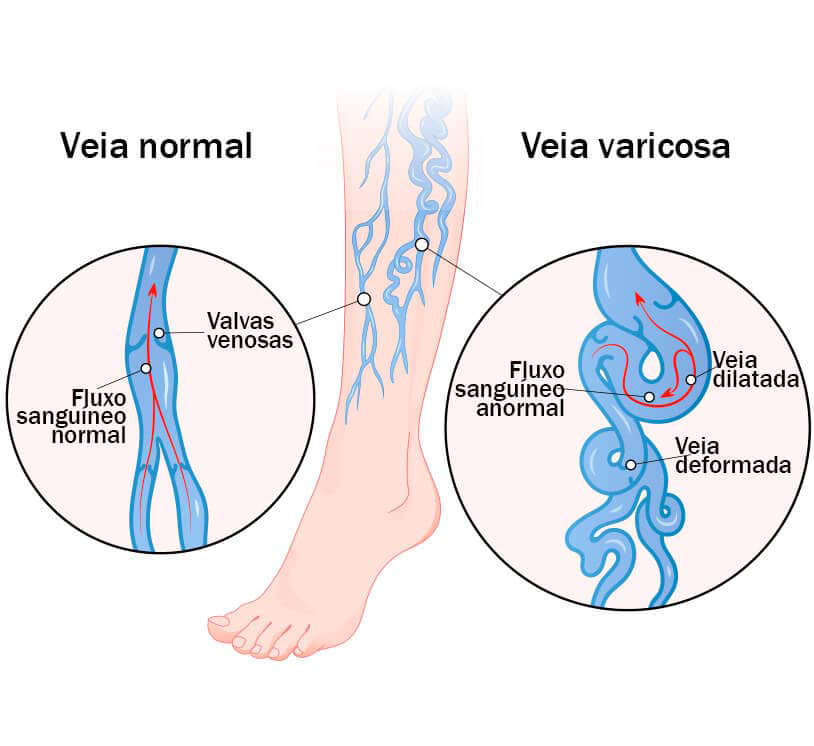
As varizes nas veias representam regiões onde as valvas venosas se tornam insuficientes ou incompetentes, reduzindo o fluxo de sangue nessa região (imagem à esquerda). Isso provoca dilatação excessiva das veias (imagem à direita), o que pode acarretar dores e desconforto local, levando pacientes ao tratamento com laser, clínico/cirúrgico ou estético.
Atividade 3
Circulação sistêmica
A circulação sistêmica inicia-se no ventrículo esquerdo.
A partir desta câmara, o sangue arterial é direcionado para a artéria aorta e, em seguida, para todos os tecidos (grande circulação).
À medida que o sangue segue, ele é direcionado para o sistema de artérias que serão distribuídos para os tecidos (exceto aos pulmões).
As artérias se dividem em numerosas estruturas menores, denominadas arteríolas, cujo calibre pode ser alterado por diversos mecanismos neurais ou metabólicos. As alterações do calibre das arteríolas podem regular tanto a pressão como o fluxo ao longo da circulação sistêmica.
Uma vez nos tecidos, as arteríolas se bifurcam em estruturas cada vez menores, denominadas capilares ou sinusóides. Nesses pequenos vasos, o oxigênio e os nutrientes são transportados em direção ao espaço extracelular e daí para as células. Ao mesmo tempo, os resíduos produzidos em função do metabolismo celular, passam das células para o fluido extracelular e, em seguida, para o sangue. Neste momento, o sangue é coletado por um sistema de muito baixa pressão, constituídos em sequências pelas vênulas e veias, que transportam o sangue venoso de volta ao coração.
Essa rede venosa drena uma quantidade significativa de sangue, cerca de 75% do volume total. Todas as veias se unem para formar as veias cavas superior e inferior, que direcionam o sangue para o átrio direito.
As artérias sistêmicas apresentam a espessura de suas paredes mais espessas que as artérias pulmonares. Além disso, as artérias que se encontram localizadas abaixo da linha do coração têm parede mais espessa que as que se encontram acima. Estas alterações refletem a maior pressão exercida pelo sangue (pressão hidrostática) suportada pelos vasos das regiões inferiores do corpo.
Circulação pulmonar
A circulação pulmonar se inicia a partir do ventrículo direito. O sangue venoso chega ao átrio direito e, em seguida, é direcionado para ventrículo no mesmo lado. Posteriormente, o sangue flui para a artéria pulmonar e para as artérias pulmonares menores, até formar os capilares pulmonares.
Nos capilares pulmonares, o CO2 é transportado em direção aos alvéolos para ser eliminado no ar ambiente, enquanto o O2 sofre difusão para o sangue, num processo denominado hematose, responsável por uma nova arterialização do sangue.
A partir deste ponto, o sangue é direcionado para as veias pulmonares com uma maior quantidade de oxigênio, retornando ao átrio esquerdo e seguindo para o ventrículo esquerdo. A partir deste ponto, o sangue arterial segue para toda a rede de distribuição de artérias novamente.
O SISTEMA CARDIOVASCULAR
Assista ao vídeo a seguir, que demonstra os aspectos anatômicos do coração (átrios, ventrículos e valvas), e como ocorre a circulação sistêmica e pulmonar.
Em resumo, podemos dizer que os diferentes segmentos do sistema cardiovascular possuem características funcionais e estruturais diversas. Estas se adequam às variações de pressão e volume de sangue conduzido a outras particularidades que são dependentes do funcionamento eficiente e harmônico do coração.
Atenção
Em função disso, torna-se necessário entender como o ritmo cardíaco é regulado para garantir o fluxo sanguíneo satisfatório aos tecidos, sem que ocorra grandes variações nas faixas de pressão e volume do sistema, a fim de garantir o controle da homeostase sistêmica.
Atividade 4
MÓDULO 2
Compreender os mecanismos responsáveis pelo controle do ritmo cardíaco
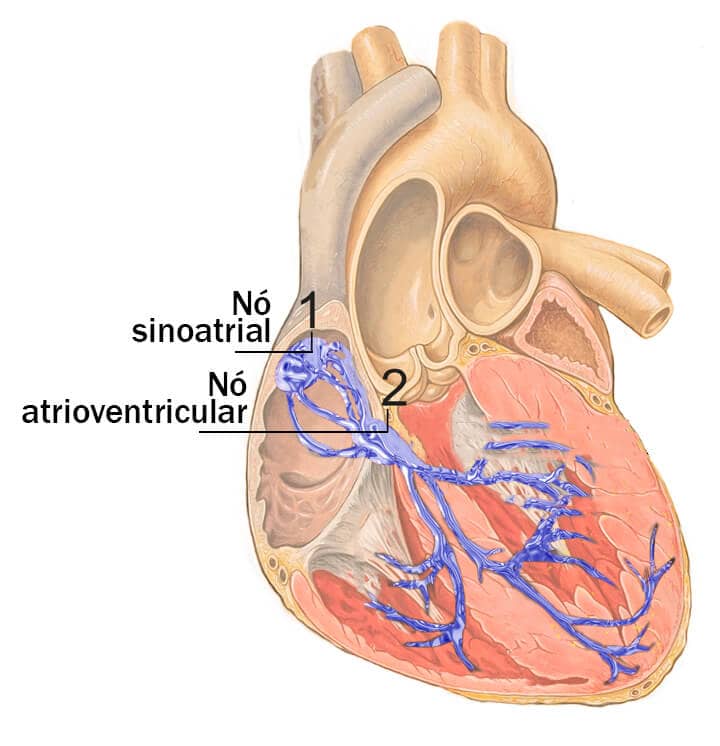
Neste sistema, as células que promovem a gênese do impulso nervoso desempenham esse mecanismo em frequências de disparo diferentes. O nó sinoatrial é a célula que possui maior frequência intrínseca de disparo espontâneo comparado ao nó atrioventricular e às fibras de Purkinje (imagem a seguir, número 1).
A propagação ocorre por este nó a uma velocidade de aproximadamente 0,06 milissegundos (ms), alcançando o átrio aproximadamente 30 ms após o início desta excitação. À medida que o impulso nervoso é originado no nó sinoatrial, ele é direcionado para as paredes atriais a uma velocidade de aproximadamente 0,9 ms, ou seja, leva cerca de 80 a 90 ms para completar sua ativação.
A trajetória do impulso então alcança outro nó, o atrioventricular (imagem a seguir, número 2).
A partir do nó atrioventricular, fibras nervosas atravessam o esqueleto fibroso do coração, localizado no anel atrioventricular, separado por um envoltório de tecido conjuntivo. Em seguida, faz conexões com a massa muscular ventricular através das junções comunicantes.
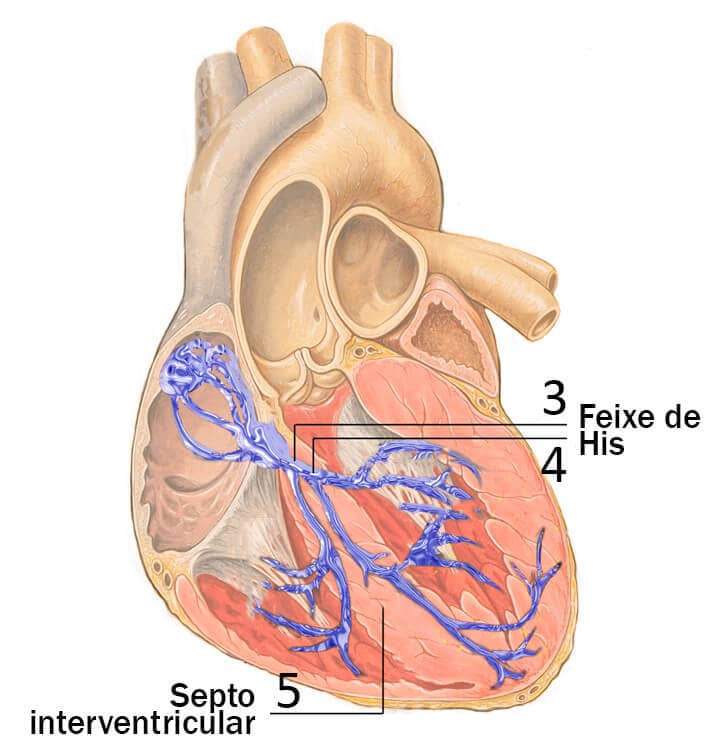
Sequencialmente, uma vez que o impulso nervoso termine seu tráfego através do nó atrioventricular, a despolarização pelo sistema de condução agora alcança o feixe de His (números 3 e 4 da imagem abaixo) e, em seguida, as fibras de Purkinje. Finalmente, toda onda de despolarização é direcionada pelas células do miocárdio ventricular, completando a ativação dessas câmaras.
Uma vez nos ventrículos, a onda de ativação percorre inicialmente as células da camada mais interna dessas câmaras (endocárdio) dos dois ventrículos e, em seguida, os impulsos são propagados em direção à camada mais externa dos ventrículos (epicárdio) até alcançar à região póstero-superior do septo interventricular (número 5).
Atividade 1
Atenção
Observa-se a existência de uma fase em que não há nenhum fluxo de corrente ao longo do coração. Neste momento os átrios encontram-se repolarizados, ao passo que os ventrículos estão totalmente despolarizados. Este período silente termina quando se inicia a repolarização ventricular a partir das regiões com potenciais de ação de menor duração. A repolarização de uma região acelera a repolarização de localidades vizinhas do mesmo modo que a despolarização, por meio do fluxo de correntes locais. Assim, pode-se dizer que há uma propagação da repolarização, a partir da região que primeiro depolariza, em direção às vizinhas.
A EXCITAÇÃO AUTOMÁTICA DO CORAÇÃO
Assista ao vídeo a seguir, que demonstra como ocorre o processo intrínseco de excitação do coração, desde o nodo sinusal até as fibras de Purkinje.
Potencial de ação cardíaco lento
Um conjunto de células cardíacas não precisam de estímulo externo (também denominado extrínseco) para iniciar um potencial de ação. Esta propriedade é conhecida como automatismo cardíaco (governada pelas células do nó sinoatrial, do nó atrioventricular e as fibras de Purkinje).
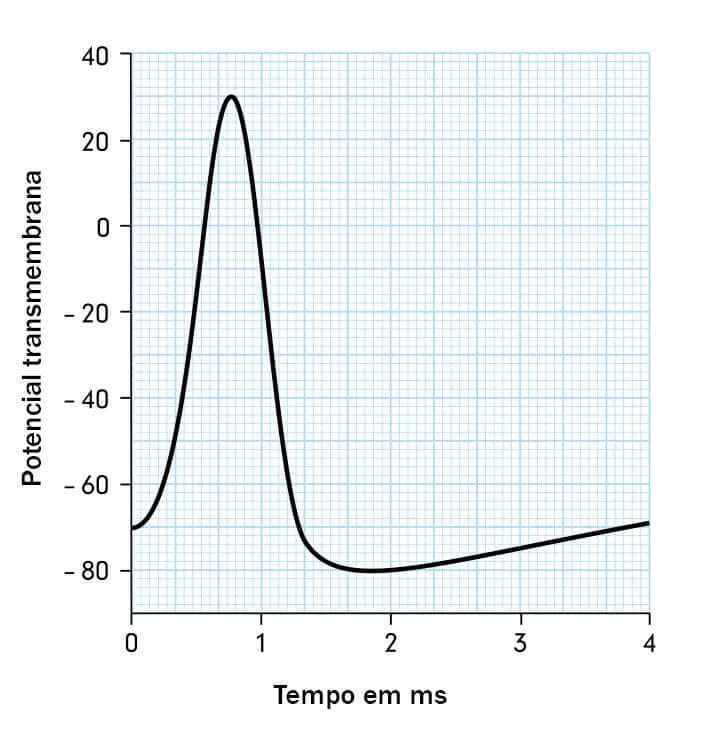
Nestes tecidos, não se observa um potencial de repouso estável (fixo) como na maioria das outras células, ao contrário, nota-se uma despolarização lenta seguida do término da fase de repolarização. Esta despolarização lenta, como ocorre na fase diastólica do potencial transmembrana, é denominada despolarização diastólica lenta, correspondente à fase 4 dos potenciais de ação responsáveis pelo automatismo cardíaco.
As correntes iônicas responsáveis pela entrada de íons nas células são denominadas correntes de influxo. As principais correntes de influxo observadas na despolarização diastólica lenta são:
Corrente marca-passo (também denominada corrente If), sendo esta mediada pelo influxo de sódio (Na+) no início da Fase 4.
Corrente transiente de cálcio, ou do tipo T (IcaT), responsável pela segunda metade da despolarização diastólica lenta até o início da Fase 0.
Ao final da Fase 4, quando o potencial transmembrana atinge o potencial limiar (por volta de -60mV), inicia-se a Fase 0. Nesta fase, observa-se uma despolarização mais rápida que aquela da Fase 4.
Atenção
Aqui, a principal corrente responsável por esta despolarização mais íngreme é a corrente de cálcio do tipo L, ICaL, que se caracteriza por uma ativação mais lenta e uma densidade de corrente bem inferior à de sódio (INa+, como será observado no potencial de ação rápido).
Na imagem, podemos observar que essas células não apresentam as Fases 1 e 2, como ocorre no potencial de ação rápido ventricular. Após a Fase 0, segue-se uma repolarização contínua, mais lenta no início e mais rápida no final (Fase 3).
Já que não há nenhuma evidência de ocorrência de IK1 nem de Ito nestas células, os canais de K+, IKr e IKs constituem as principais vias de correntes repolarizantes. Contribuem com corrente despolarizante durante todo o potencial de ação lento, a ICa,L, além da corrente carreada pelo trocador Na+/Ca2+.
Potencial de ação cardíaco rápido
Os átrios e ventrículos são constituídos por células miocárdicas através das quais a atividade elétrica se propaga. Imersas nessa massa muscular contrátil (miocárdio), existem estruturas especializadas na geração e condução da atividade elétrica, formadas por tecido muscular especializado denominado de sistema de condução.
No átrio direito, próximo da inserção da veia cava superior, situa-se o nó sinoatrial, que no coração normal é o local onde ocorre a gênese da atividade elétrica cardíaca. Por isso, o nó sinoatrial é considerado o marcapasso cardíaco. Também no átrio direito, próximo ao seio coronariano, na superfície endocárdica da porção inferior do septo interatrial, localiza-se o nó atrioventricular.
A partir deste, outro tecido especializado em condução é o feixe de His, que parte do nó atrioventricular e se estende para a musculatura ventricular, subsequentemente dividindo-se e formando uma extensa rede de condução intraventricular, as fibras de Purkinje.
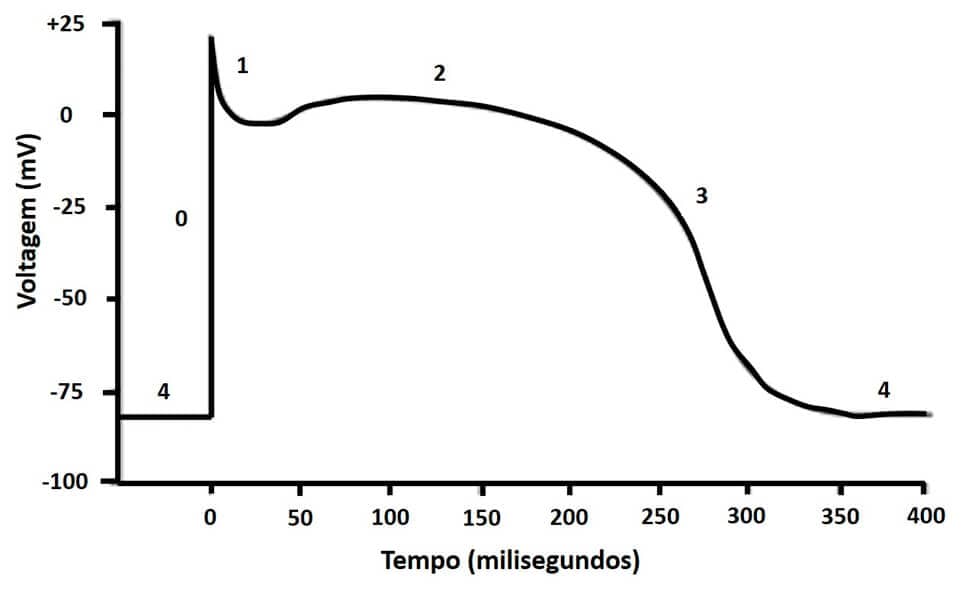
O potencial de ação rápido cardíaco pode ser dividido em fases que serão descritas a seguir:
Esta fase está relacionada ao aumento rápido que ocorre durante a despolarização do potencial de ação rápido. Neste momento a principal corrente despolarizante é a de sódio dependente de voltagem (INa). Isto irá promover a despolarização adicional, caracterizada por um processo de retroalimentação positiva e resultando em rápido e intenso influxo de Na+. Por sua enorme densidade, esta corrente é fundamental para a rápida propagação do potencial de ação (1 a 5 ms), no entanto, cabe ressaltar que as menores velocidades ocorrem no miocárdio atrial e ventricular; e as maiores, nas fibras de Purkinje, tecido especializado na condução do potencial de ação.
Nesta rápida e transitória repolarização, após a despolarização inicial, está relacionada à abertura do canal de K+ (representado pela abreviatura Ito1), que por sua vez é ativado por despolarização.
Também considerada como a fase de platô, nesta fase ocorre o equilíbrio das correntes despolarizantes (influxo de Na+ e Ca2+) e das correntes repolarizantes (efluxo de K+ e influxo de Cl–). Assim, o fluxo efetivo de carga (somatório de cargas que entram e saem da célula) durante esta fase é muito pequeno, razão pela qual o potencial transmembrana permanece relativamente estável. As correntes despolarizantes presentes nesta fase incluem a corrente de ICaL, o componente não inativável ou de inativação lenta de INa, além da corrente de influxo carreada pelo trocador Na+/Ca2+. Em relação às correntes repolarizantes, a corrente retificadora de influxo, IK1, que permanece aberto durante o repouso, fecha-se quase instantaneamente com a despolarização da Fase 0. Assim, durante o platô, ele permanece fechado, contribuindo para diminuir a corrente de efluxo, mantendo a membrana despolarizada.
A fase de repolarização rápida final ocorre em decorrência de uma predominância de correntes de efluxo, uma vez que as correntes de influxo presentes durante o platô diminuem consideravelmente. Nesta fase, a condutância ao K+ depende de canais iônicos diferentes daqueles que determinam o potencial de repouso. Ela está diretamente associada à ativação dos canais de K+ dependentes de voltagem, denominados retificadores retardados (IKr, IKs e IKur), estimulada pela despolarização da Fase 0, que promove um grande efluxo de K+, acarretando rápida repolarização. Este fenômeno permite a reabertura do canal IK1, responsável por contribuir para o processo de repolarização. Por todos estes motivos, a Fase 3 é considerada a fase determinante da duração do potencial de ação.
Quanto ao comportamento do potencial de ação, nesta fase há novamente um equilíbrio entre as correntes de efluxo e influxo, de modo que o saldo é uma corrente efetiva nula, como já vimos na Fase 2.
Atividade 2
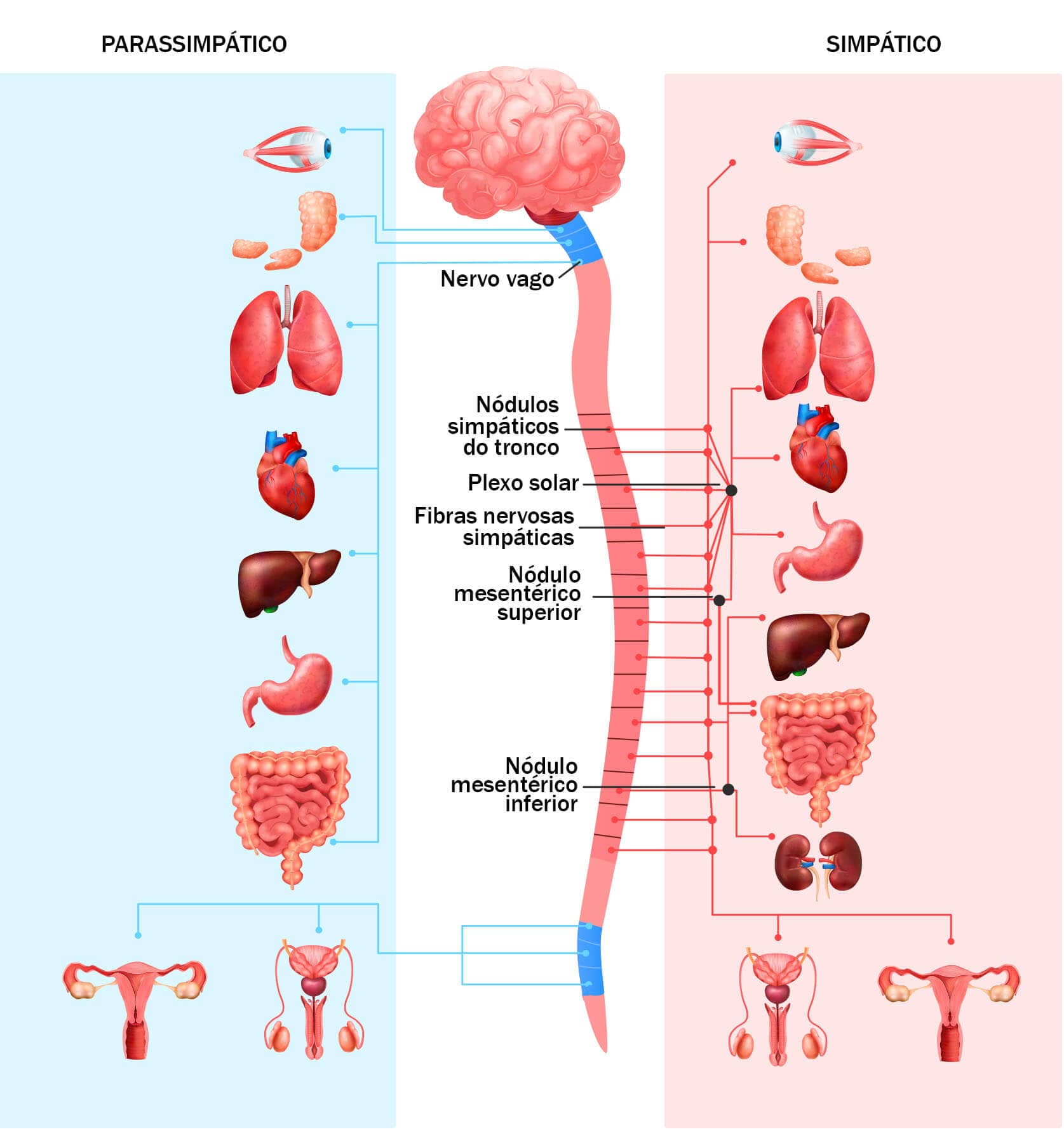
O sistema nervoso autônomo é subdividido em dois componentes, o sistema nervoso simpático e o parassimpático. Ambos apresentam características comuns que estão descritas na imagem.
Nos dois sistemas, a inervação é realizada por neurônios efetores que se situam antes da cadeia simpática, os neurônios pré-ganglionares. Estes originam as fibras pós-ganglionares que estabelecem as sinapses com os órgãos-alvo. Os neurônios pré-ganglionares são ativados previamente por conexões diretas de neurônios situados no sistema nervoso central.
Durante a ativação das fibras pós-ganglionares, os neurotransmissores são liberados no interstício até encontrarem seus receptores específicos. No caso dos terminais axônios das fibras pós-ganglionares simpáticas, o neurotransmissor principal é a noradrenalina (NA), também chamada de norepinefrina (NE), enquanto nos terminais axônicos das fibras pós-ganglionares parassimpáticas, o neurotransmissor principal é a acetilcolina.
A regulação autonômica no controle do ritmo cardíaco e dos vasos sanguíneos é de fundamental importância para a manutenção do sistema cardiovascular, como por exemplo, a regulação da pressão arterial, da resistência periférica total e da função cardíaca. Durante a estimulação simpática, ocorre o aumento da frequência cardíaca, da força de contração (contratilidade) e da pressão arterial.
Os efeitos do sistema nervoso simpático sobre a musculatura cardíaca são mediados pelos receptores adrenérgicos do subtipo β1. Já a inervação parassimpática atua diminuindo a frequência cardíaca, assim como reduz a contratilidade e a pressão arterial através da interação da acetilcolina com os receptores muscarínicos do tipo 2 (M2).
Atenção
No coração, ambos os sistemas simpático e parassimpático têm atividade tônica, isto é, as fibras pós-ganglionares desses sistemas apresentam potenciais de ação contínuos, com liberação mantida de seus respectivos neurotransmissores. Assim, podemos dizer que a frequência cardíaca de um indivíduo a cada instante é o resultado do efeito excitatório simpático e do efeito inibitório parassimpático.
Além do seu importante papel no controle do ritmo cardíaco, o sistema nervoso autônomo é bastante eficiente no monitoramento rápido da perfusão sanguínea para os tecidos. Para isto, o sistema nervoso autônomo recebe informações de sensores localizados nos vasos sanguíneos (barorreceptores) sobre a quantidade de sangue que o coração está bombeando por minuto (débito cardíaco).
Considerando o sistema cardiovascular um sistema de tubos fechados, para que o coração seja capaz de bombear certa quantidade de sangue por minuto ele precisa receber a mesma quantidade das veias, fenômeno este denominado retorno venoso. Sendo assim, o sistema nervoso autônomo promove o controle da função miocárdica, visando a manutenção do débito cardíaco e do retorno venoso para garantir níveis adequados de oxigênio e nutrientes para os tecidos.
Atividade 3
MÓDULO 3
Reconhecer os fenômenos associados à função miocárdica e seu papel na manutenção do débito cardíaco e retorno venoso
A perfusão adequada de sangue para os tecidos se dá pela força de contração que o coração é capaz de exercer (contratilidade), quer a pessoa esteja em repouso ou desenvolvendo diferentes atividades diárias. Por isso, o coração é responsável por garantir que a quantidade de sangue bombeada por minuto no compartimento arterial (débito cardíaco), bem como seu retorno de volta ao coração pelas veias (retorno venoso) sejam eficientes.
O débito cardíaco depende da frequência cardíaca e do volume sistólico, e este é determinado pela contratilidade miocárdica combinada com a magnitude do retorno venoso (pré-carga) e com a resistência periférica total.
O retorno venoso, também caracterizado como pré-carga, é dependente da magnitude do volume sanguíneo (volemia), bem como de outros fatores responsáveis pelo direcionamento do sangue de volta ao coração, entre os quais a capacitância venosa.
Atenção
Adicionalmente, levando em consideração que os fatores citados anteriormente possuem grande impacto no débito cardíaco (normalmente, quanto maior o retorno venoso, maior será o débito cardíaco) e na resistência periférica total (RPT), a pressão arterial também pode ser efetivamente influenciada, uma vez que esta representa o produto do débito cardíaco e da RPT.
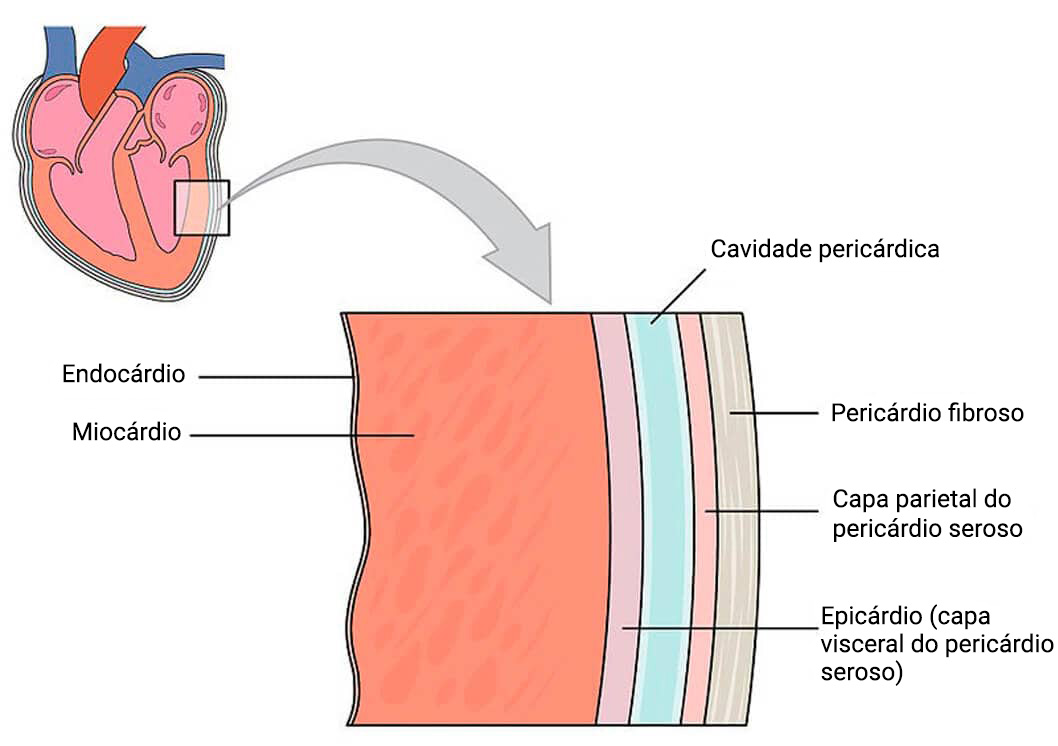
O tecido cardíaco pode ser dividido em três camadas. Na porção externa, encontra-se o pericárdio, dividido em duas camadas, uma fibrosa e outra serosa que garantem a fixação e a sustentação do coração na parede torácica; na porção média, fica a camada mais espessa, responsável pela contração do coração, o miocárdio; na porção interna está localizado o endocárdio.
O sinal para a contração do miocárdio atrial e ventricular é originado pelas células autoexcitáveis provenientes do sistema de condução do nó sinoatrial e do atrioventricular, porém pode ser modulado pelo sistema nervoso autônomo. Visualizando as características estruturais, o músculo cardíaco é estriado, mas difere bastante do músculo estriado esquelético não somente em relação à estrutura, como também em sua função.
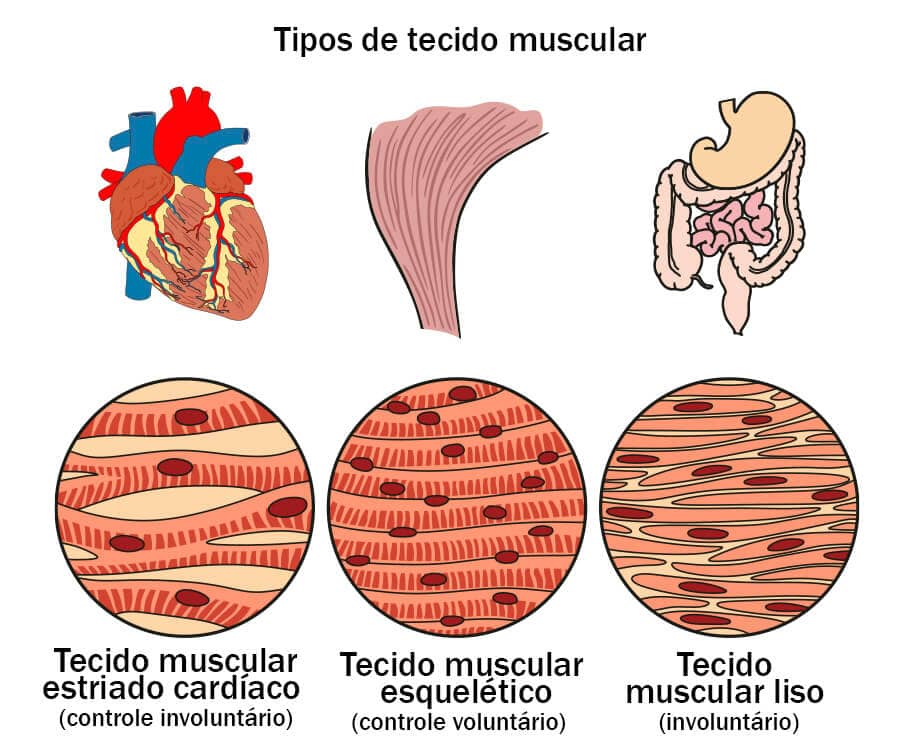
Listamos as principais diferenças observadas entre os músculos estriados cardíaco e esquelético:
1 - As fibras do músculo estriado cardíaco são menores que as do músculo estriado esquelético;
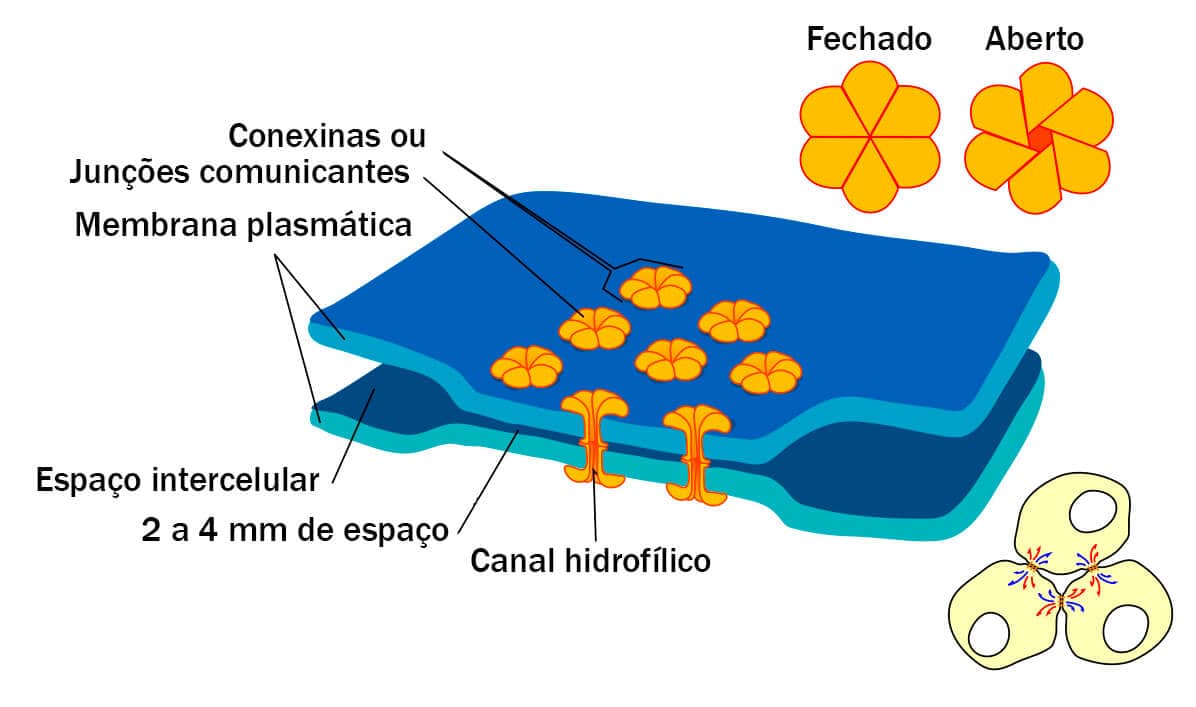
2 - As células do músculo cardíaco se ramificam com as células vizinhas, e essa conexão é mantida graças à presença de diversos discos intercalares, denominados também junções comunicantes;
3 - Essas junções permitem que ocorra o transporte de íons de célula para célula. Por isso, quando uma célula é estimulada, todas as outras são estimuladas quase que simultaneamente (motivo pelo qual o coração é considerado um sincício funcional);
4 - O retículo sarcoplasmático do miócito cardíaco é menos desenvolvido se comparado ao músculo esquelético, fazendo com que o músculo cardíaco dependa do Ca2+ extracelular durante o fenômeno da contração muscular;
5 - O músculo cardíaco consome cerca de 75% do oxigênio que chega a ele, isto se deve ao fato do alto número de mitocôndrias no citoplasma (ocupam cerca de 40% do volume celular).
Quando ocorre o aumento da necessidade de oxigênio pelo miocárdio (como durante o exercício físico), o coração consome quase todo o oxigênio que chega pelas artérias coronárias. Por este motivo, o aumento do fluxo sanguíneo pelo miocárdio é o principal mecanismo que garante mais oxigênio para o músculo cardíaco nessas condições.
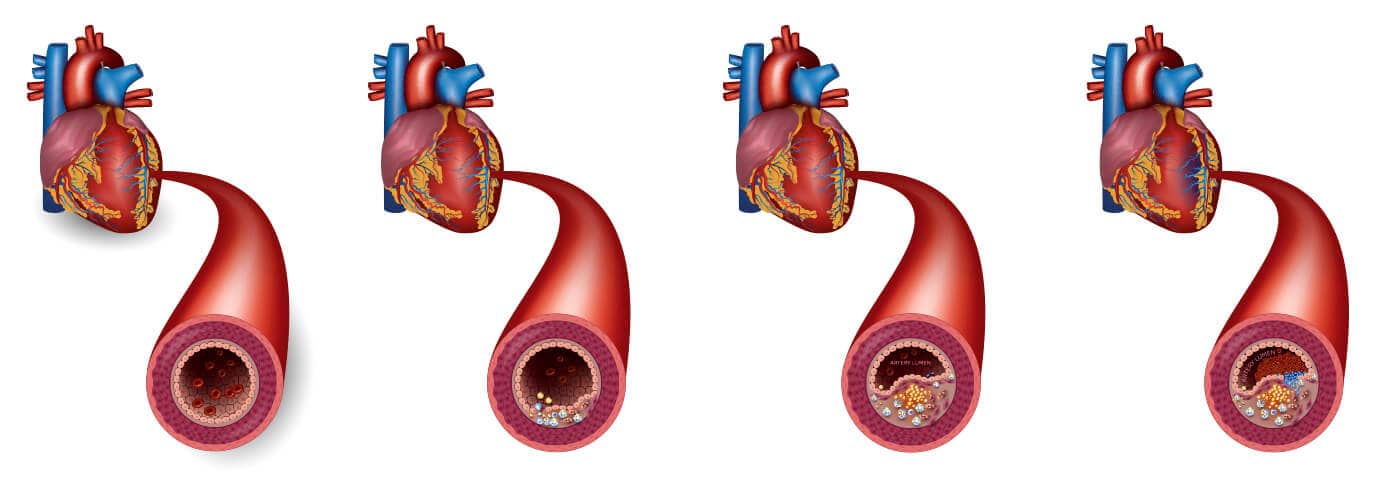
Quando o fluxo sanguíneo miocárdico reduz devido ao estreitamento de um vaso coronário ou de algum de seus ramos (imagem), como ocorre na doença arterial coronariana, as células miocárdicas podem ser comprometidas ou até mesmo lesionadas, caracterizando o infarto do miocárdio.
Atividade 1
No músculo cardíaco, o potencial de ação inicia o acoplamento excitação-contração, e este potencial é originado pelas células autoexcitáveis (com atividade marca-passo) do coração e se propaga para as células vizinhas através das junções comunicantes.
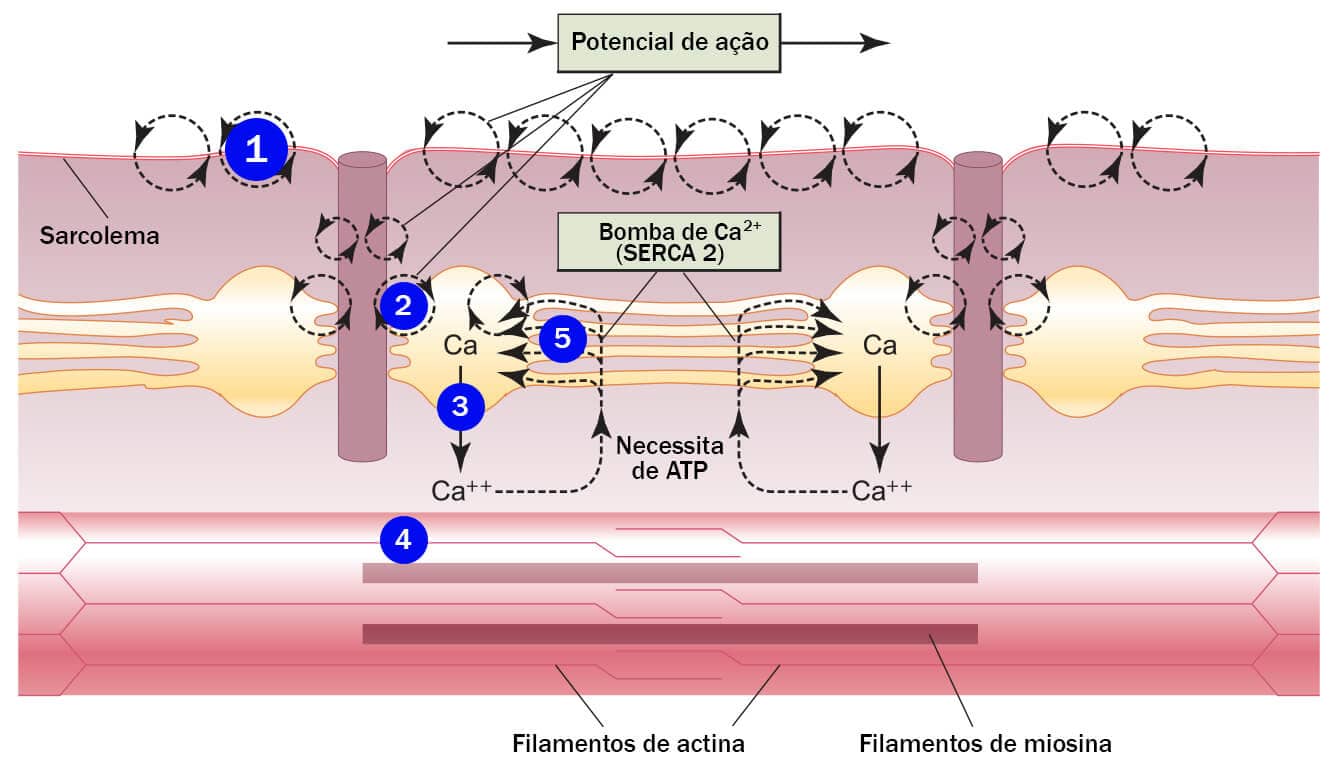
Veja, a seguir, as etapas do acoplamento excitação-contração do miocárdio.
Com o início do potencial de ação (número 1) e seu tráfego pela membrana do músculo estriado cardíaco, ocorre a abertura dos canais de Ca2+ dependentes de voltagem tipo L (IcaL) na membrana celular (número 2). O Ca2+ entra nas células através desses canais, movendo-se a favor do seu gradiente de concentração (a concentração de Ca2+ no meio extracelular é maior que no meio intracelular).
À medida que ocorre a entrada de Ca2+ para o interior da célula, ele promove a abertura dos canais liberadores de Ca2+ do tipo rianodínico 2 (RyR2), localizados no retículo sarcoplasmático (número 3).
O processo do acoplamento excitação-contração no músculo cardíaco é também chamado de liberação de Ca2+-induzida pela entrada de Ca2+ através da membrana. Quando os canais RyR2 se abrem, o Ca2+ estocado é liberado para o citoplasma da célula, neste momento o Ca2+ irá desempenhar o papel no acoplamento excitação-contração, promovendo a contração do miocárdio.
A liberação de Ca2+ do retículo sarcoplasmático fornece cerca de 90% do Ca2+ que é necessário para contração muscular, e os outros 10% entram na célula a partir do líquido extracelular. O Ca2+ difunde-se pelo citosol para as proteínas contráteis, onde se liga à troponina C e inicia a interação e o movimento das pontes cruzadas (número 4).
Durante o relaxamento do miocárdio, a maior parte do Ca2+ liberado durante a contração precisa ser removido do citoplasma para que a interação entre as pontes cruzadas seja desfeita. A maior parte do Ca2+ é transportada de volta para o retículo sarcoplasmático (cerca de 70%) com o auxílio de uma bomba, a Ca2+-ATPase do tipo 2 (SERCA2) (número 5). A outra parcela de Ca2+ que foi liberada durante a contração é removida para fora da célula pelo trocador Na+/Ca2+ (NCX) ou é transportada para o interior das mitocôndrias.
Atividade 2
CICLO CARDÍACO
Ciclo cardíaco
Neste vídeo, você vai acompanhar detalhadamente como ocorre o ciclo cardíaco, com a fase de relaxamento e enchimento cardíaco (diástole) e a fase de contração e esvaziamento cardíaco (sístole).
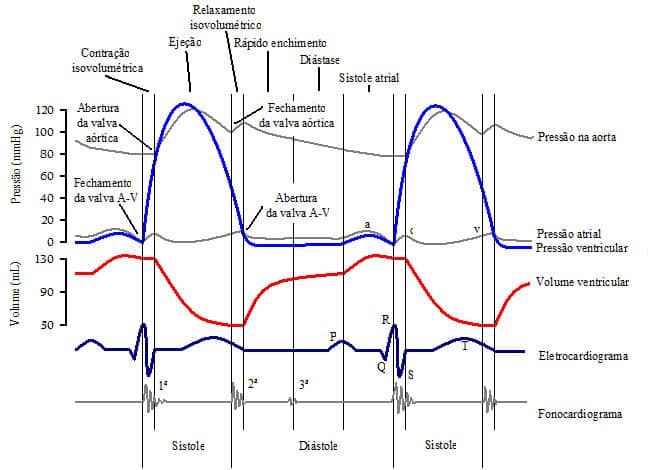
A cada sequência de estímulos no coração inicia-se um novo ciclo cardíaco, que pode ser compreendido como o período em que ocorre o início de um batimento até o início do próximo. Embora os períodos em que o ciclo cardíaco ocorre sejam divididos em sístole (contração) e diástole (relaxamento), notamos que esses períodos podem ser divididos e analisados nas sete fases que listamos a seguir.
Cabe ressaltar que esta análise é realizada nas câmaras esquerdas do coração.
O ciclo cardíaco inicia-se com a excitação atrial, com o surgimento da onda P no registro eletrocardiográfico (ECG). A elevação da pressão atrial durante a contração origina a onda a. Embora os átrios estejam se contraindo neste momento, o enchimento ventricular ocorre antes desta fase, basta notar a curva de volume ventricular (vermelha) que sofre pequena elevação com a contração atrial.
Outra observação importante é a diminuição progressiva da pressão aórtica durante a diástole ventricular, isto porque o sangue flui dos grandes vasos arteriais em direção aos tecidos.
Mas por que os átrios contribuem pouco para o enchimento ventricular?
A explicação está relacionada com o fato de que a maior parte do enchimento ocorre, de modo passivo, simplesmente pela abertura das valvas atrioventriculares. No entanto, quando a frequência cardíaca está elevada, o período da fase diastólica reduz bastante. Nestas condições, a contração atrial passa a exercer um papel importante para o enchimento ventricular. Agora, observe a curva de volume ventricular (curva vermelha). Note que nesta fase o volume ventricular atinge seu máximo valor ao final do período diastólico, por isso é chamado de volume diastólico final.
Após a contração atrial, quando a despolarização alcança as células do ventrículo esquerdo, note que o complexo QRS é iniciado no ECG, seguido da sístole ventricular. Neste momento, observamos um rápido aumento da pressão ventricular. Ao mesmo tempo ocorre o fechamento da valva mitral, acarretando a primeira bulha cardíaca (primeiro ruído no fonocardiograma).
A elevação da pressão atrial, representada pela onda c, ocorre em função da interrupção do fluxo sanguíneo do átrio para o ventrículo esquerdo. Observe que neste momento, a valva mitral e a aórtica encontram-se fechadas. Sendo assim, a sístole ventricular ocorrerá sem redução do volume no ventrículo esquerdo (esta fase da sístole é denominada contração isovolumétrica ventricular).
O aumento progressivo da tensão na parede ventricular, em decorrência da fase sistólica, produz rápido aumento da pressão no interior do ventrículo esquerdo. No momento em que essa pressão fica mais elevada que a da aorta (pressão arterial diastólica de 80 mmHg em função da fase diastólica), a valva semilunar aórtica se abre, iniciando a fase de ejeção ventricular para a aorta.
Com a abertura da valva semilunar aórtica, a fase de ejeção ventricular é iniciada. Esta fase pode ser dividida em um período inicial rápido (com duração de 0,11 s aproximadamente) seguido de outro mais lento (cerca de 0,13 s). Esta fase é dividida em ejeção ventricular rápida e lenta.
Inicialmente, observamos que ocorre o aumento da pressão ventricular (curva azul) e o declínio da curva de volume ventricular (curva vermelha). Como a entrada de sangue na aorta ocorre mais rapidamente do que a passagem deste para as artérias menores, a pressão aórtica, que antes estava em reduzida (80 mmHg), agora aumenta até atingir um valor máximo (cerca de 120 mmHg), próximo da metade do tempo de ejeção ventricular. Isto ocorre durante a sístole ventricular, por isso a pressão máxima é referida como pressão arterial sistólica.
A partir deste momento, o miocárdio ventricular inicia a fase de repolarização, conforme se constata pelo início da onda T no ECG.
Ao final da sístole, a pressão ventricular encontra-se menor que a pressão aórtica, mas a ejeção continua, com fluxo menor que na fase inicial. A ejeção é mantida pela alta aceleração do sangue pela contração ventricular na fase anterior. A partir daí, ocorre uma queda rápida da pressão ventricular esquerda. Isto resulta no fechamento da valva aórtica, terminando o período de sístole e a ejeção ventricular. No momento em que ocorre o fechamento da valva aórtica, note o surgimento da segunda bulha cardíaca no fonocardiograma.
Você irá perceber que, mesmo ao final da sístole ventricular, nem todo volume contido no ventrículo esquerdo é lançado para a aorta, restando um certo volume de sangue no ventrículo ao final da sístole. Este volume é chamado de volume sistólico final.
Durante a sístole em indivíduos normais em repouso, um volume de aproximadamente 80 ml de sangue é ejetado (volume de ejeção ou volume sistólico) e 35ml permanecem no ventrículo esquerdo. Dividindo os valores do volume sistólico pelo volume diastólico final, encontramos um valor equivalente a 0,7 ou 70%, denominado como fração de ejeção.
Ao término da fase de contração ventricular, ocorre um aumento na onda de pressão atrial (curva cinza), denominada v, que representa o acúmulo de sangue nos átrios quando as valvas atrioventriculares estavam fechadas ao longo de todo o período de contração ventricular.
Fração de ejeção = volume sistólico ÷ volume diastólico final
Nota Clínica: A fração de ejeção é uma variável importante para o diagnóstico clínico da insuficiência cardíaca, uma vez que pacientes com insuficiência cardíaca congestiva apresenta valores inferiores a 40%.
De modo similar ao que ocorre na contração isovolumétrica, nesta fase as valvas atrioventricular e semilunar encontram-se fechadas. Então, por mais que a pressão intraventricular esteja sofrendo grande redução, não há variação de volume. A isso denominamos relaxamento ventricular isovolumétrico, marcando o início da diástole.
O valor da pressão ventricular diminui rapidamente devido ao relaxamento e consequente queda de tensão ativa na parede ventricular. A pressão aórtica varia pouco por causa da elasticidade de suas paredes, mas depois decresce durante toda a diástole. A pressão atrial se eleva, pelo retorno venoso e pelo fato de a valva mitral estar fechada, até o momento em que esta supera a pressão intraventricular.
Quando a pressão ventricular (esquerda) fica mais elevada que a pressão intraventricular, a válvula mitral se abre (a válvula aórtica continua fechada) e termina a fase de relaxamento ventricular isovolumétrica.
Nesta fase, ocorre a segunda bulha cardíaca, cujo som é provocado, em grande parte, pelo contato do sangue nas valvas semilunares (aórtica), já que o sangue tenta voltar para o ventrículo esquerdo pela grande redução de pressão nesta câmara.
Com a abertura da valva atrioventricular esquerda (bicúspide), o sangue é transportado do átrio esquerdo em direção ao ventrículo esquerdo e, à medida que a pressão atrial se estabiliza, ocorre a contração atrial. Por este motivo os átrios contribuem com apenas cerca de 25% do volume ventricular.
O enchimento ventricular ocorre de maneira bem rápida no início, porque o gradiente de pressão é mais elevado nesta fase inicial, favorecendo a passagem do sangue da cavidade atrial para a ventricular. O enchimento rápido recebe grande influência da perda de tensão na parede ventricular no início da diástole, que depende tanto da eficiência do processo de relaxamento muscular como da complacência da câmara.
Assim, esse componente passivo de enchimento ocorre em menor proporção nas câmaras mais rígidas ou menos complacentes, caracterizando a disfunção diastólica.
À medida que o gradiente pressórico através da valva atrioventricular diminui, na fase média da diástole, a velocidade de enchimento se reduz. Simultaneamente, a pressão aórtica continua caindo lentamente até atingir um valor mínimo no final da diástole (pressão arterial diastólica).
O CICLO CARDÍACO
Assista ao vídeo que demonstra as fases do ciclo cardíaco desde a contração atrial até o enchimento ventricular lento.
Atividade 3
O débito cardíaco é um parâmetro importante da função ventricular, uma vez que representa a quantidade de sangue que é ofertado para os tecidos. Pode ser representado como a quantidade de sangue lançada pelo ventrículo esquerdo durante o período de um minuto.
Pensando nisso, basta pegar os valores referentes ao volume sistólico (quantidade de sangue ejetada pelo ventrículo em cada contração, que em uma pessoa em repouso é aproximadamente de 70 a 80 ml de sangue) e multiplicar pela frequência cardíaca, que representa o número de batimentos cardíacos durante um minuto. Desta forma, o débito cardíaco pode ser calculado pela seguinte equação:
débito cardíaco = volume sistólico × frequência cardíaca.
Na prática, imagine que em repouso sua frequência cardíaca esteja com um ritmo de 70 batimentos por minuto e seu volume sistólico seja equivalente a 70 ml, assim, seu débito cardíaco será de 4.900 ml/min ou, aproximadamente, 5 l/min. Por isso assume-se que o débito cardíaco em repouso de uma pessoa saudável seja equivalente a 5 l/min.
Lembrando o que foi dito na Nota Clínica anterior sobre a fração de ejeção em pacientes com insuficiência cardíaca congestiva, por que esse diagnóstico padronizado quando a pessoa possui o valor inferior a 40%?
Diversos estudos demonstraram que abaixo de 40% de fração de ejeção o débito cardíaco em repouso não consegue manter o valor mínimo de 5 l/min, levando a limitações orgânicas sérias. Nestas condições, pode-se dizer que a pessoa possui insuficiência cardíaca descompensada.
Determinantes do débito cardíaco
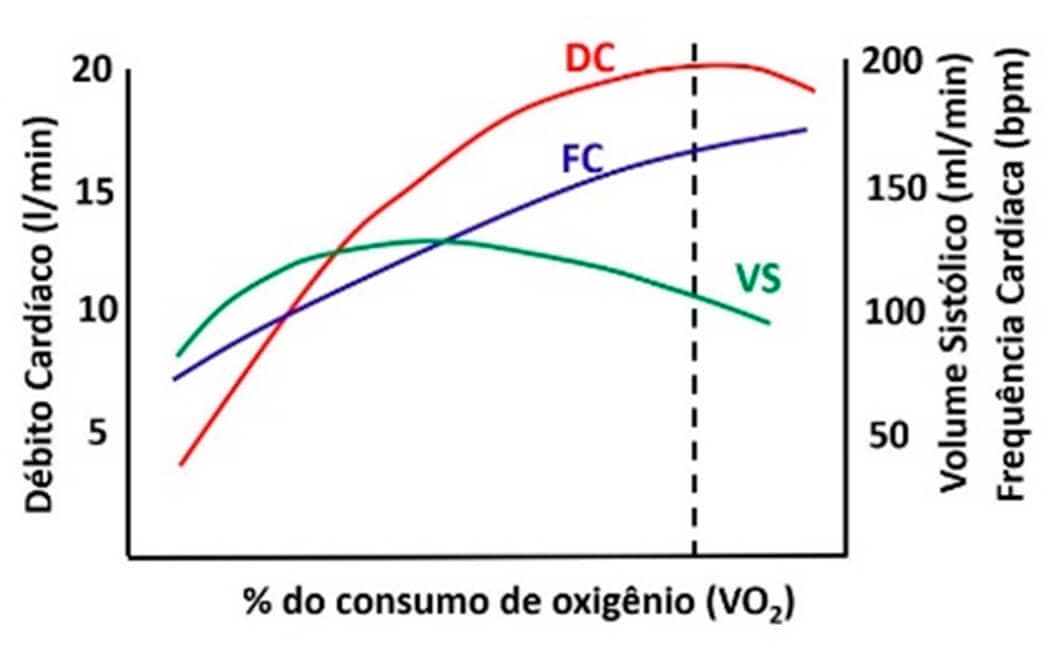
Considerando que o débito cardíaco representa o produto da frequência cardíaca pelo volume sistólico, qualquer fator que exerça influência nessas variáveis irá alterá-lo.
Mas não é tão simples assim, porque nem sempre aumentos da frequência cardíaca ou do volume sistólico irão promover aumentos no débito cardíaco. Isto porque o volume sistólico não consegue se manter estável quando ocorre um grande aumento da frequência cardíaca.
Exemplo
Durante uma taquicardia (batimentos acima de 100 bpm em repouso), o intervalo entre os dois batimentos cardíacos diminui, provocando uma redução no tempo de diástole. Assim, você pode chegar à conclusão de que o tempo de enchimento ventricular diminui e o volume diastólico final também ser reduz. Por este motivo, a redução do volume diastólico final e do volume sistólico promoverá redução ou estabilização do débito cardíaco.
Regulação do volume sistólico
O volume sistólico possui um papel importante no controle do débito cardíaco e pode sofrer influência de três fatores:
A pré-carga está relacionada ao aumento do retorno venoso que, por sua vez, pode ocorrer em função de três fatores: bomba muscular (a contração muscular comprime as veias facilitando o retorno de sangue), bomba respiratória (os movimentos respiratórios aumentam a pressão intra-abdominal, direcionando o sangue da região abdominal para região torácica) e venoconstrição (representada pela constrição das veias que direcionam o sangue mais rapidamente para o coração).
O aumento da contratilidade (força de contração) promove um aumento da pressão intraventricular, e esse mecanismo é responsável pela saída de maior quantidade de sangue do ventrículo, aumentando o débito cardíaco. O aumento da contratilidade pode ocorrer em decorrência das adaptações cardíacas promovidas pelos exercícios físicos ou quando o coração é estimulado pelo sistema nervoso simpático.
A pós-carga refere-se à força externa que promove resistência à saída de sangue pelo ventrículo. Sendo assim, quando ocorre o aumento da pós-carga (por exemplo, aumento na pressão arterial), por mais que a contratilidade aumente, como a força externa é muito elevada, o débito cardíaco irá reduzir.
Nota Clínica: O aumento da pós-carga é um dos fenômenos provocados pela hipertensão arterial sistêmica. Por este motivo, esta doença pode acarretar o aumento do risco de infarto do miocárdio e do acidente vascular encefálico, já que o débito cardíaco se torna reduzido.
Nesses três exemplos, ocorre o aumento do volume diastólico final, ou aumento da pré-carga. Tal fenômeno aumenta a força elástica do coração, promovendo assim o aumento da força contrátil e do débito cardíaco.
Atividade 4
MÓDULO 4
Comparar as respostas hemodinâmicas relacionadas à redistribuição do fluxo sanguíneo e à manutenção da pressão arterial
A redistribuição de sangue para diferentes compartimentos corporais é importante não somente para a oferta aos tecidos, mas também para a regulação da temperatura corporal denominada como termorregulação.
A termorregulação é um dos principais exemplos citados nos mecanismos de controle da homeostase. Veremos que o sistema cardiovascular é um dos mais eficientes na manutenção da temperatura corporal pelo simples fato de atuar na redistribuição do fluxo sanguíneo para diferentes compartimentos do corpo.
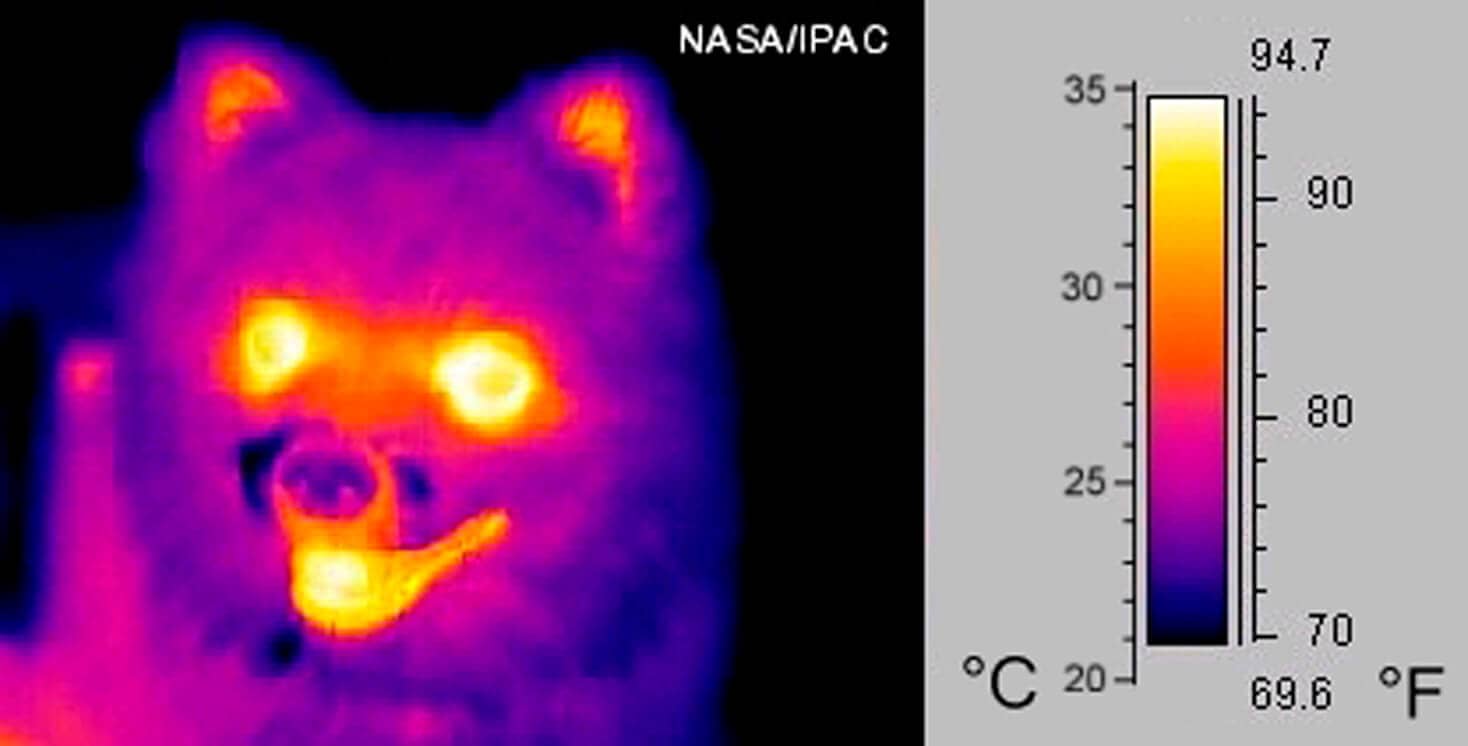
Quando mensuramos nossa temperatura (próximo de 37°C) com um termômetro, temos uma estimativa da temperatura interna, pois a temperatura externa normalmente é inferior.
Redistribuição do fluxo sanguíneo na manutenção da temperatura corporal
Os mecanismos responsáveis pela perda de calor pelo corpo podem ser classificados em quatro processos: irradiação, condução, convecção e evaporação. Os três primeiros mecanismos de perda de calor necessitam de um gradiente de temperatura entre a pele e o meio ambiente:
Na irradiação, a perda de calor ocorre através da transferência de raios infravermelhos do corpo em direção ao ambiente. Em repouso, esse mecanismo representa cerca de 60% da perda de calor corporal.
A condução está relacionada com a transferência de calor do corpo para as moléculas presentes nos objetos que entram em contato direto com a superfície corporal. Geralmente, o corpo perde somente pequenas quantidades de calor em decorrência desse processo. Um exemplo para esse mecanismo é a transferência de calor do corpo para uma cadeira de metal. Quando uma pessoa permanece sentada, o fenômeno ocorre enquanto a cadeira estiver mais fria do que a superfície corporal que está em contato.
A convecção é uma forma de transferência de calor pelo contato das partículas de ar e da água com a superfície corporal. Quando isto ocorre, o calor da superfície corporal se dissipa para o meio ambiente. De modo prático, a utilização de um ventilador desloca grandes quantidades de ar na superfície corporal, acarretando a perda de calor. Deste modo, a eficiência desse mecanismo depende da velocidade do fluxo de ar em contato com a superfície corporal. De maneira semelhante, a exposição da pessoa em água fria e em movimento resulta em uma grande perda de calor, também por convecção. Cabe lembrar que a água possui uma força convectiva cerca de 25 vezes maior do que a apresentada pelo ar a uma mesma temperatura.
Durante os períodos de calor ou quando estamos realizando exercícios físicos, a evaporação é o principal mecanismo de regulação da temperatura, e é neste mecanismo que o sistema cardiovascular atua. Na evaporação, o calor é transferido do corpo para a água na superfície da pele em forma de suor. Na medida em que a água acumula calor, ela sofre o processo de evaporação e é dissipada para o ambiente. Deste modo, durante o exercício ou em dias quentes, a temperatura corporal aumenta assim como o fluxo sanguíneo cutâneo. Simultaneamente, as glândulas sudoríparas secretam suor sobre a superfície da pele. Conforme as partículas de água evaporam, o calor é transferido para o meio ambiente, o que contribui para a manutenção da temperatura corporal.
A organização do mecanismo de perda de calor envolvendo o sistema cardiovascular
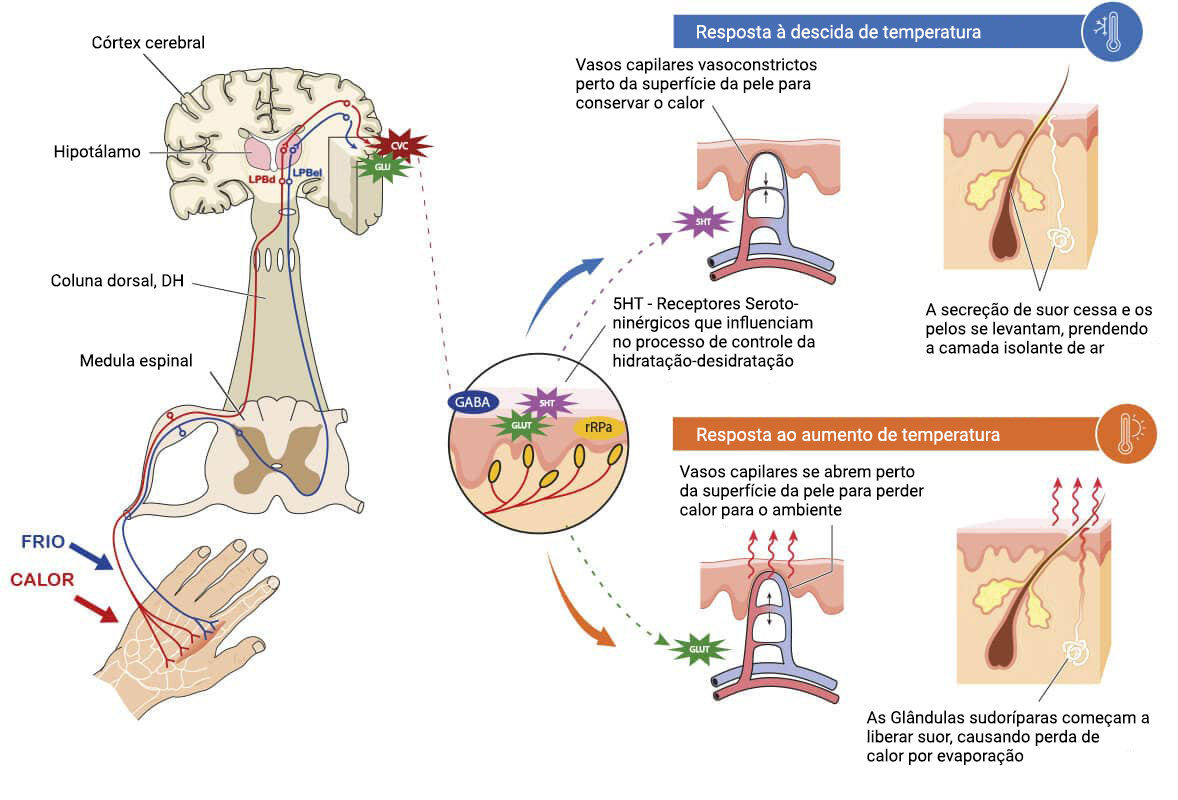
Inicialmente, os estímulos referentes às variações de temperatura no meio ambiente são captados por receptores sensoriais (termorreceptores) localizados na região cutânea (imagem abaixo).
Em seguida, os estímulos são enviados primeiro para a medula espinal (coluna dorsal, DH) e, em seguida, para o núcleo parabraquial (LPB). Observe que os estímulos referentes ao frio são direcionados para a região externa lateral (LPBel, em azul) e os relacionados ao calor, para a região direita deste núcleo (LPBd, em vermelho).
Na sequência, esses estímulos são direcionados para a área pré-óptica mediana (MnPO). Nesta região, neurônios excitatórios (glutamatérgicos, GLU em verde) ou inibitórios (GABAérgicos, GABA em vermelho) são projetados para a área pré-óptica medial (MPO).
Neste local, encontram-se os centros de integração mais importantes para a regulação da temperatura, pois regulam a atividade de tecidos que são importantes na promoção da termogênese (produção de calor), entre eles: o centro cardiovascular, o tecido adiposo marrom e o músculo esquelético.
Músculo esquelético
O músculo esquelético, especialmente, é recrutado durante o frio e desencadeia o fenômeno dos tremores.
Atenção
Este último, especialmente, é recrutado durante o frio e desencadeia o fenômeno dos tremores.
Como nosso foco está voltado para o centro cardiovascular, veremos o que irá acontecer a partir daqui. Nesta área, existem núcleos que são excitados com estímulos provenientes do calor e do frio:
CALOR
Durante o calor (CVC, em vinho), os núcleos são estimulados – mas perceba que esses núcleos liberam o neurotransmissor inibitório GABA para os núcleos da rafe (rRPa). Neste sentido, os neurônios inibitórios projetados para os núcleos da rRPa irão inibir neurônios estimulantes, responsáveis pela liberação de glutamato (GLUT). Os neurônios glutamatérgicos dessa região (rRPa) se projetam para a cadeia simpática ou intermediolateral, responsáveis pela regulação da atividade simpática e controle da resposta cardiovascular ao calor.
À medida que os neurônios excitatórios (GLUT) da rafe são inibidos, os neurônios pós-ganglionares simpáticos irão diminuir a resposta simpática para os vasos na região cutânea, acarretando a vasodilatação nesta região que ajudará no mecanismo de evaporação e evitará que ocorra o aumento da temperatura central (hipertermia).
FRIO
Durante o frio, neurônios inibitórios irão se projetar até o centro cardiovascular e, em seguida, deixarão de inibir os neurônios excitatórios localizados nos núcleos da rRPA. Assim, os estímulos excitatórios provenientes da rRPA irão aumentar a atividade dos neurônios pós-ganglionares simpáticos e, como consequência, promoverão vasoconstrição na região cutânea.
Por este motivo, durante o frio, o fluxo sanguíneo na região cutânea reduz e a pessoa se apresenta pálida. Isso ocorre para redirecionar o sangue para a região central e conservar o calor do corpo, evitando assim a hipotermia.
Veja o resumo do mecanismo da perda de calor na imagem a seguir:
Outros fatores podem interferir no mecanismo de termorregulação. Entre eles, a umidade relativa do ar e a velocidade do vento. Este último contribui com a perda de calor relacionada à convecção do ar. A umidade relativa do ar pode ser representada como o percentual de vapor de água contido no ar.
Exemplo
A umidade relativa do ar de 40% indica que o ambiente contém apenas 40% da umidade que é capaz de sustentar. Ou ainda, quando a umidade relativa do ar se encontra a 80%, significa que apenas mais 20% de umidade podem ser absorvidos pelo ar que nos rodeia. A umidade relativa do ar de 40% com temperatura de 22°C indica risco baixo no índice de estresse causado pelo calor (baixa sensibilidade térmica), enquanto a umidade relativa de 80% numa condição térmica de 33°C apresenta alto risco de estresse térmico (alta sensibilidade térmica).
Na primeira condição, não haverá dificuldade em promover a regulação da temperatura corporal. No entanto, no segundo caso, a pessoa terá mais dificuldade em realizar a evaporação, uma vez que já existe uma grande quantidade de vapor no ambiente, dificultando a transferência de calor.
Atividade 1
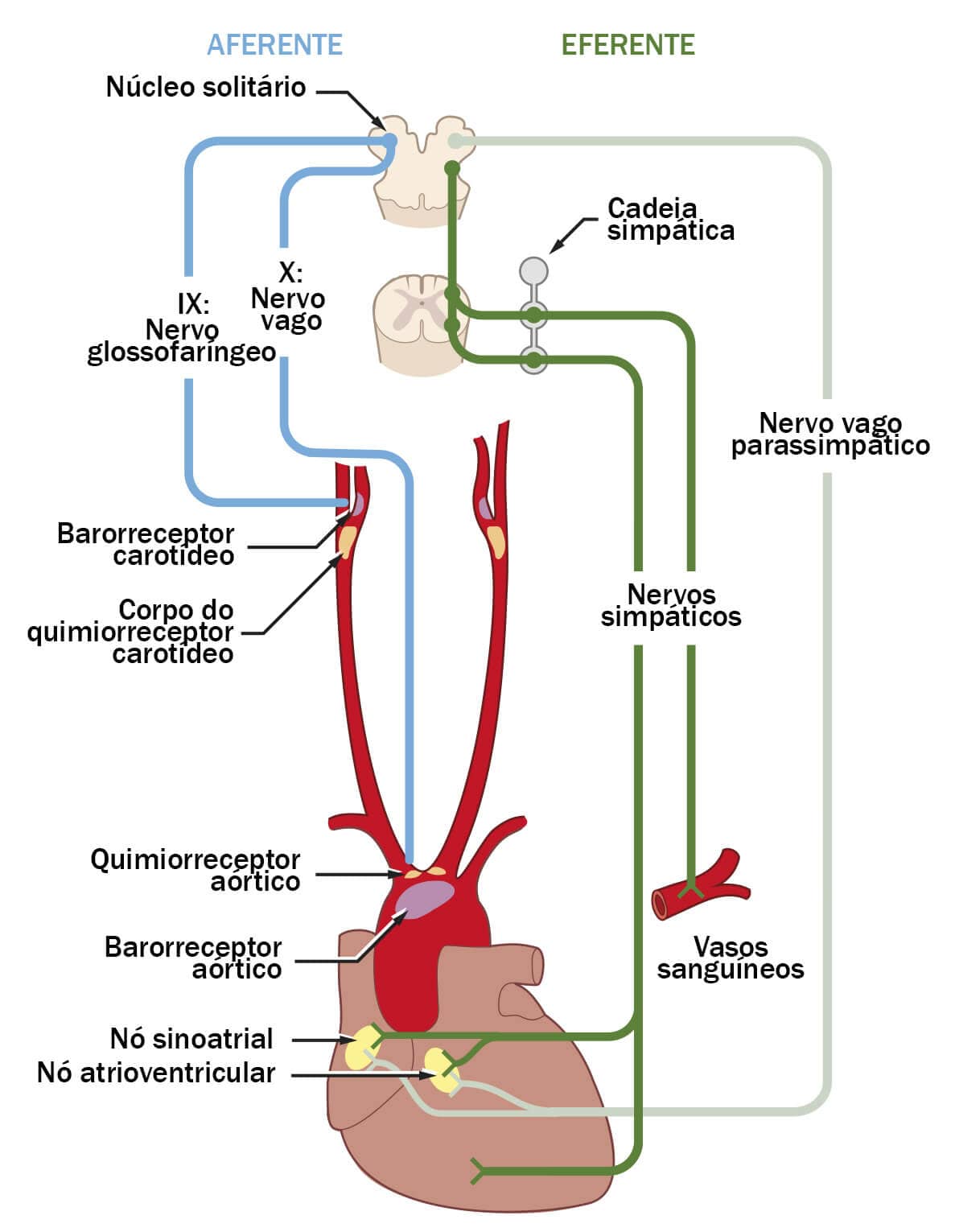
A regulação da pressão arterial a curto prazo é mediada pelo mecanismo envolvendo os barorreceptores arteriais, também chamado de mecanismo barorreflexo. Os barorreceptores são considerados mecanorreceptores localizados no arco aórtico e na bifurcação das artérias carótidas comuns (imagem a seguir).
Quando ocorre o aumento do débito cardíaco e da pressão arterial, essas artérias são excessivamente dilatadas ocasionando deformações. Quanto maior for a deformação do arco aórtico e das artérias carótidas, maior será a frequência de disparo através desses mecanorreceptores.
Vejamos como ocorre o aumento da pressão arterial:
- Quando ocorre a elevação da pressão arterial, os barorreceptores são ativados e enviam impulsos nervosos para o tronco cerebral, especificamente para o núcleo do trato solitário, informando sobre a elevação da pressão arterial (deformação das artérias).
- Assim, este promove a excitação dos neurônios pré-ganglionares parassimpáticos, localizados na região do núcleo dorsal motor do nervo vago e núcleo ambíguo. Com isso, ocorre o aumento do tônus vagal, através da excitação dos neurônios depressores do bulbo ventrolateral caudal e da inibição da atividade dos neurônios da região bulbar ventrolateral rostral (redução do tônus simpático).
- A resposta efetora desencadeada por estes centros nervosos promove a redução da frequência cardíaca, do volume sistólico, da resistência periférica e do retorno venoso. Como consequência, o débito cardíaco reduzirá promovendo a redução da pressão arterial.
Vejamos agora como ocorre a redução da pressão arterial:
- Inversamente, durante uma redução da pressão arterial acentuada, observamos respostas de taquicardia e vasoconstrição reflexas que prontamente a trazem de volta a seus valores basais. Neste caso, os barorreceptores aórticos e carotídeos são menos ou não são deformados, e a atividade aferente dos nervos depressores aórtico e sinusal é reduzida ou mesmo suprimida.
- Os neurônios do núcleo do trato solitário deixam de excitar os neurônios pré-ganglionares parassimpáticos localizados no núcleo dorsal motor do nervo vago e núcleo ambíguo (redução do tônus vagal).
- Não excitando os neurônios depressores do bulbo ventrolateral caudal, ocorre a liberação da atividade dos neurônios do bulbo ventrolateral rostral (aumento simultâneo do tônus simpático), criando as condições necessárias para que a frequência cardíaca e o volume sistólico se elevem e haja elevação da resistência periférica por vasoconstrição e do retorno venoso por venoconstrição. Deste modo, ocorre um aumento do débito cardíaco, o qual traz a pressão arterial para seus valores basais.
Atividade 2
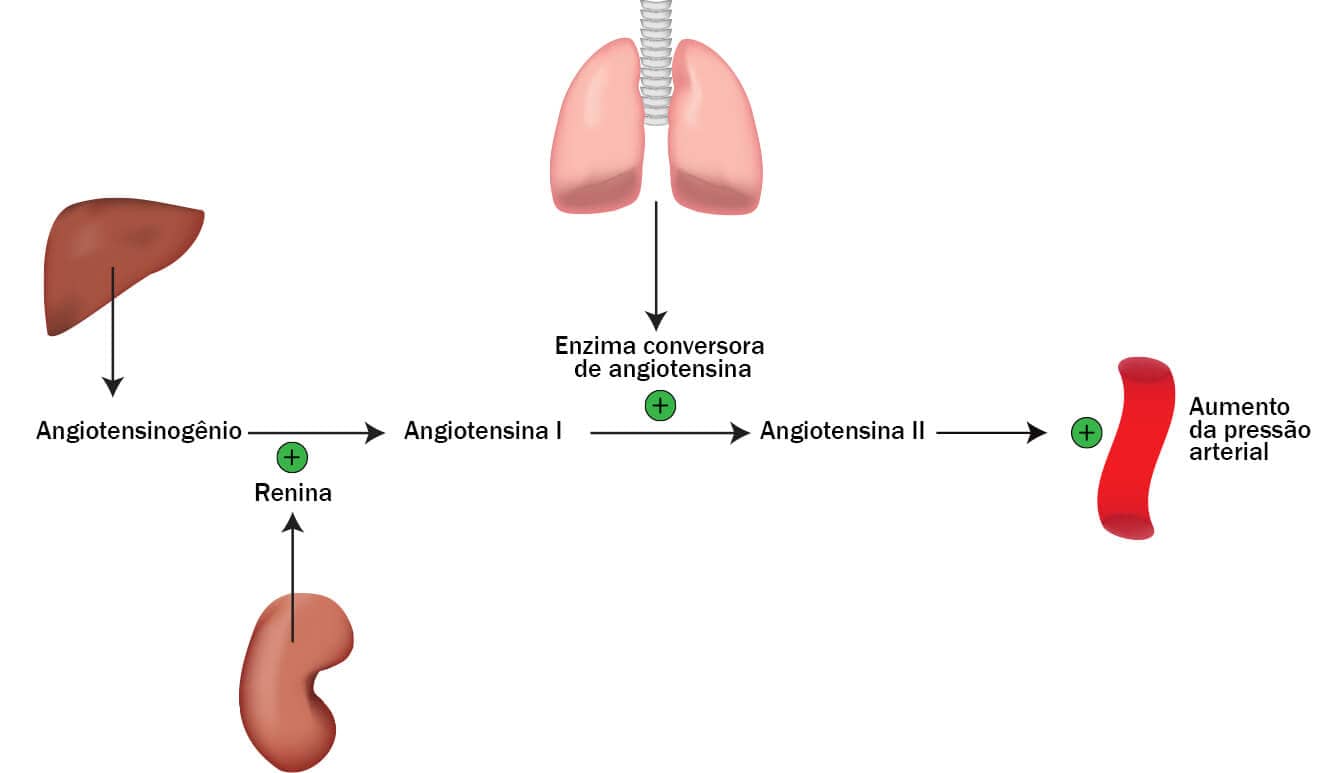
A longo prazo, existe um sistema importante no mecanismo de regulação da pressão, o sistema renina-angiotensina-aldosterona. Este sistema é considerado como peptidérgico com características endócrinas, cujo substrato principal é o angiotensinogênio, uma α-glicoproteína predominantemente produzida no fígado.
O angiotensinogênio é clivado pela enzima renina, secretada pelas células do aparelho justaglomerular nas arteríolas aferentes nos rins, as quais convertem o angiotensinogênio à forma de um decapeptídeo, denominado angiotensina I.
A angiotensina I não possui atividade biológica tão relevante e o seu aumento leva à formação de um octapeptídeo, denominado de angiotensina II. A reação de conversão da angiotensina I para angiotensina II é catalisada pela ação da enzima conversora de angiotensina (ECA), que é expressa em altas concentrações pelo endotélio da circulação pulmonar.
A ação da angiotensina II, via receptor AT1-R, está acoplada à proteína Gq que por sua vez, ativa a fosfolipase C-beta (PLCβ). A PLCβ ativada age sobre o fosfatidilinositol 4,5-bifosfato (PIP2) transformando-o em dois subprodutos: inositol 1,4,5-trifosfato (IP3) e o diacilglicerol (DAG).
O IP3 difunde-se rapidamente para o citosol e age em canais de cálcio do retículo sarcoplasmático, promovendo a liberação de Ca2+ desta organela, que ativa uma proteína cinase C (PKC). A PKC promove a fosforilação da proteína cinase ativada por mitógeno (MAPK) que, por sua vez, promove a ativação de outras cinases, tais como: cinase p38, cinase reguladora de sinal extracelular (ERK), cinase c-jun terminal (JNK), janus cinase e transdutores de sinal e ativadores de transcrição (JAK/STAT). Todas essas cinases ativam e aumentam a expressão de fatores de transcrição (ATF2, ATF6, c-Jun, Elk1, GATA4 e MEF2) que participam da regulação da proliferação e do crescimento celular, desencadeando hipertrofia cardíaca.
Atenção
Por isso, a angiotensina II é considerada o principal peptídeo ativo do sistema renina-angiotensina-aldosterona que, ao agir em receptores específicos na musculatura lisa vascular (receptores do tipo 1, AT1-R), produz vasoconstrição intensa, aumento da reabsorção de Na+, resultando no aumento da pressão arterial. Adicionalmente, interage com receptores do córtex da glândula supra adrenal, estimulando a produção e liberação da aldosterona, que interage com receptores mineralocorticoides nos túbulos renais estimulando a reabsorção de sódio e a secreção de potássio. Tal efeito irá promover o aumento do volume sanguíneo (volemia) e o aumento da pressão arterial.
OS MECANISMOS REGULATÓRIOS DA PRESSÃO ARTERIAL
Assista ao vídeo que demonstra os mecanismos de regulação de curto e longo prazo da pressão arterial.
Atividade 3
Conclusão
O que você aprendeu neste conteúdo?
- Estrutura do coração e dos vasos sanguíneos.
- Circulação sistêmica e pulmonar
- Automatismo cardíaco.
- Potencial cardíaco lento e rápido.
- Controle intrínseco e extrínseco do coração.
- Débito cardíaco e retorno venoso.
- Redistribuição do fluxo sanguíneo e manutenção da temperatura corporal.
- Regulação da pressão arterial em curto e longo prazo.
Podcast
Agora, o especialista abordará, de forma resumida, as doenças relacionadas ao sistema cardiovascular abordadas ao longo do tema: insuficiência cardíaca, doença arterial coronariana, infarto do miocárdio e hipertensão arterial sistêmica.
CONQUISTAS
Você atingiu os seguintes objetivos:
Descreveu a organização do sistema cardiovascular
Compreendeu os mecanismos responsáveis pelo controle do ritmo cardíaco
Reconheceu os fenômenos associados à função miocárdica e seu papel na manutenção do débito cardíaco e retorno venoso
Comparou as respostas hemodinâmicas relacionadas à redistribuição do fluxo sanguíneo e à manutenção da pressão arterial