Descrição
Farmacologia e uso clínico de fármacos anti-hipertensivos e diuréticos. Farmacologia e uso clínico de fármacos anticoagulantes, hemostáticos, trombolíticos e antitrombóticos.
PROPÓSITO
Compreender as características de cada classe de fármacos, para alcançar o controle eficiente da pressão arterial e a aplicabilidade clínica do uso de diuréticos, e o princípio da terapia com anticoagulantes, hemostáticos, trombolíticos e antitrombóticos, que terão como fundamento a redução de mortalidade e da recorrência de eventos cardiovasculares.
Preparação
Antes de iniciar o conteúdo deste tema, tenha em mãos um dicionário de Termos Técnicos em Saúde para entender termos específicos da área.
OBJETIVOS
Módulo 1
Descrever a classificação, os mecanismos de ação, os principais efeitos farmacológicos e a aplicabilidade clínica dos fármacos anti-hipertensivos
Módulo 2
Descrever a farmacologia e a aplicabilidade clínica dos agentes anticoagulantes, hemostáticos, trombolíticos e antitrombóticos
Introdução
Neste tema, aprenderemos as características dos diferentes fármacos que atuam no sistema cardiovascular e renal. Entenderemos as estratégias farmacológicas para atuar nesse sistema, que integra a hemodinâmica vascular e os fatores de coagulação, garantindo a normalização da pressão arterial e a prevenção de eventos cardiovasculares.
MÓDULO 1
Descrever a classificação, os mecanismos de ação, os principais efeitos farmacológicos e a aplicabilidade clínica dos fármacos anti-hipertensivos
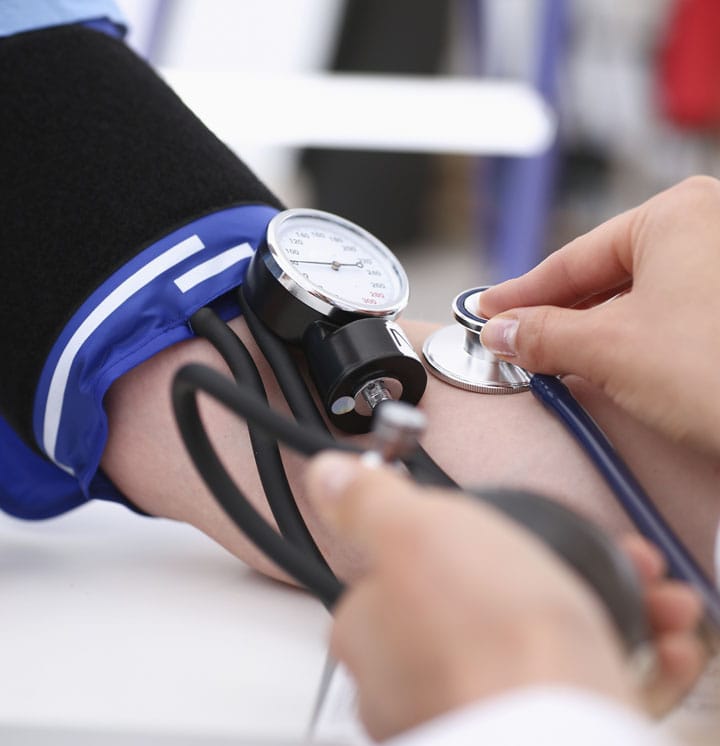
HIPERTENSÃO ARTERIAL SISTÊMICA
A hipertensão arterial sistêmica é uma doença cardiovascular crônica responsável pela maior parte dos eventos cardiovasculares e cerebrovasculares da população mundial, e muitos desses eventos podem ser prevenidos com tratamento precoce e adequado.
A HAS é definida pela condição clínica multifatorial caracterizada por elevação sustentada da pressão arterial sistólica ≥ 140 e/ou da pressão arterial diastólica ≥ 90 mmHg. A pré-hipertensão é uma condição caracterizada por PAS entre 121 e 139 e/ou PAD entre 81 e 89 mmHg.
Acredita-se que indivíduos pré-hipertensos devem ser monitorados, pois boa parte deles poderá desenvolver HAS futuramente. O diagnóstico e estadiamento da hipertensão baseiam-se em medidas repetidas e reproduzíveis da elevação da pressão arterial acima dos parâmetros estabelecidos pelas diretrizes internacionais que vemos na tabela a seguir.
| Classificação da PA de acordo com a medição casual ou no consultório a partir de 18 anos de idade | ||
|---|---|---|
| Classificação | PAS (mm Hg) | PAD (mm Hg) |
| Normal | ≤ 120 | ≤ 80 |
| Pré-hipertensão | 121-139 | 81-89 |
| Hipertensão estágio 1 | 140-159 | 90-99 |
| Hipertensão estágio 2 | 160-179 | 100-109 |
| Hipertensão estágio 3 | ≥ 180 | ≥ 110 |
Em 90% dos casos de HAS, não há uma causa definida, mas, em 10% deles, é possível identificar uma causa específica, e, então, é considerada hipertensão secundária. Algumas das causas são passíveis de tratamento, como o feocromocitoma, a constrição da artéria renal, coarctação da aorta, doença de Cushing e o aldosteronismo primário.
Uma vez diagnosticada a HAS, o paciente será orientado a fazer alterações nos seus hábitos de vida e na dieta. Algumas mudanças podem normalizar os níveis de pressão arterial de pacientes com hipertensão leve e retardar o início da terapia farmacológica, como, por exemplo:

Práticas regulares de exercícios físicos

Redução da ingestão de sal

Redução da ingestão de bebidas alcoólicas

Parar o tabagismo
A abordagem terapêutica da HAS inclui medidas não medicamentosas, como citado anteriormente, e o uso de fármacos anti-hipertensivos, com o objetivo de normalizar a pressão arterial, proteger os órgãos-alvo e prevenir desfechos cardiovasculares e renais.
A REGULAÇÃO DA PRESSÃO ARTERIAL
Para abordarmos os aspectos farmacológicos da terapia anti-hipertensiva, precisamos entender, em primeiro lugar, como ocorre o controle da pressão arterial no organismo.
Sabemos que a pressão arterial é diretamente proporcional ao produto do débito cardíaco pela resistência vascular sistêmica, ou seja:
Para que seja caracterizada a HAS, um desses componentes (ou os dois) tem de estar aumentado. Lembrando que o DC é composto pelo produto da frequência cardíaca pelo volume sistólico. A FC é determinada principalmente pela atividade simpática proveniente da atividade do sistema nervoso central, e o VS depende das condições de pré e pós-carga e da contratilidade cardíaca. A RVS dependerá, principalmente, do estado contrátil das arteríolas do sistema microvascular.
Pré e pós-carga
A pré-carga representa o grau de enchimento do ventrículo esquerdo, dependendo do retorno venoso. A pós-carga representa carga combinada do sangue no ventrículo e da resistência durante a contração ventricular.
A pressão arterial é mantida pela regulação contínua do DC e da RVS
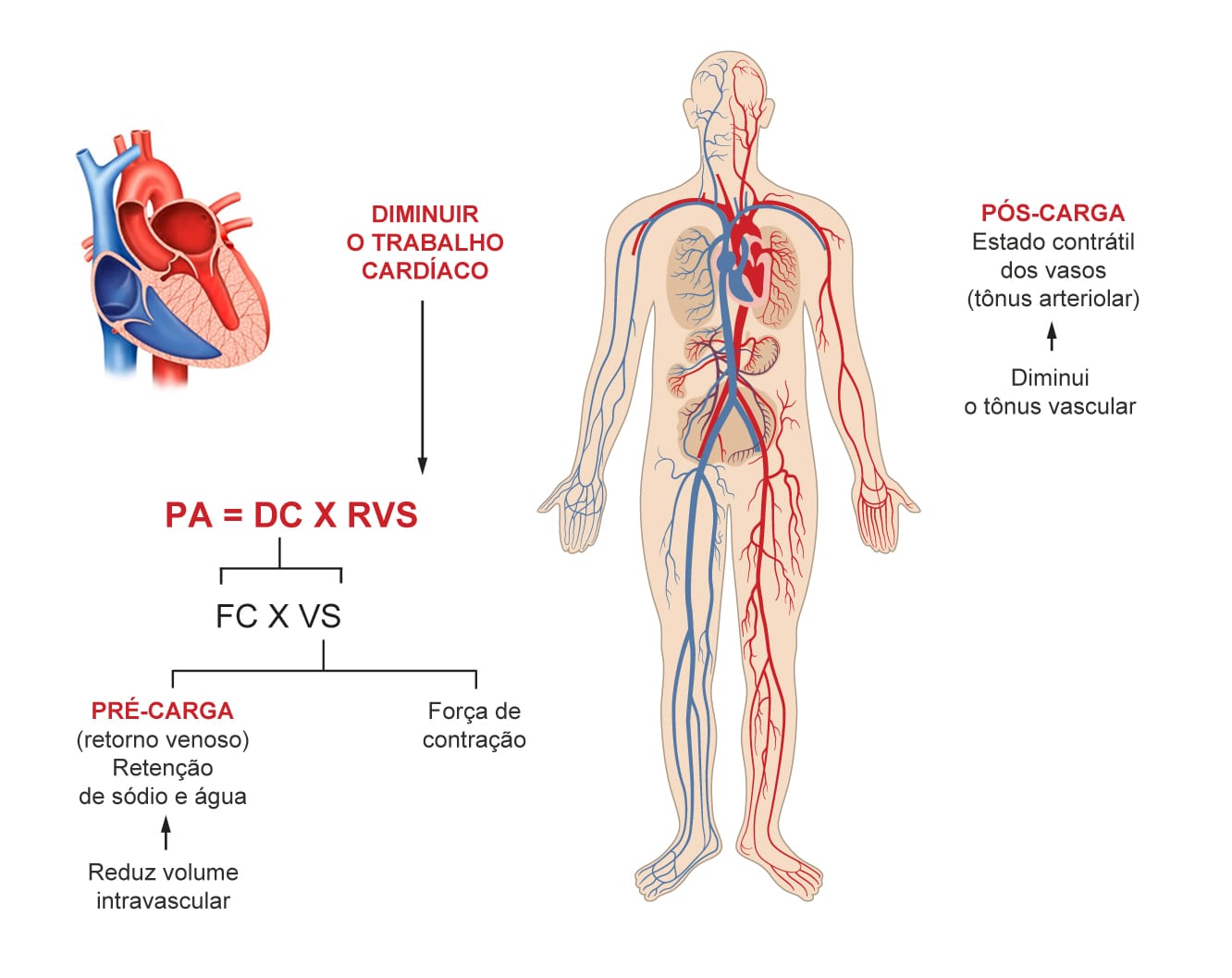
Sendo assim, fica mais claro de entender que agentes anti-hipertensivos podem ser eficazes em diminuir a PA através da redução do tônus arteriolar, do volume intravascular ou do trabalho cardíaco. Esta regulação conta com quatro locais de controle:

O coração, atuando como a bomba desse circuito fechado.

As arteríolas de resistência.

As veias e vênulas de capacitância
Os rins, que controlam os níveis de sódio e água no sangue, e, portanto, o volume intravascular.
O comportamento da pressão arterial é muito dinâmico, variando em situações simples do cotidiano, como o ato de falar, levantar-se, exercitar-se, ou até mesmo em virtude do estresse emocional. O motivo dessa variabilidade é a influência do sistema nervoso autônomo na pressão arterial.
O sistema barorreflexo é mediado por nervos autônomos que atuam juntamente a mecanismos humorais, como o sistema renina-angiotensina-aldosterona, orquestrando as funções dos quatro locais de controle da pressão arterial citados anteriormente.
Além dos controles centrais e humorais, ainda estão presentes fatores vasoativos, que agem no nível do endotélio vascular, contribuindo para a dilatação (como o óxido nítrico e as prostaglandinas, por exemplo) ou constrição (endotelinas e tromboxanos, por exemplo) dos vasos sanguíneos, diminuindo ou aumentando a RVS, respectivamente.
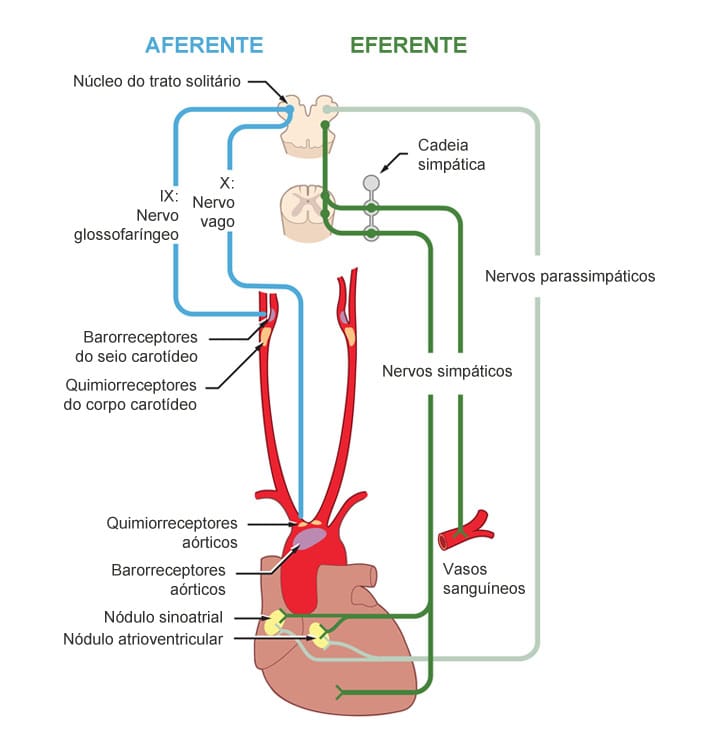
O sistema barorreflexo representa o ajuste rápido da pressão arterial, como na transição da posição de decúbito para a ereta ou redução do volume sanguíneo intravascular por uma hemorragia, por exemplo. Os barorreceptores aórticos e carotídeos são constantemente ativados pelo estiramento das paredes arteriais em resposta ao aumento da pressão intravascular. Por outro lado, quando ocorre redução do estiramento, ou seja, queda da pressão arterial, há redução da ativação dos barorreceptores.
A ativação barorreflexa inibe a descarga simpática central, reduzindo a ação constritora das catecolaminas nas arteríolas e no miocárdio, diminuindo, assim, a RVS e o DC, respectivamente. Além da via simpática, há também a via parassimpática, onde ocorre aumento da atividade vagal e queda da FC.
O sistema de controle dos barorreceptores tem pouca importância na regulação a longo prazo da pressão arterial, pois eles se reajustam, entre 1 e 2 dias, a qualquer nível de pressão a que sejam expostos. No entanto, no paciente hipertenso, parece haver disfunção dos barorreceptores, atenuação da sensibilidade barorreflexa e hiperatividade simpática.
O sistema renina-angiotensina-aldosterona representa o controle a longo prazo da pressa arterial. Esse sistema determinará o controle do volume sanguíneo através de retenção de sódio e água nos rins. A renina é uma enzima produzida no aparelho justaglomerular das arteríolas aferentes renais, em resposta à redução da perfusão renal, por queda da pressão arterial ou pelo aumento da atividade simpática, com ativação dos receptores β-adrenérgicos.
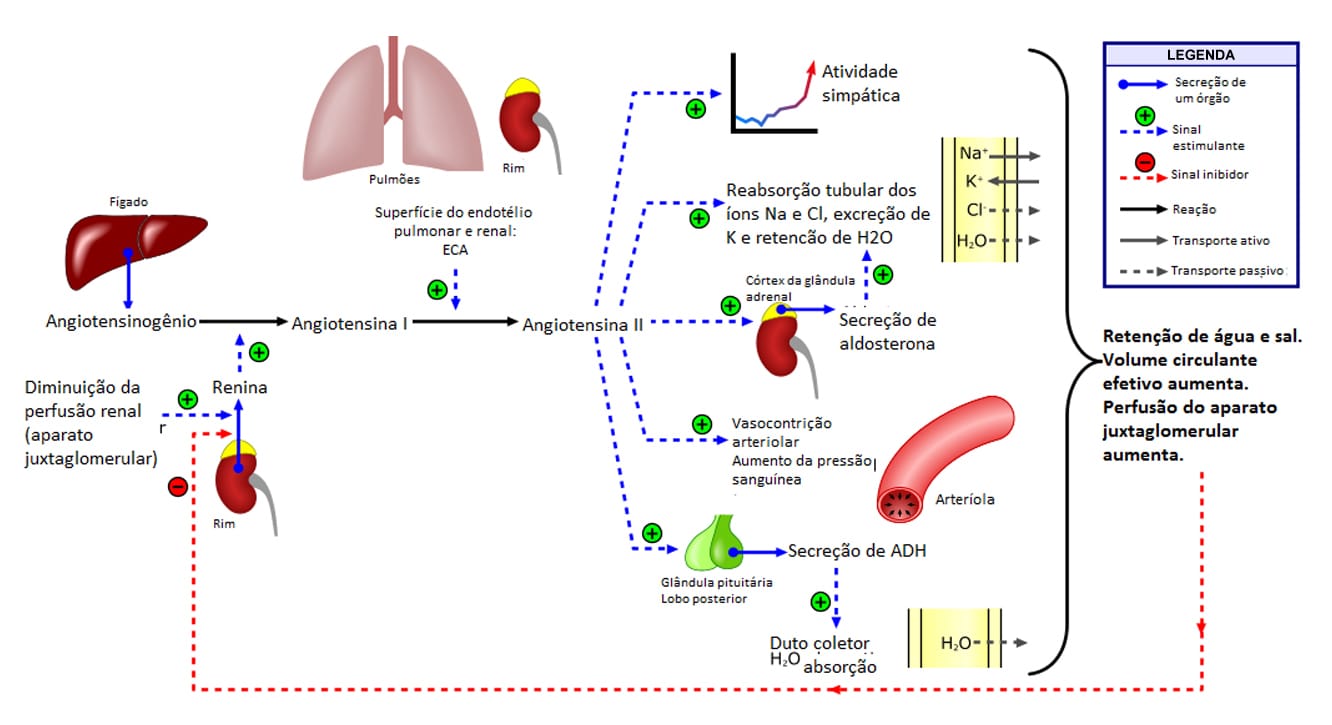
A sua função primordial é converter o angiotensinogênio em angiotensina I no plasma. A enzima conversora de angiotensina, presente no plasma e em diversos tecidos, converte a angiotensina I em angiotensina II. Esta última exerce efeitos importantes no aumento da PA, como constrição arterial e venosa e estímulo da síntese de aldosterona pela suprarrenal, causando retenção de sódio e água pelos rins. Além disso, a Ang II causa efeitos tróficos tanto nos vasos como no miocárdio, contribuindo para o processo de remodelamento vascular e remodelamento cardíaco, respectivamente.
Remodelamento vascular
Processo de hipertrofia de células do musculo liso vascular, prejudicando a vasodilatação.
Remodelamento cardíaco
Processo de hipertrofia das células miocárdicas, aumentando a massa cardíaca, prejudicando a capacidade contrátil do coração.
MANEJO FARMACOLÓGICO DA HIPERTENSÃO ARTERIAL SISTÊMICA
Considerando que o DC e a RVS são os componentes determinantes da PA, torna-se mais fácil compreender as estratégias farmacológicas dos fármacos anti-hipertensivos e seus locais de ação.
O tratamento da HAS visa, além da redução da pressão arterial, a diminuição da morbimortalidade cardiovascular. Evidências científicas mostraram os benefícios de alguns tratamentos em monoterapia, mas a maioria dos estudos evidenciou a melhora efetiva de eventos cardiovasculares com a associação de diferentes classes de medicamentos.
As categorias de fármacos anti-hipertensivos podem ser divididas em:
Simpaticolíticos
Fármacos que reduzem os efeitos do sistema nervoso simpático.
Inibidores do sistema-renina-angiotensina-aldosterona
Fármacos que bloqueiam a produção ou ação da Ang II.
Vasodilatadores
Fármacos que relaxam o músculo liso vascular.
Bloqueadores de canais de cálcio
Fármacos que reduzem influxo de cálcio nas células musculares lisas arteriais.
Diuréticos
Fármacos que reduzem o volume intravascular.
A imagem a seguir ilustra a ação dos fármacos anti-hipertensivos.
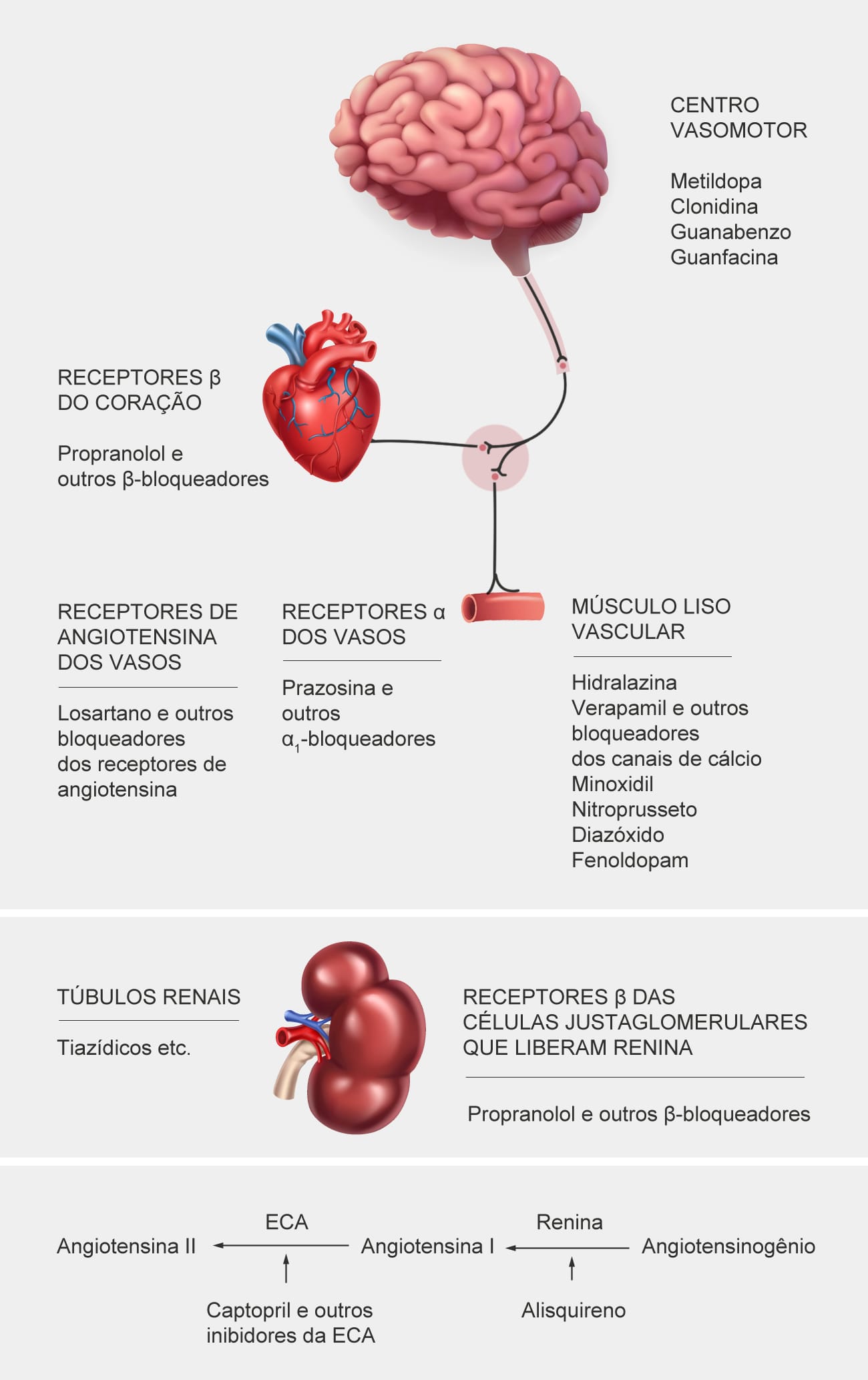
A seguir, veremos com mais detalhes cada categoria de fármacos anti-hipertensivos.
Simpaticolíticos: fármacos que reduzem o tônus simpático
Esta classe de fármacos anti-hipertensivos reduz a PA pelo fato de modificarem a função simpática, causando redução da RVS e o DC. Os fármacos podem ser divididos em subclasses: betabloqueadores, alfabloqueadores e agentes de ação central.
Agora, vamos conhecer cada subclasses em detalhes.
Betabloqueadores ou antagonistas β-adrenérgicos
Promovem diminuição inicial do DC e da secreção de renina, havendo readaptação dos barorreceptores e diminuição das catecolaminas nas sinapses nervosas. Os representantes dessa classe são:
Veja as principais características farmacológicas dos simpaticolíticos:
Esses fármacos são antagonistas de receptores β-adrenérgicos e atuam inibindo a ação das catecolaminas endógenas, da adrenalina e noradrenalina nos receptores β1-adrenérgicos cardíacos, diminuindo o inotropismo e cronotropismo, reduzindo, assim, o DC. Além disso, o antagonismo β-adrenérgico diminui a produção renal de renina e, consequentemente, os níveis de angiotensina e aldosterona. Os betabloqueadores têm efeitos protetores cardíacos, por reduzirem o consumo de oxigênio pelo miocárdio, além de efeito antiarrítmico, prevenindo a morte súbita pós- infarto agudo do miocárdio. O uso prolongado de betabloqueadores parece diminuir o tônus vasomotor, com consequente redução da RVS.
Esses fármacos apresentam diferenças na seletividade pelos receptores β-adrenérgicos, além de efeitos de bloqueio concomitante dos receptores α-1 adrenérgicos (carvedilol e labetalol) ou aumento da síntese de óxido nítrico no endotélio vascular (nebivolol). A seletividade pelos receptores β1 cardíacos, como atenolol, bisoprolol, metoprolol e nebivolol, por exemplo, garante o efeito anti-hipertensivo, enquanto a ação não seletiva do propranolol, além de atuar sobre os receptores β1, interage também com os receptores β2 dos brônquios e hepatócitos, causando broncoconstrição e bloqueio da gliconeogênese hepática mediada pelas catecolaminas – principais efeitos adversos da classe.
Os betabloqueadores apresentam diferenças na lipossolubilidade, onde os agentes lipossolúveis, como o propranolol, metoprolol e bisoprolol, apresentam maior metabolismo hepático e meia-vida mais curta, além de atravessarem a barreira hematoencefálica, causando efeitos adversos no SNC. Para reduzir esses efeitos, tais fármacos podem ser prescritos em formulação de liberação prolongada (bisoprolol, nebivolol).
HAS leve a moderada, para pacientes pós-infarto do miocárdio e doença coronariana sintomática. Na insuficiência cardíaca, o uso preferencial é do carvedilol.
Broncoespasmo, hipoglicemia, insônia, pesadelos, depressão psíquica, astenia e disfunção sexual. Em doses altas, os betabloqueadores seletivos perdem a seletividade. Não se deve interromper o tratamento de forma abrupta, pois, caso isso seja feito, pode ocorrer aumento rebote da pressão arterial, taquicardia e tremores pelo fenômeno de suprarregulação dos receptores.
Asma, bradiarritmias, insuficiência cardíaca descompensada, diabetes.
Alfabloqueadores ou antagonistas α1-adrenérgicos
São exemplos dessa classe de anti-hipertensivos:

Doxazosina

Prasozina

Terazosina
Veja as principais características farmacológicas dos alfabloqueadores:
Os medicamentos desta classe agem como antagonistas competitivos dos α1-receptores pós-sinápticos, inibindo o tônus da musculatura arterial e venosa, que está constantemente ativado pelas catecolaminas circulantes, levando à vasodilatação arteriolar e redução da RVS e do retorno venoso pela venodilatação, no início do tratamento. Porém, com o uso prolongado, o DC é normalizado. Esses fármacos reduzem a PA principalmente na posição ortostática, e ocorre retenção de sal e água, quando administrados sem diuréticos. Os alfabloqueadores têm efeito benéfico no perfil lipídico, reduzindo LDL-colesterol e os triglicerídeos e aumentando HDL-colesterol.
Não são a primeira escolha para pacientes hipertensos. Opta-se, preferencialmente, pelo uso associado a β-bloqueadores ou diuréticos. São indicados para hipertensos com hiperplasia prostática benigna.
Dependendo da dose, podem causar hipotensão postural e taquicardia, “fenômeno de primeira dose”, em 50% dos pacientes, principalmente quando fazem uso de diuréticos. Pode ocorrer o fenômeno de tolerância, levando ao aumento da dose ao longo do uso. Além disso, causa incontinência urinária em mulheres.
Há evidências de que os pacientes tratados com doxazosina têm maior risco de
incidência de
Inibidores de ação central
Os simpaticolíticos de ação central causam a diminuição da atividade simpática central e do barorreflexo. Fazem parte dessa classe:
Veja as principais características farmacológicas dos inibidores de ação central:
Os fármacos desta classe reduzem a pressão arterial por agirem no SNC, ativando os receptores pré-sinápticos α2-adrenérgicos centrais (metildopa, clonidina e guanabenzo) e receptores imidazolínicos centrais (clonidina, rilmenidina e moxonidina), diminuindo a liberação de noradrenalina no tronco encefálico e a atividade simpática eferente do SNC, tendo como consequência a diminuição da RVS e do DC. Os níveis de renina também são reduzidos pela inibição adrenérgica.
A metildopa é um pro-fármaco metabolizado nos neurônios adrenérgicos à sua forma ativa α-metilnorepinefrina que agirá nos receptores α2 -adrenérgicos centrais. É excretada em sua forma ativa na urina, e seu tempo de meia-vida (t ½) é prolongado na insuficiência renal.
Não são a primeira escolha para monoterapia em pacientes hipertensos, devido aos seus efeitos variados no sistema nervoso central, como boca seca, sedação, depressão e hipotensão postural. O uso da clonidina pode ser favorável em hipertensão associada a situações de síndrome de pernas inquietas, retirada de opioides, diarreia associada à neuropatia diabética, hiperatividade associada à cirrose alcoólica. O diagnóstico de feocromocitoma pode ser feito com a clonidina, onde a ausência da supressão de concentrações de noradrepinefrina sugere tumor. A metildopa é o fármaco preferido para hipertensão na gravidez, por causar vasodilatação e não atravessar a barreira placentária, garantindo a segurança da mãe e do feto.
Sedação e xerostomia são os mais evidentes, mas podem ser minimizados com a clonidina transdérmica ou com a rilmenidina, por agirem em receptores imidazolínicos. Além de depressão, causam dificuldade de concentração, disfunção sexual, síndrome de abstinência e “crise de rebote”, em virtude da retirada abrupta, o que pode ser perigoso em pacientes com hipertensão não controlada. Esse fenômeno ocorre pela suprarregulação dos receptores adrenérgicos pós-sinápticos, que ficam disponíveis quando os níveis de noradrenalina voltam a aumentar. Vale ressaltar que os diuréticos potencializam seu efeito hipotensor e antidepressivos tricíclicos podem inibir seus efeitos anti-hipertensivos.
Inibidores do sistema-renina-angiotensina-aldosterona: fármacos que bloqueiam a produção ou ação da Ang II
No início deste modulo, vimos a importância da Ang II no controle das funções cardiovasculares. Assim, entende-se que a redução da sua síntese, como também a inibição de seus receptores nos órgãos-alvo, representa uma importante estratégia terapêutica no tratamento da HA.
Fazem parte dessa classe:
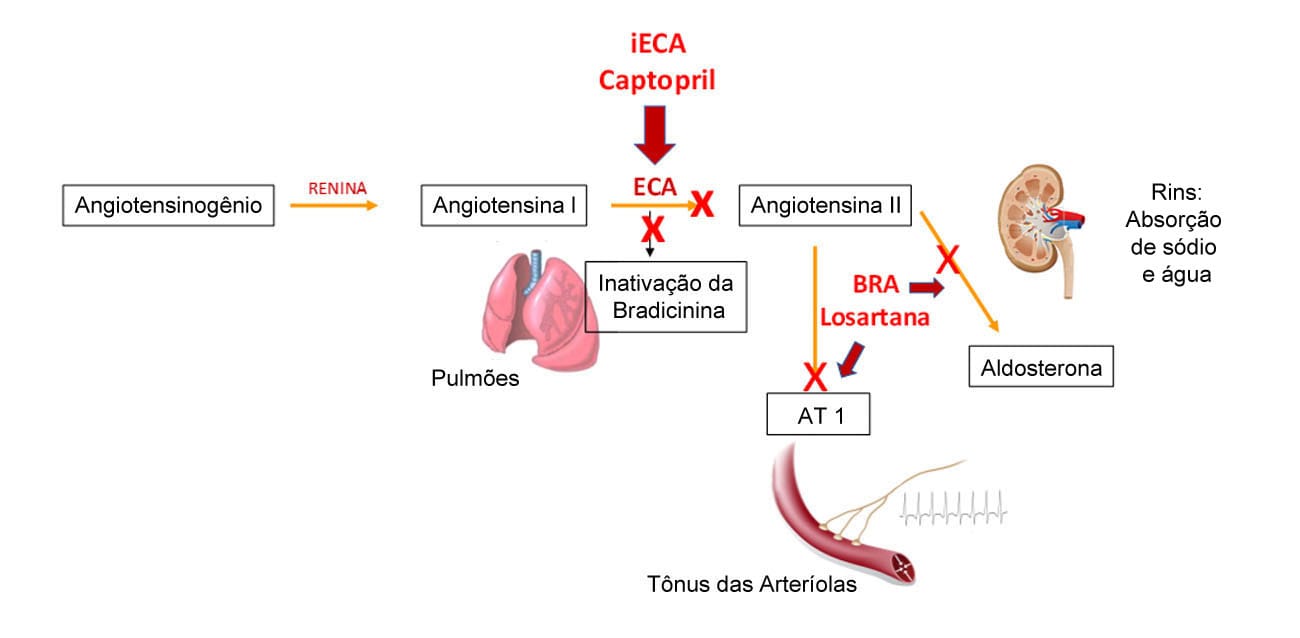
Mecanismo de ação: o captopril e outros desta classe, como enalapril, quinalapril e lisinopril, são fármacos que têm como ação principal a inibição da enzima que converte a Ang I em Ang II, peptídeo que apresenta ação vasoconstritora arterial, reduzindo a RVS e venodilatadora, diminuindo o retorno venoso e o DC. Além disso, a redução da Ang II circulante tem como consequência a atenuação da secreção de aldosterona pela suprarrenal e leve efeito natriurético. Esta mesma enzima inativa a bradicinina, que tem ação vasodilatadora e estimuladora de óxido nítrico e prostaciclina; portanto, a inibição da ECA exacerba os efeitos vasodilatadores da bradicinina e os irritativos na árvore brônquica, causando tosse seca. Além disso, a resposta adrenérgica reflexa à vasodilatação é inibida, não acarretando a taquicardia reflexa.
Os iECA têm efeito nefroprotetor, pois apresentam vasodilatação preferencial das arteríolas eferentes renais, causando redução da hiperfiltração glomerular. Uma vantagem expressiva desta classe de fármacos é a prevenção dos efeitos tróficos da Ang II sobre o remodelamento cardíaco e vascular, melhorando a função cardíaca e a rigidez vascular.
São fármacos administrados por via oral e apresentam algumas diferenças nas suas características farmacológicas. O captopril é ativo por VO, tem rápida absorção, e sua biodisponibilidade é reduzida na presença de alimentos, t ½ de 2h e depuração renal. O enalapril e o quinalapril são pro-fármacos com rápida absorção VO, metabolismo hepático por esterases para sua ativação, t ½ inicial de 2h, mas a t ½ terminal é de 25h (alta afinidade pela ECA tecidual), excreção renal e pelas fezes. Já o lisinopril sofre lenta absorção, sua biodisponibilidade não é afetada pela presença de alimento, t ½ de 12h e é excretado inalterado na urina.
Indicações: HAS, hipertensos com insuficiência cardíaca com fração de ejeção reduzida, pós-infarto do miocárdio, além de possíveis propriedades antiateroscleróticas e pacientes com nefropatia diabética ou de outras etiologias.
Efeitos adversos: tosse seca, angioedema, hipercalemia, hipotensão de primeira dose (pacientes hipovolêmicos).
Contraindicação: estenose da artéria renal, broncoespasmo e gravidez.
Fazem parte desse grupo a losartana, candesartana, valsartana e olmesartana.
Mecanismo de ação: ligam-se com maior afinidade e seletividade aos receptores AT1 do que pelos AT2 da Ang II, antagonizando os efeitos da Ang II sobre esses receptores em diversos tecidos. Logo, a inibição dos receptores AT1 da Ang II na musculatura lisa vascular causa vasodilatação arterial e venosa, semelhante aos efeitos dos iECA. No entanto, os BRA não aumentam os níveis de bradicinina, responsáveis pelos efeitos de tosse seca e broncoespasmo. Em contraste com os iECA, esses fármacos permitem a ação da Ang II sobre os receptores AT2, que apresentam efeitos vasodilatadores e inibidores da proliferação celular. São fármacos ativos por VO e apresentam diferentes características farmacológicas com relação aos seus metabolismos, interações com outros medicamentos e alimentos e o processo de excreção. A candesartana e a losartana são pro-fármacos que são convertidos à sua forma ativa no TGI ou no fígado, respectivamente.
Indicações: todos os BRA são aprovados para o tratamento da HAS, nefropatia diabética, profilaxia do acidente vascular encefálico e insuficiência cardíaca. Além de reduzir a pressão arterial, esses fármacos diminuem o remodelamento vascular e cardíaco. São semelhantes aos iECA, e não foi estabelecido se as diferenças farmacológicas resultam em alterações nos desfechos clínicos; porém, esses fármacos podem substituí-los quando o paciente não tolera a tosse induzida por tais medicamentos.
Efeitos adversos: são bem tolerados. Com exceção da tosse seca e de broncoespasmos, os efeitos adversos dos BRA são semelhantes aos dos iECA. É possível que aumente os efeitos de outros anti-hipertensivos, podendo exigir o ajuste da dose. Assim como os iECA, têm efeito teratogênico e são contraindicados na gravidez.
Alisquireno, único representante da classe disponível para uso clínico, promove a inibição direta da ação da renina, mas não foi estudado o suficiente para ser prescrito em monoterapia para a hipertensão. Não existem, contudo, evidências de seus benefícios sobre morbimortalidade. Evidências de associação com iECA ou antagonista dos receptores AT1 mostraram que o bloqueio completo do sistema renina-angiotensina traz mais prejuízo do que benefícios ao paciente.
Efeitos adversos: “Rash” cutâneo, diarreia (especialmente
com doses elevadas, acima de
Vasodilatadores
Os medicamentos que representam essa classe são:
Hidralazina
Mecanismo de ação da hidralazina: ainda é incerto, mas pode atuar reduzindo as concentrações intracelulares de cálcio, relaxando a musculatura lisa arterial, levando à redução da RVS, mas não age sobre as vênulas. Apresenta diminuição seletiva da resistência de arteríolas na circulação vascular coronariana, cerebral e renal, rápida absorção por via oral e metabolismo hepático. Embora sua t ½ seja de 1 hora, o seu efeito hipotensor pode se estender por até 12 horas.
Indicação: hipertensão grave, mulheres com pré-eclâmpsia. Na insuficiência cardíaca congestiva, pode ser combinada com dinitrato de isossorbida, apresentando importante efeito venodilatador, reduzindo também a pré-carga, facilitando o trabalho ventricular. Essa associação é reservada a pacientes que não podem tolerar os inibidores da ECA.
Efeitos adversos: cefaleia, náuseas, rubor, hipotensão, taquicardia, tontura e angina de peito. Se administrado isoladamente, pode ocorrer retenção de sal, levando a IC de alto débito. Reações imunológicas semelhantes à síndrome lúpica podem ocorrer com o tratamento a longo prazo, exigindo sua interrupção.
Minoxidil
Mecanismo de ação do minoxidil: provoca vasodilatação arteriolar através da abertura dos canais de potássio ATP sensíveis, causando hiperpolarização e retardo da despolarização. O efeito do relaxamento da musculatura é somente arteriolar, e não venular, com redução da RVS e queda da PA e sem alteração no retorno venoso. É um fármaco bem absorvido por via oral e eliminado como glicuronídeo – 20% inalterado na urina.
Indicação: hipertensão grave e insuficiência renal que não responde à hidralazina em dose máxima; uso tópico para tratamento da calvície e tratamento de hipoglicemia.
Efeitos adversos: hipotensão intensa; estimulação simpática reflexa com taquicardia e retenção de líquido, levando ao acidente vascular encefálico e infarto do miocárdio – por isso, deve ser associado a β-bloqueadores e diuréticos de alça –, e hiperglicemia, pela inibição da liberação de insulina.
Nitropreusseto de sódio
Mecanismo de ação do nitroprusseto de sódio: este fármaco age por meio da liberação de óxido nítrico no musculo liso vascular, causando dilatação arteriolar e venosa, tendo como consequência a redução da RVS e do retorno venoso.
O nitroprusseto é uma molécula estável e é degradada em condições alcalinas ou em exposição à luz. É administrado por via parenteral, por infusão venosa. É metabolizado rapidamente pela captação dos eritrócitos com liberação de cianetos e óxido nítrico, e seu metabólito tiocianato é eliminado pelos rins. O efeito é de curta duração, 1 a 10 minutos após suspensão do fármaco.
Indicação: emergências hipertensivas, IC grave. Indução de hipotensão controlada na anestesia, para evitar sangramentos em procedimentos cirúrgicos.
Efeitos adversos: a curto prazo, a vasodilatação excessiva e suas consequências. Quando é utilizado por mais de 24 horas em infusão, a toxicidade por cianeto pode ocorrer, causando anorexia, náusea, fraqueza, psicose e convulsão.
Bloqueadores de canais de cálcio
São fármacos que reduzem influxo de cálcio nas células musculares lisas arteriais. Os bloqueadores dos canais de cálcio compõem um importante grupo de fármacos no tratamento da HAS. São classificados em dois grupos, de acordo com sua estrutura química:
Diidropiridinas
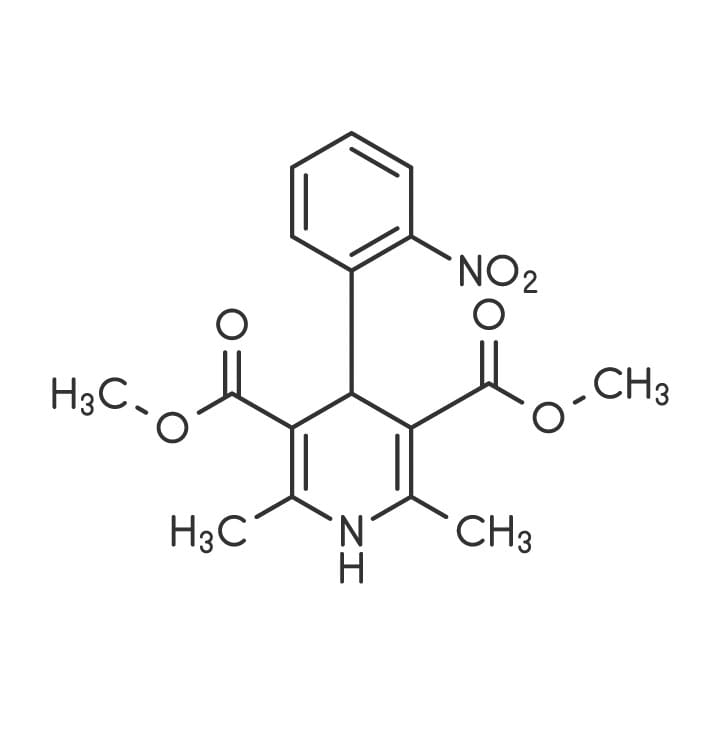
Nifedipina
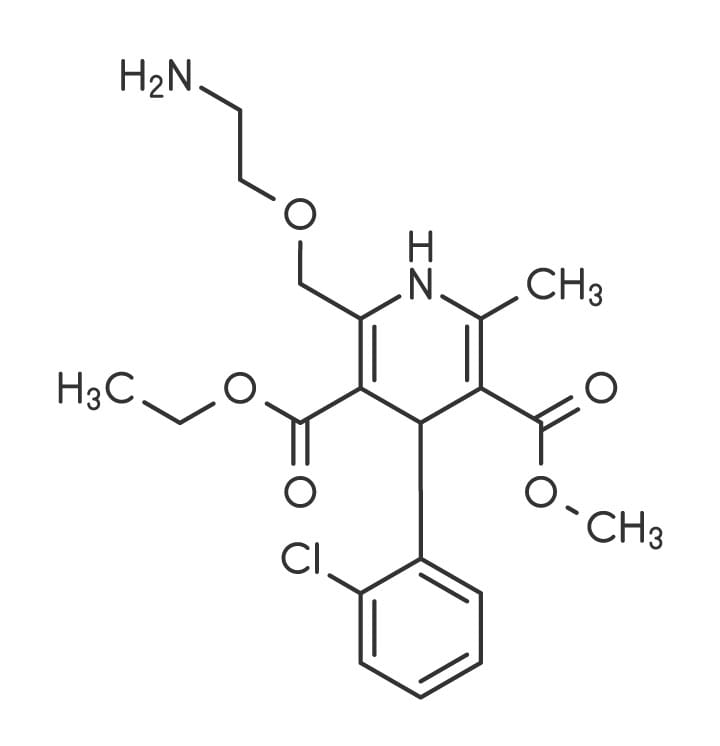
Anlodipino
Não diidropiridinas (benzotiazepinas e fenilalquilaminas)
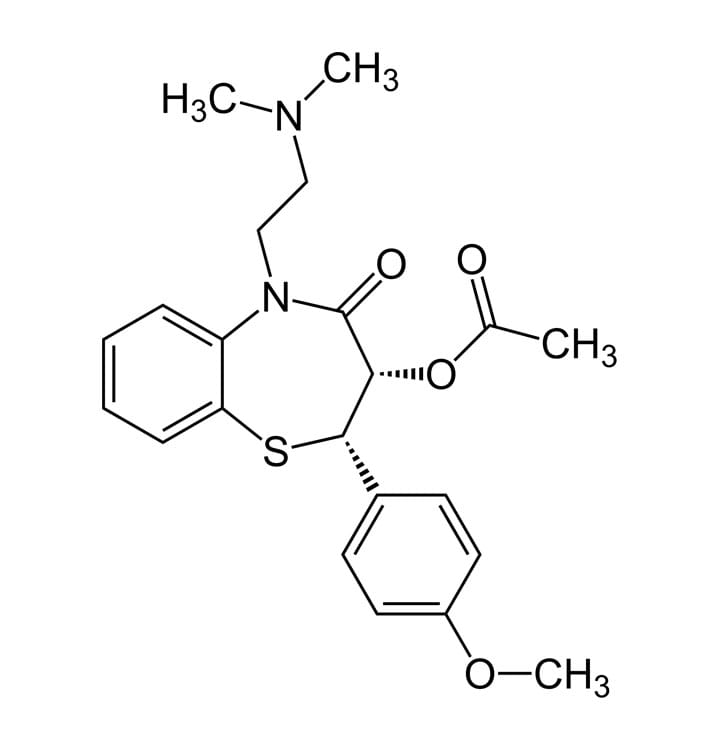
Diltiazem
Verapamil
Veja as principais características farmacológicas dos bloqueadores de canais de cálcio:
Mecanismo de ação
Bloqueiam os canais de cálcio tipo L da membrana celular, reduzindo o influxo de cálcio. Nifedipina e anlodipino apresentam seletividade para receptores do músculo liso vascular, principalmente em artérias e arteríolas, diminuindo mais a RVS do que o DC. Já o diltiazem e a verapamil possuem seletividade pelos receptores dos cardiomiócitos, reduzindo o inotropismo, o cronotropismo e, portanto, o DC. Um efeito renal também está presente, já que a vasodilatação das arteríolas aferentes renais melhora o fluxo renal e a filtração glomerular. Outro efeito benéfico é a vasodilatação coronariana, conferindo propriedade antianginosa a esse fármaco.
Indicação
Estão entre os fármacos preferidos para o tratamento da HAS, tanto em monoterapia como em associações com outros anti-hipertensivos. São considerados antianginosos, antiarrítmicos; têm eficácia superior aos iECA e β-bloqueadores na população negra. Deve-se dar preferência aos agentes vasosseletivos de ação prolongada, a fim de que sejam evitadas oscilações indesejáveis na FC e na PA. São anti-hipertensivos eficazes e reduzem a morbimortalidade CV.
Efeitos adversos
Aqueles relacionados à vasodilatação para os da família das di-hidropiridinas (nifedipina e anlodipino): edema periférico, cefaleia, tontura e nervosismo; efeitos depressores cardíacos com verapamil e diltizem: bradicardia e bloqueio AV.
Diuréticos: fármacos que reduzem o volume intravascular
Esta classe de fármacos tem como efeito anti-hipertensivo inicial a natriurese, com perda de sódio corporal, acompanhado de aumento da excreção de água e, portanto, redução do volume sanguíneo e do DC. Após algumas semanas de tratamento, o volume sanguíneo se normaliza e ocorre também a redução da RVS.
Diuréticos tiazídicos
Os diuréticos tiazídicos, como hidroclorotiazida, clorotizida ou similares, como a clortalidona e indampamida, apresentam, na sua estrutura química, um grupo sulfonamida.
Veja as principais características farmacológicas dos diuréticos tiazídicos:
Mecanismo de ação
Consiste na inibição do simporte de Na+-Cl- (NCC) no túbulo contorcido distal nos néfrons, inibindo, assim, a reabsorção de NaCl para a circulação. Ocorre também reabsorção passiva de Ca2+.
Os tiazídicos são bem absorvidos por via oral; no entanto, a clorotiazida é o único tiazídico disponível para administração parenteral, e a hidroclorotiazida é mais potente que as demais. A clortalidona apresenta absorção mais lenta e ação mais prolongada. Todos os tiazídicos são secretados pelo sistema secretor de ácidos orgânicos no túbulo proximal e competem com a secreção de ácido úrico, podendo elevar seus níveis séricos.
Indicação
São fármacos de primeira escolha em monoterapia para o tratamento de hipertensão leve a moderada, reduzindo a pressão arterial em 10 a 15 mmHg na maioria dos pacientes. Para pacientes com hipertensão grave, os diuréticos são usados em associação com outros agentes, como simpaticoplégicos e vasodilatadores diretos. Podem ser utilizados na redução de edema relacionado à insuficiência cardíaca congestiva, doença hepática e renal.
Efeitos adversos
Seus principais efeitos adversos são dependentes da dose, e o uso de doses baixas diminui o risco desses efeitos, sem prejuízo da eficácia anti-hipertensiva. São eles: fraqueza, câimbras, hipovolemia, hipopotassemia, eventualmente acompanhada de hipomagnesemia, que podem induzir arritmias ventriculares e impotência (especialmente com a clortalidona).
Contraindicações
Pacientes com hiperuricemia com história de gota pela reabsorção de Ca2+ citada anteriormente.
Diuréticos de alça
Os diuréticos de alça são agentes de alta potência diurética, causando redução importante da volemia e, portanto, do retorno venoso. São representados por furosemida, bumetamina, torsemida e ácido etacrínico.
Veja as principais características farmacológicas dos diuréticos de alça:
Mecanismo de ação
São fármacos que agem na porção ascendente da alça de Henle, inibindo o cotransportador de Na+-K+-2Cl- (NKCC2), resultando em aumento de 25% da excreção de sódio, além de K+, Ca2+ e água.
A furosemida tem biodisponibilidade oral que varia de 10-100%; 65% é excretada inalterada na urina, e o restante é conjugado com ácido glicurônico nos rins, tendo a sua t ½ aumentada na insuficiência renal. Já a bumetamina e a torsemida possuem alta biodisponibilidade oral e metabolismo hepático, tendo a sua t ½ aumentada na doença hepática.
Indicação
Não são fármacos utilizados no tratamento crônico da HAS. São fármacos reservados para hipertensão grave e crise hipertensiva, por seu efeito rápido, situações de edema, como na ICC, insuficiência renal, quando a taxa de filtração glomerular é <30 mL/min, e cirrose hepática.
Efeitos adversos
Semelhantes aos tiazídicos, exceto os efeitos no Ca2+, pois, diferente dos tiazídicos, aumentam a excreção urinária de cálcio, sendo contraindicados na litíase renal. Podem causar ototoxicidade pelas alterações no transporte de eletrólitos no ouvido interno de pacientes com comprometimento preexistente. Interações medicamentosas: ototoxicidade com aminoglicosídeos e cisplatina; aumento da atividade de anticoagulantes; hiperglicemia com sulfonilureias; arritmias com digitálicos .
Diuréticos poupadores de potássio
São fármacos utilizados na hipertensão associados aos diuréticos para reverter ou prevenir a hipocalemia e hipomagnesemia. Os fármacos representantes desta classe são a espironolactona, eplerenona e amilorida; apresentam pouco ou nenhum efeito diurético e podem já vir associadas aos diuréticos tiazídicos ou de alça.
Veja as principais características farmacológicas dos diuréticos poupadores de potássio:
Mecanismo de ação
A espironolactona e a eplerenona agem como antagonistas do receptor da aldosterona, reduzindo a troca de Na+-K- no túbulo distal e ducto coletor do néfron. Já a amilorida interfere com o mecanismo envolvido na troca de sódio por potássio no túbulo contorcido distal e no túbulo coletor do néfron, o que diminui o potencial líquido negativo do lúmen tubular e a secreção de potássio e hidrogênio e sua subsequente excreção.
A amilorida apresenta biodisponibilidade oral de 15-15%, tem t ½ de 21h e é eliminada intacta pela excreção renal. O triantereno apresenta biodisponibilidade oral de 50% e t ½ mais curta de 4h. Já a espironolactona é absorvida parcialmente, sofre metabolismo hepático e, apesar de ter t ½ curta, de 1,5h, seus metabólitos apresentam t ½ longas.
Efeitos adversos
Hiperpotassemia, em particular em pacientes com déficit de função renal. A espironolactona (mas não a eplerenona, por ser mais moderna e seletiva) pode causar ginecomastia. O triantereno pode reduzir a tolerância à glicose e induzir à fotossensibilidade.
Diuréticos osmóticos
O manitol é o protótipo dos diuréticos osmóticos. É um açúcar osmoticamente ativo, mas não é reabsorvido no sistema renal e no TGI, por isso provoca retenção de água e promove a diurese hídrica.
Veja as principais características farmacológicas dos diuréticos osmóticos:
Mecanismo de ação
Exerce efeito osmótico no túbulo proximal e no ramo descendente da alça de Henle, impedindo a reabsorção de água e aumentando o volume urinário. É pouco absorvido pelo TGI e, quando administrado por via oral, provoca mais diarreia osmótica. Este fármaco não é metabolizado e é excretado por filtração glomerular em até 1h. Quando administrado por via intravenosa, causa aumento do fluxo urinário com maior diurese hídrica do que natriurese, levando, por fim, à perda excessiva de água, com desenvolvimento da hipernatremia.
Indicações
Redução da pressão intracraniana e intraocular antes de procedimentos cirúrgicos.
Efeitos adversos
IC e edema pulmonar. Cefaleia, náuseas, vômitos, desidratação e, em pacientes com disfunção renal, o fármaco fica retido no sangue, causando hiponatremia.
Diuréticos em estados edematosos e não edematosos
Neste vídeo, a Professora Vanessa Freitas fala sobre a aplicação de diuréticos no tratamento de doenças que causam edemas e aquelas que não causam, ressaltando que diurese provoca melhora do quadro.
Verificando o aprendizado
ATENÇÃO!
Para desbloquear o próximo módulo, é necessário que você responda corretamente a uma das seguintes questões:
O conteúdo ainda não acabou.
Clique aqui e retorne para saber como desbloquear.
MÓDULO 2
Descrever a farmacologia e a aplicabilidade clínica dos agentes anticoagulantes, hemostáticos, trombolíticos e antitrombóticos

FÁRMACOS QUE IMPEDEM OU REDUZEM A FORMAÇÃO DE TROMBOS
Diversas doenças cardiovasculares que acometem as artérias, como infarto agudo do miocárdio, acidente vascular encefálico e isquemia periférica, ou comprometem as veias, como a trombose venosa profunda e a embolia pulmonar, decorrem de oclusões ou trombos na vasculatura. Logo, existem agentes farmacológicos que podem ser utilizados para impedir ou reverter esse quadro.
Os anticoagulantes e antiagregantes são fármacos que agem na prevenção da formação de trombos, e os fibrinolíticos são usados como tratamento de intervenção em trombos já formados. Em condições normais, há equilíbrio entre a formação de coágulos no sangue (hemostasia) e a decomposição desses (fibrinólise).
Para impedir ou reduzir a formação de trombos, existem três principais tipos de fármacos: anticoagulantes, antiagregantes plaquetários (ou antiplaquetários) e trombolíticos.
Veremos cada tipo a seguir.
ANTICOAGULANTES
São fármacos que impedem a formação de trombina e da fibrina.
Assim como os antiplaquetários, são utilizados tanto para prevenção quanto para o tratamento de doenças trombóticas. São indicados no manejo de síndromes coronarianas agudas e na anticoagulação profilática e terapêutica.
Vamos conhecer os principais representantes desta classe.
Heparina não fracionada (HNF) e de baixo peso molecular (HBPM)
A heparina não fracionada por muito tempo foi a única opção como anticoagulante parenteral. Atualmente, já existem formas mais seletivas, como as de baixo peso molecular. As heparinas impedem a coagulação intravascular, impossibilitando a cascata de coagulação. A heparina interage com a antitrombina, inibindo o fator X e a trombina.
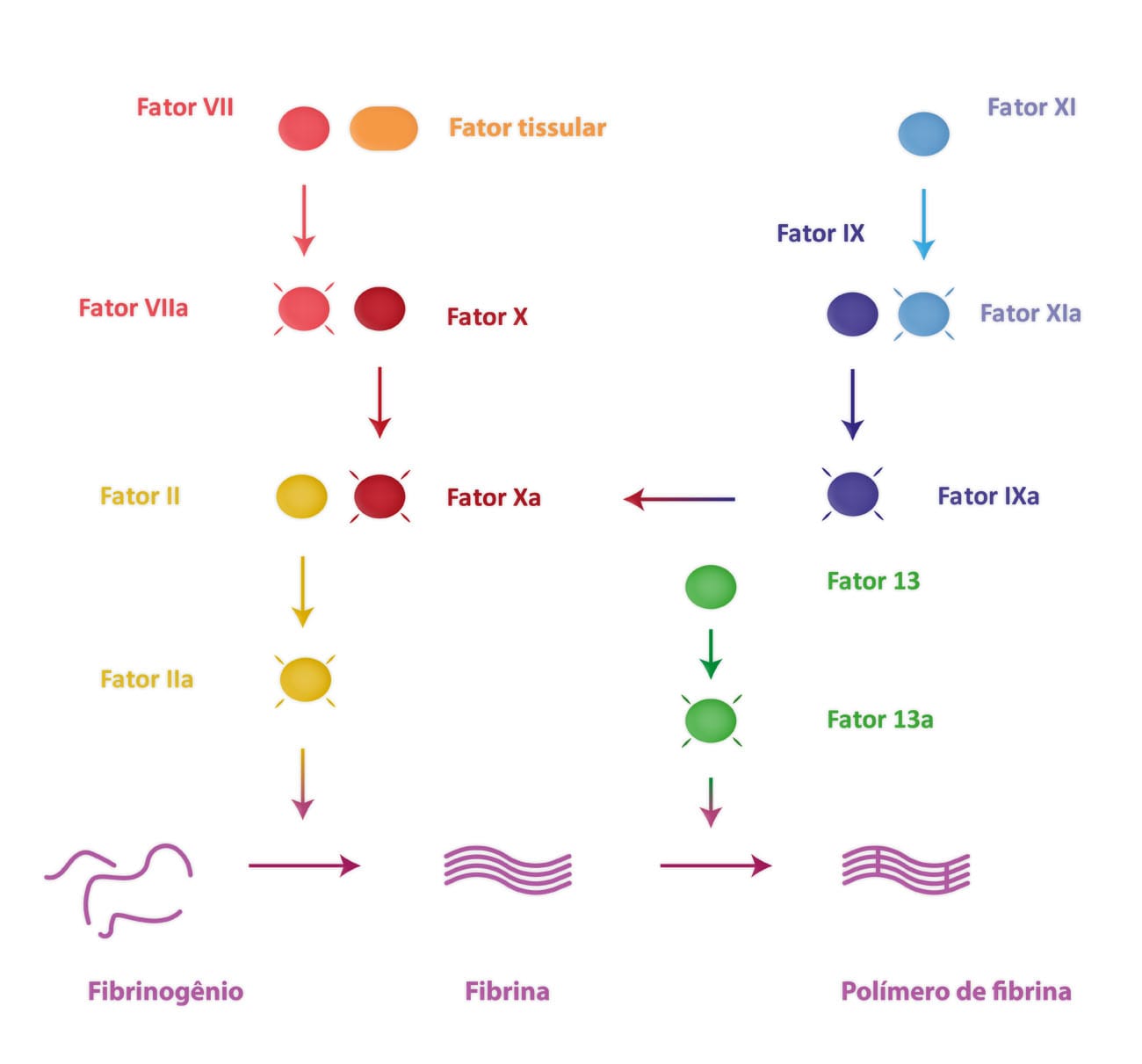
A HNF é preparada a partir do pulmão bovino ou da mucosa intestinal suína e apresenta alto peso molecular, de 5 a 30 kDa. Já a HBPM é preparada por cromatografia, a partir da HNF, e seu peso molecular pode variar de 1 a 5 kDa.
A diferença do mecanismo de ação entre a HNF e a HBPM se dá pela ligação à trombina e ao fator X, onde a HNF tem tamanho suficiente para se ligar a esses fatores ao mesmo tempo, inativando a trombina e o fator X. Já a HBPM só é capaz de interagir e inativar o fator Xa.
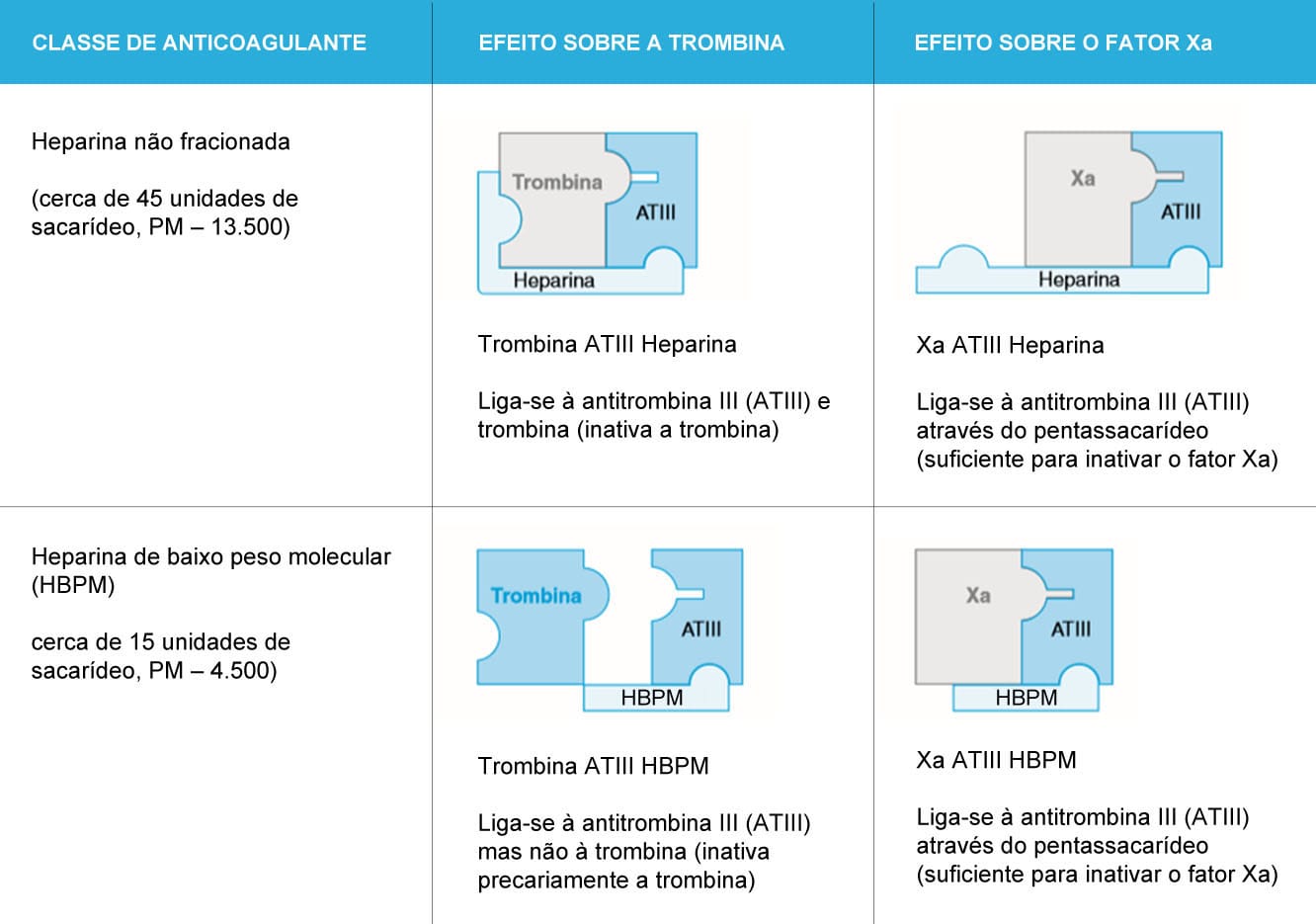
Estes fármacos apresentam algumas diferenças na sua farmacocinética, na resposta coagulante e na forma de administração.
Indicação: fármaco de primeira linha para pacientes com quadro agudo de TVP e EP. Apresenta t ½ de 2h, biodisponibilidade de 20% e só pode ser administrada pela via parenteral em ambiente hospitalar.
Efeitos adversos: incluem hemorragias, necrose na pele nos locais de injeção, osteoporose pelo uso crônico, trombocitopenia grave e hipersensibilidade.
São exemplos os fármacos enoxaparina e dalteparina.
Apresentam menor ligação inespecífica, proporcionando uma resposta farmacológica mais previsível. É excretada por via renal, necessitando de ajuste de dose na insuficiência renal. Apresentam t ½ de 4h e maior biodisponibilidade. Podem ser usadas pelo paciente em domicílio via SC.
Indicação: prevenção de TVP e EP e complicações isquêmicas associadas a angina instável primária e infarto agudo do miocárdio.
Efeitos adversos: semelhantes aos com HNF, porém menos frequentes. Não há necessidade de monitoramento rotineiro, pois existem testes para o monitoramento da atividade do fator Xa em pacientes de risco, como grávidas e nefropatas.
O antídoto sulfato de protamina forma o complexo irreversível, com a heparina, inativando-a e revertendo hemorragias.
Contraindicações: hemofilia, úlceras e sangramento intestinais, trombocitopenia, cirurgias recentes.
Inibidores diretos da trombina: hirudina e bivalirudina (parenterais)
Os inibidores diretos da trombina a bloqueiam sem a necessidade de cofatores e sem intervir em outros mecanismos pró-trombóticos. Essa ação, independente de cofatores, torna as antitrombinas drogas potentes para evitar a trombose, pois não há individualidade de ação, como ocorre com os coatores, e, por ter ação direta, neutraliza a trombina onde ela se encontrar. Os inibidores diretos da trombina têm duas vantagens inquestionáveis em substituição ao complexo antitrombina-heparina: na plaquetopenia induzida por heparina e na deficiência congênita de antitrombina.
Dabigatrana (oral)
Recentemente lançado no mercado brasileiro, trata-se de um inibidor reversível do sítio ativo da trombina. É um agente para uso oral que requer monitorização laboratorial. Cerca de 80% da droga é excretada via renal, não sendo recomendável seu uso em pacientes com insuficiência renal moderada a grave.
Efeitos adversos: o uso contínuo pode aumentar o risco de sangramento perioperatório. Não há antagonista direto.
Inibidores diretos orais do fator Xa
Os inibidores do fator Xa orais, como o fondaparinux e a rivaroxabana, podem agir diretamente, ligando-se ao sítio ativo de ação, ou indiretamente, catalisando a ação da antitrombina. Possui pouca interação com componentes do plasma e, dessa forma, age de maneira previsível com baixa variabilidade individual. Fondaparinux apresenta meia-vida de 17 horas, e rivoroxabana, de 9h; excreção renal; não induz trombocitopenia e não necessita de monitoramento da ação.
Indicação
Sua eficácia tem sido demonstrada em pacientes com maior risco de eventos tromboembólicos e submetidos a cirurgias ortopédicas.
Efeitos adversos
Podem ocorrer sangramentos perioperatórios, mas o risco é baixo.
Varfarina
É um anticoagulante oral. Trata-se de um composto derivado da 4-hidroxicumarina, que tem como mecanismos de ação o antagonismo da vitamina K e a síntese de fatores de coagulação sanguínea, como os fatores II, VII, IX e X, além de cofatores, como as proteínas C e S. Apresenta boa disponibilidade por via oral, absorção no TGI e t ½ de 36-42h. Acumula-se no fígado, onde é metabolizada. Seu efeito depende do tempo de protrombina do paciente.
Tempo de protrombina
O tempo de protrombina, TP ou TAP é um teste para avaliar a via extrínseca e a via comum, ou seja, os fatores VII, X, V, II e o fibrinogênio da cascata de coagulação.
Indicação
Profilaxia e tratamento da embolia pulmonar, trombose venosa profunda, cardiopatia valvar e no uso de próteses valvares.
Efeitos adversos
Hemorragia, hepatite, síndrome de embolização do colesterol e reação de hipersensibilidade. O antídoto para a hemorragia é a administração de vitamina K.
Uso clínico de anticoagulantes no tratamento da COVID-19
Neste vídeo, a Professora Vanessa Freitas fala sobre o uso de anticoagulante para o tratamento da COVID-19 e os cuidados necessários na utilização desses fármacos para este fim.
ANTIAGREGANTES PLAQUETÁRIOS
São fármacos que impedem a adesão e a ativação de plaquetas, como:
Esses fármacos inibem a cicloxiogenase (COX), enzima que converte o ácido araquidônico em prostaglandina H2 e, posteriormente, em tromboxano A2 (TXA2). Este mediador é essencial para a ativação plaquetária, evento fundamental para a agregação das plaquetas. O TXA2 liberado pelas plaquetas ativadas aciona a fosfolipase C (PLC), enzima que age nos fosfolipídios de membrana, ativando a PLA2 e a GPIIb-IIIa, fundamentais para o evento de agregação plaquetária. A COX-1 é a isoforma predominante das plaquetas, enquanto as células endoteliais parecem expressar tanto a COX-1 quanto a COX-2 em condições fisiológicas.
Os fármacos desta classe são os anti-inflamatórios não estereoidais (AINES), e o seu representante é o ácido acetilsalicílico (AAS), a Aspirina. Esta droga difere dos demais AINES, pois inibe, de forma irreversível, a COX plaquetária. O efeito do AAS é duradouro, já que as plaquetas não sintetizam novas moléculas de enzima.
Como o AAS age tanto na COX-1 quanto na COX-2 de modo não seletivo, essa droga atua como agente não plaquetário efetivo. Por outro lado, os inibidores seletivos da COX-2 não podem ser usados como agentes antiplaquetários.
O AAS em baixas doses é utilizado para profilaxia e manejo de doença coronariana aguda, acidente vascular encefálico e infarto agudo do miocárdio.
Efeitos adversos: o tratamento a longo prazo com AAS pode levar a distúrbios gástricos pela eliminação da citoproteção na mucosa gástrica, que seria conferida por eicosanoides (prostaglandinas) produzidos pela COX-1. São eles: dispepsia, lesão e ulceração da mucosa gástrica.
São fármacos que impedem a degradação do AMPc através da inibição da enzima que o degrada, a fosfodiesterase. Logo, ocorre o aumento das concentrações de AMPc dentro da plaqueta que reduz a ativação plaquetária. O dipiridamol exerce esses efeitos, porém tem ação fraca quando administrado sozinho. Por isso, dipiridamol é associado à varfarina para redução de trombos em próteses valvares cardíacas, enquanto a associação do dipiridamol com AAS é indicada para reduzir a probabilidade de trombose em pacientes com trombose.
Efeitos adversos: esses agentes podem induzir angina em pacientes com doença arterial coronariana, pois causam vasodilatação e, apesar de parecer paradoxal, originam um fenômeno chamado sequestro coronariano, fazendo com que haja um desvio do fluxo para as artérias coronárias.
Fármacos como o clopidogrel apresentam dois mecanismos de ação: inibição de forma irreversível da ligação do receptor do ADP, impedindo uma das vias responsáveis pela ativação plaquetária, e inibição do fibrinogênio ao complexo GP IIb/IIIa. A ticlopidina apresenta os mesmos mecanismos que o clopidogrel, além de interferir com a ligação do FvW ao receptor membranar GPIb. Esses fármacos não interferem na via da cicloxiogenase, no entanto apresentam efeitos irreversíveis e sinérgicos com AAS, ou com antagonistas do receptor GPIIb/IIIa. São drogas bem absorvidas por via oral, mas o efeito inibitório sobre as plaquetas só é observado ao final de quatro dias, pois esse é o tempo que leva para toda a cascata de coagulação ser inibida. Outra possibilidade é utilizar uma dose de ataque, para obter um efeito rápido. São indicados na prevenção secundária de acidentes vasculares encefálicos trombóticos em pacientes intolerantes ao AAS ou em associação com o AAS, a fim de prevenir trombose do stent coronariano.
Efeitos adversos: as principais limitações são o efeito antiplaquetário irreversível e a variabilidade desse efeito entre os indivíduos.
Esta classe de antiplaquetários inibe a ligação das plaquetas umas com as outras pelo receptor GPIIb/IIIa através da ponte formada pelo fibrinogênio (como descrito anteriormente). Existem estratégias farmacológicas para inibir esse receptor, e uma delas é o uso de anticorpo monoclonal humano dirigido ao receptor, como o abciximab. Causa a inibição de 50% dos receptores e inibição significativa da coagulação.
Efeitos adversos: hemorragia, trombocitopenia e indução de imunogenicidade.
A tirobifana é indicada em pacientes de alto risco e no pré-operatório de angioplastia. Uma segunda estratégia é o uso de um análogo de tirosina não peptídico, usado por via oral e que antagoniza reversivelmente a ligação do fibrinogênio ao receptor plaquetário GPIIb/IIIa, e foi aprovada para o tratamento de pacientes com síndromes coronarianas agudas e angina estável.
Complexo GP IIb/IIIa
É um heterodímero cálcio-dependente presente nas plaquetas e nos megacariócitos. Esses receptores possibilitam que as plaquetas interajam com plaquetas vizinhas mediadas pelo fibrinogênio, possibilitando a agregação plaquetária.
AGENTES FIBRINOLÍTICOS
São fármacos que estimulam a formação de plasmina e, portanto, a fibrinólise para dissolver um trombo plaquetário.

Rev Soc Cardiol Estado de São Paulo 2018;28(4):421-7.
São fármacos que promovem fluidificação do sangue e são utilizados no tratamento da trombose venosa profunda, embolia pulmonar e na oclusão vascular periférica aguda. São contraindicados para pericardite aguda, hemorragia interna, acidente vascular cerebral recente, feridas profundas, câncer em metástase.
Estreptoquinase
É uma proteína derivada de estreptococos β-hemolíticos, como um componente do mecanismo de destruição tecidual desses microrganismos. Esse fármaco deve ser utilizado por via IV. Ele se liga ao plasminogênio, formando um complexo 1:1 não covalente e estável com o plasminogênio, facilitando a conversão do plasminogênio em plasmina, que degrada os polímeros de fibrina, desfazendo a malha de fibrina formada durante a coagulação.
Efeitos adversos: muito antigênica, pois é derivada dos estreptococos, e seu uso prévio é uma contraindicação, pois pode causar anafilaxia.
Ativador do plasminogênio tecidual recombinante (rt-PA)
São fármacos produzidos pela tecnologia do DNA recombinante. Fazem parte desse grupo:

Alteplase

Tenecteplase

Reteplase
Estas moléculas causam fibrinólise dependente da presença de fibrina, ligando-se apenas no local de um trombo. Possui atividade enzimática semelhante à molécula endógena do ativador de plasminogênio, que tem por efeito final a degradação da fibrina. Acredita-se que essas drogas apresentem menos riscos de hemorragia.
Vamos, agora, discutir uma abordagem prática do uso de fibrinolíticos.

Homem de 39 anos, etilista, hipertenso, procura pronto-socorro queixando-se de dispneia súbita em repouso com início há 12 horas. Seis dias antes da admissão, teve episódio de dor no flanco direito associada à sensação de peso nos membros inferiores, dificultando a deambulação, seguida por episódio de síncope. Paciente negou hemoptise e diagnóstico prévio de trombose venosa profunda (TVP). Verificaram-se pressão arterial de 145x91mmHg, frequência cardíaca de 95bpm, frequência respiratória de 24irpm e saturação de oxigênio de 83%.
Diante da hipótese de tromboembolismo pulmonar (TEP) agudo, foi realizado ecocardiograma
transtorácico em pronto-socorro,
tendo sido evidenciados sinais de dilatação e disfunção de ventrículo direito (VD), com
a presença do
sinal de McConnell.
Foi solicitada uma angiotomografia de tórax, que mostrou trombos endoluminais, confirmando o
diagnóstico. O tratamento no pronto-socorro foi feito com
tenecteplase
O paciente foi anticoagulado com fondaparinux
No caso relatado, os êmbolos sanguíneos são as principais causas de obstrução da circulação pulmonar, sendo fatores de risco as condições que levam aestase venosa, dano endotelial e trombofilias ou estados de hipercoagulabilidade.
A anticoagulação com heparina (não fracionada ou de baixo peso molecular) está bem estabelecida no tratamento desta patologia. No entanto, novos estudos comprovaram que o uso da rivaroxabana, inibidor oral do fator Xa, obteve índices semelhantes de sucesso na prevenção de novos episódios tromboembólicos. O uso dos novos anticoagulantes orais no tratamento do TEP apresenta diversas vantagens, quando comparado à varfarina, como o fato de não necessitarem de ajuste de dose com coagulograma.
Quando usados com sucesso, os medicamentos fibrinolíticos revertem a insuficiência cardíaca direita, ao promoverem dissolução física do trombo responsável pela obstrução da artéria pulmonar. A trombólise também pode melhorar o fluxo sanguíneo nos capilares pulmonares e reduzir a probabilidade de desenvolvimento de hipertensão pulmonar tromboembólica crônica. No entanto, é exigida cautela nesta conduta, já que foi encontrado aumento significativo de sangramentos importantes, incluindo eventos intracranianos.
Adaptado de Sandra Nívea dos Reis Saraiva Falcão et al., 2017.
Sinal de McConnell
Achado ecocardiográfico descrito em pacientes com Tromboembolismo Pulmonar (TEP) Agudo.
Verificando o aprendizado
ATENÇÃO!
Para desbloquear o próximo módulo, é necessário que você responda corretamente a uma das seguintes questões:
O conteúdo ainda não acabou.
Clique aqui e retorne para saber como desbloquear.
Conclusão
Considerações Finais
Neste tema, vimos as descrições dos fármacos utilizados para o tratamento da pressão arterial. É fundamental incentivar a prevenção desta doença, principalmente com ações relativas à educação do paciente com hipertensão, para que ele faça o controle continuado da pressão, evitando que outras condições patológicas, como a insuficiência cardíaca, desenvolvam-se. Afinal, como diz o ditado: “Prevenir é melhor do que remediar”.
Vimos também que a hemostasia é um processo altamente regulado por diversos fatores que devem estar em plena funcionalidade para manter o sangue fluido e a circulação adequada. Fármacos efetivos nesse sistema são amplamente usados em diversas doenças cardiovasculares e devem ser administrados com cautela e acompanhamento médico.
Podcast
CONQUISTAS
Você atingiu os seguintes objetivos:
Lorem ipsum dolor sit amet, consectetur adipiscing elit
Ut enim ad minim veniam, quis nostrud exercitation ullamco
Duis aute irure dolor in reprehenderit in voluptate velit esse