Descrição
Compreensão da farmacocinética e farmacodinâmica dos diferentes tipos de anestésicos locais e utilização de vasoconstritores no intuito de equilibrar as ações vasodilatadoras dos anestésicos.
PROPÓSITO
Entender a estrutura química dos anestésicos locais, seus mecanismos de ação e suas associações com vasoconstritores é essencial para compreender a duração dos seus efeitos no organismo do paciente. Saber escolher o melhor tipo de anestésico a ser empregado nos diferentes tipos de intervenções clínicas que necessitem de um bloqueio temporário da condução nervosa em uma determinada região, sem perda da consciência.
OBJETIVOS
Módulo 1
Compreender conceitos gerais dos anestésicos locais e dos vasoconstritores, e seu comportamento farmacocinético e farmacodinâmico
Módulo 2
Distinguir as características, indicações, possíveis eventos adversos e contra indicações dos anestésicos locais utilizados na prática clínica
Introdução
Neste tema vamos explorar os anestésicos locais mais utilizados em procedimentos que necessitem de um efeito de bloqueio temporário local da condução nervosa, sem levar à perda da consciência do paciente. Iremos também discutir a importância do uso de vasoconstritores associados a alguns anestésicos locais com o objetivo de equilibrar a vasodilatação provocada por esses fármacos. Veremos que as associações entre essas duas classes são amplamente utilizadas, uma vez que os vasoconstritores fazem com que haja menor absorção sistêmica dos anestésicos. Com isso, a duração do efeito analgésico local é maior e o risco de toxicidade pelos anestésicos é menor, devido à sua reduzida concentração na circulação sistêmica.
MÓDULO 1
Compreender conceitos gerais dos anestésicos locais e dos vasoconstritores, e seu comportamento farmacocinético e farmacodinâmico
Conceito e tipos de anestesia
Os anestésicos são fármacos utilizados quando se deseja provocar, em determinada região do corpo, a perda da sensibilidade aos estímulos externos e internos de maneira parcial ou total. Desse modo, dependendo do tipo de anestésico empregado, poderá ou não haver perda da consciência. Para começarmos a discutir os conceitos de anestésicos, é primordial conhecer, mesmo que de forma sucinta, os tipos de anestesias comumente utilizados para bloqueios de nervos, de receptores específicos para dor e de musculaturas.
A anestesia é um procedimento que visa ao bloqueio temporário da condução nervosa, impedindo que o cérebro reconheça um estímulo doloroso. Pode apresentar ação regional, geral ou local. O que irá ditar a escolha da anestesia é o tipo de procedimento e o estado geral do paciente. Vamos conhecer cada uma delas.
Anestesia regional
É indicada para procedimentos considerados mais simples, não havendo necessidade de o paciente estar inconsciente. Nesse tipo de anestesia ocorre apenas um bloqueio regional no local onde será realizado o procedimento; por exemplo, um membro superior ou inferior, ou toda a região inferior do corpo. Existem dois tipos principais de anestesia regional: a raquianestesia (anestesia raquidiana) e a peridural. Basicamente, o que as diferencia é a região na qual é administrado o anestésico. No quadro a seguir, podemos comparar as características dessas anestesias:
|
RAQUIDIANA |
PERIDURAL |
|---|---|
|
Administração de concentrações baixas |
Administração de concentrações mais altas |
|
Administração no espaço subaracnoide, |
Administração no espaço epidural |
|
Dose única |
Múltiplas doses durante o mesmo procedimento, |
|
Menor risco de intoxicação |
Maior risco de intoxicação |
|
Região do procedimento fica |
Região do procedimento fica sensível |
|
Indicada em diversas cirurgias |
Indicada no parto normal |
Observando o quadro, fica a pergunta:
Por que a anestesia peridural é mais usada em procedimentos de parto normal quando comparada à raquidiana?
A razão de escolha se dá pelo fato de o anestésico poder ser administrado de modo contínuo ou espaçado por meio de um cateter, dependendo da necessidade, uma vez que muitos trabalhos de parto duram horas. Esse tipo de anestesia, além de possibilitar que a paciente não sinta dor, não provoca perda da contração uterina, movimentos involuntários extremamente importantes para a expulsão do bebê. Por outro lado, a anestesia raquidiana seria mais indicada no parto cesariana, por não haver necessidade dos movimentos de contração e seu efeito perdurar por até três horas, tempo suficiente para a preparação da paciente e realização de todo o procedimento.
Por que não podemos dizer que esse tipo de anestesia não é local, e sim regional?
Nas anestesias regionais, o fármaco é depositado em locais específicos e promove um bloqueio maior da condução nervosa. Imagine, por exemplo, que um paciente sofreu um corte profundo no pé e necessita de sutura. Se o médico administrar uma anestesia regional, todo o membro inferior do paciente sofrerá interrupção da condução nervosa. Por outro lado, a aplicação da anestesia local próxima à lesão levará a um bloqueio apenas das terminações nervosas daquela região e os impulsos nervosos das outras partes do membro inferior do paciente permanecem normais.
Anestesia geral
A anestesia geral é realizada em procedimentos extremamente invasivos e muitas vezes de duração longa, nos quais utilizam-se anestésicos que provocam a perda de consciência do paciente. Nesses casos, o anestésico é administrado na veia do paciente e/ou inalado a partir de uma máscara, na forma de gás. A duração do efeito está diretamente relacionada com a concentração do fármaco administrado. É comum um paciente submetido a esse tipo de anestesia estar entubado e acoplado a um respirador artificial.
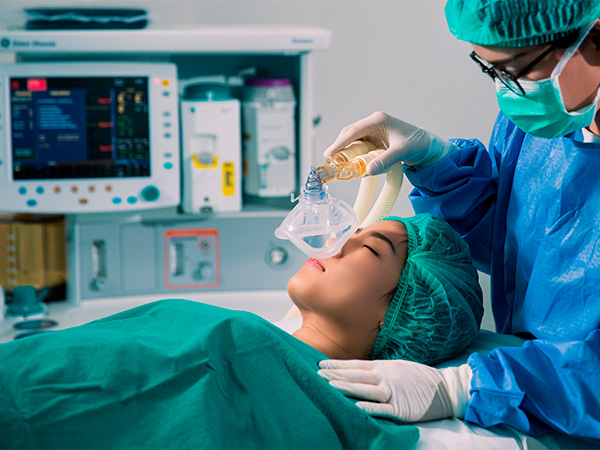
Anestesia local
A anestesia local é a conduta anestésica mais empregada e mais comum, com intuito de levar bloqueio a pequenas regiões do corpo. É muito utilizada em procedimentos como biópsias, punções de veias profundas, suturas de pele, procedimentos odontológicos, dentre outros. Esse tipo de anestesia pode ser utilizado por diversos profissionais, não apenas por anestesiologistas, como ocorre nas anestesias regional e geral. Uma observação de extrema relevância sobre os anestésicos locais é que esses fármacos são encontrados em diferentes preparações farmacêuticas, tais como gel, creme, spray e soluções injetáveis. Portanto, podem ser empregados por administração tópica e por infiltração.
Atenção
É importante ressaltar que a escolha pelo tipo de anestesia deve levar em consideração, além dos aspectos farmacológicos do anestésico, o procedimento a ser realizado no paciente.
Agora que você já entendeu o conceito e conheceu os diferentes tipos de anestesia, vamos nos aprofundar na farmacologia dos anestésicos locais, assunto central deste tema.
Breve histórico dos anestésicos locais
O primeiro anestésico local, que data do final do século XIX, foi a cocaína. Sua descoberta se deu ao acaso, devido a informações coletadas de índios que viviam nos Andes da América do Sul. Eles mascavam as folhas do arbusto da coca, Erythroxylum coca, e descreviam efeitos eufóricos e estimulantes. Até então, a perda – ou a diminuição – da sensibilidade para a execução dos procedimentos em regiões periféricas era obtida com o uso de gelo, neve ou mistura de sal com gelo. Esse fato despertou a curiosidade de um químico alemão chamado Albert Neumann, em meados de 1860, exatos 62 anos após a descoberta da anestesia geral. Ele obteve o extrato alcalino da folha de coca e o experimentou, a fim de observar os efeitos já descritos por algumas pessoas. A administração da droga por via oral ou aplicada localmente provoca midríase, vasoconstrição de artérias periféricas e dormência na língua.
Outros pesquisadores, depois disso, estudaram os efeitos anestésicos da cocaína e fizeram uso dela na prática clínica. Podemos citar como exemplos o pai da psicanálise, Sigmund Freud, usuário de cocaína para fins científicos, estudando a sua ação fisiológica, e o Médico Karl Koller, responsável pelo emprego da cocaína como anestésico tópico em cirurgias oftálmicas, em meados de 1884.
O Cirurgião americano William Stewart Halsted iniciou o uso da cocaína na infiltração e anestesia por bloqueio de condução, após testar a droga em si mesmo e em colaboração com seus estudantes e outros médicos. Seus testes tiveram início após ler um artigo médico europeu que relatava o uso da cocaína como uma alternativa mais segura à morfina na anestesia.
Características químicas e farmacológicas dos anestésicos locais
Compreender a farmacocinética e a farmacodinâmica dos anestésicos locais é fundamental quando se trata de escolher a droga mais adequada para determinados procedimentos que necessitam de uma ação anestésica, sempre visando à segurança do paciente. A escolha do anestésico envolve, principalmente:
• Suas características físico-químicas.
• A duração do efeito farmacológico, que por sua vez deve estar atrelada ao tipo de
procedimento.
• O estado geral do paciente, determinado por fatores como: patologia relatada, alergias
de quaisquer naturezas, lesões cutâneas, medicamentos usados, tabagismo, dentre outros.
Atenção
As características físico-químicas dos anestésicos locais é o que irá decidir sua ação, bem como sua potência em exercer o efeito anestésico e a duração desta anestesia.
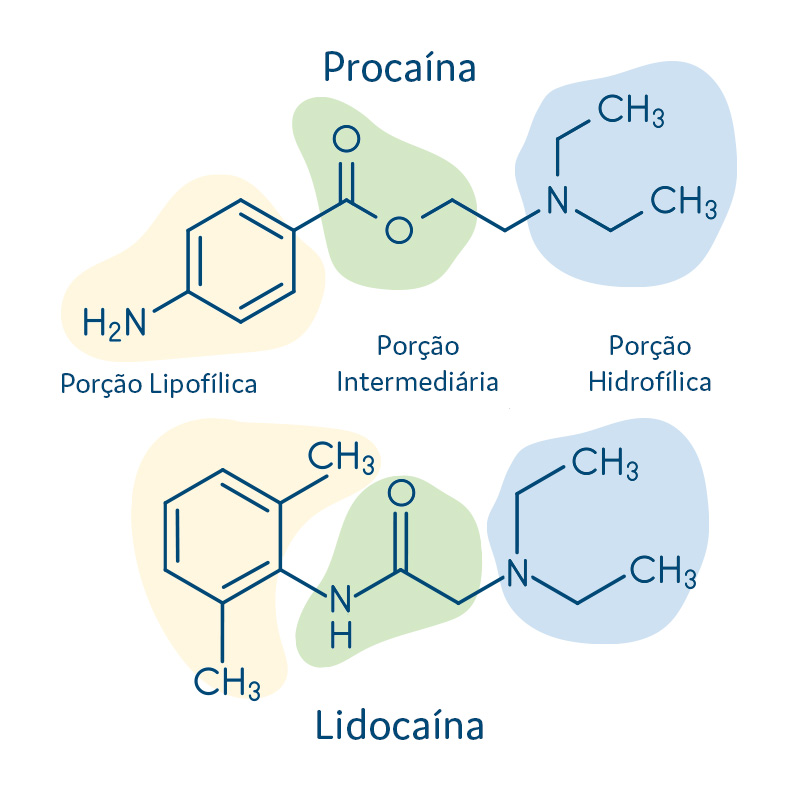
A estrutura química geral dos anestésicos locais é dividida em três partes:
Porção hidrofílica, que usualmente é uma amina secundária ou terciária.
Porção hidrofóbica ou lipofílica, em geral um anel aromático.
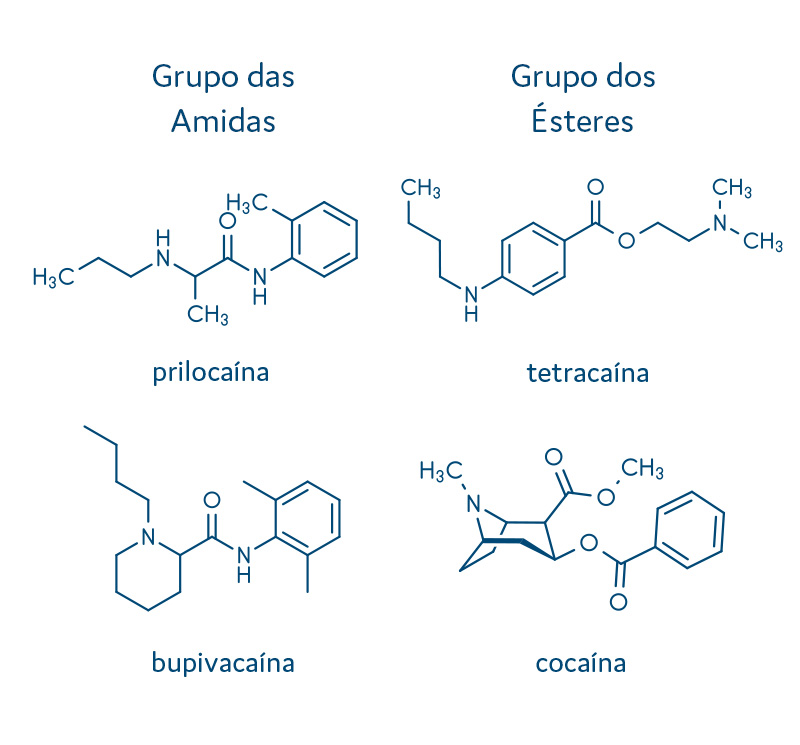
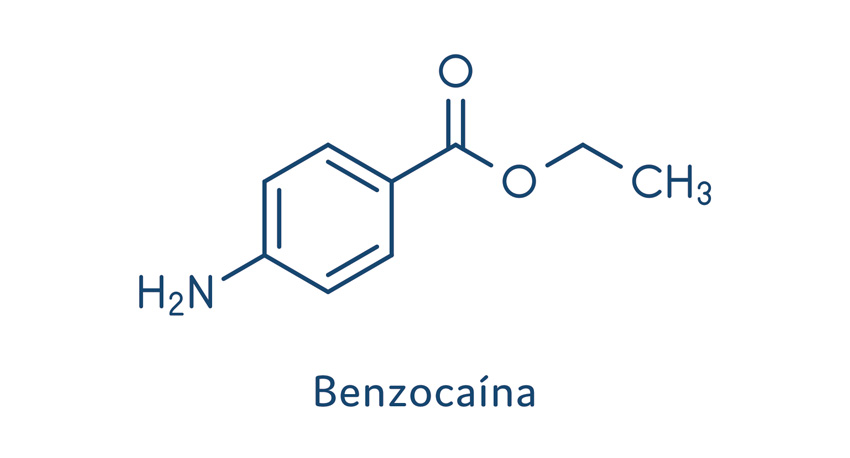
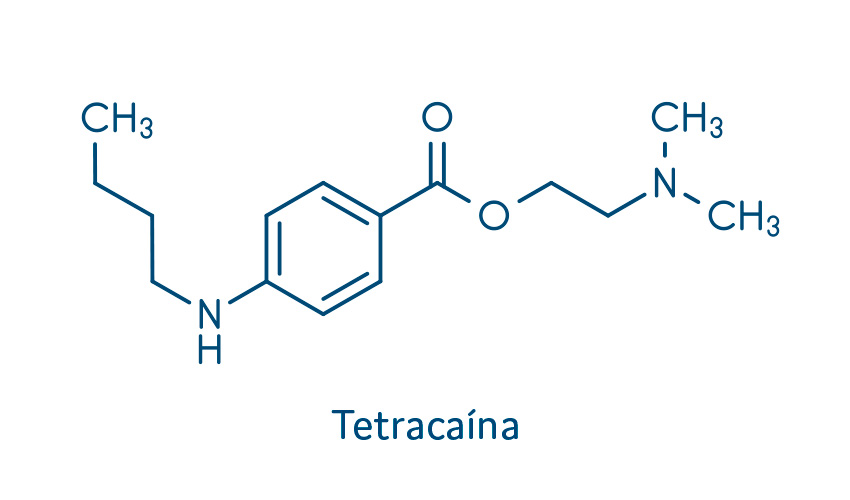
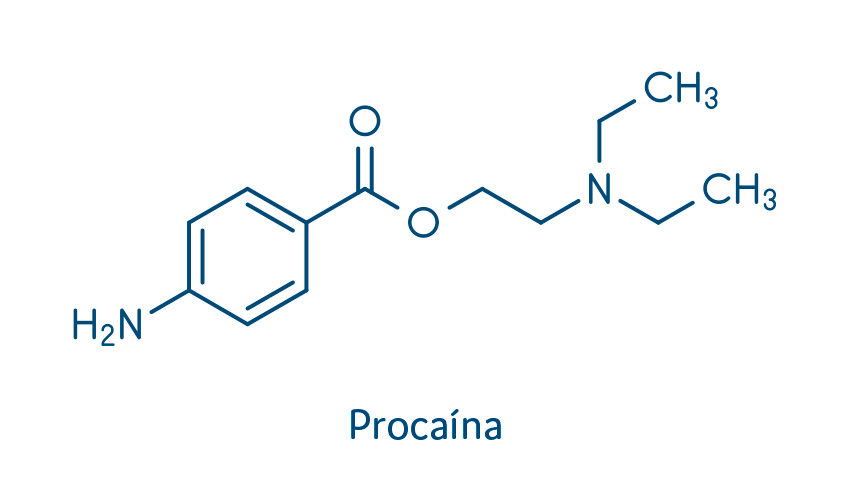
Porção intermediária, uma cadeia que fica entre a porção hidrofílica e a porção hidrofóbica, podendo conter um grupamento amida ou um grupamento éster. Podemos citar como anestésicos do grupo das amidas a lidocaína, a bupivacaína e a prilocaína. Os principais anestésicos do grupo dos ésteres incluem a procaína, a tetracaína e a cocaína (hoje utilizada apenas como droga de abuso).
Veja, na figura 1, as porções hidrofílica, hidrofóbica e intermediárias da procaína e da lidocaína.
Na figura 2, você poderá analisar a estrutura de alguns anestésicos do tipo amida e do tipo éster.
Essas duas classificações podem ser diferenciadas não somente quanto à estrutura (amida e éster), mas também por sua metabolização na via sistêmica.
Anestésicos do
grupo
dos
ésteres
A ligação molecular presente nos anestésicos locais do tipo éster é mais facilmente hidrolisada quando comparada às amidas. Os ésteres sofrem hidrólise por esterases plasmáticas – chamadas de pseudocolinesterases –, sendo mais instáveis em solução, e não ficam armazenados por muito tempo. Ao serem hidrolisados, na maioria das vezes os ésteres geram um metabólito que pode estar associado a processos alérgicos, o PABA (ácido para-aminobenzóico).
Anestésicos do
grupo
das
amidas
A biotransformação das amidas depende da entrada dessas substâncias nos microssomos hepáticos.
Os anestésicos do grupo dos ésteres são menos utilizados se comparados aos do grupo das amidas.
Saiba mais
Um outro fator que influencia no efeito dos anestésicos é a lipofilicidade: moléculas lipofílicas provocam aumento da potência e duração anestésica local. Isso porque elas se acumulam no tecido adiposo e se ligam a locais que apresentam certa lipofilicidade, amplificando o coeficiente de partição dos anestésicos aos seus locais de ação e levando a uma menor taxa de metabolização pelas esterases plasmáticas e enzimas hepáticas.
É importante destacar que, quanto maior a lipofilicidade, maior será a chance do aparecimento de efeitos tóxicos, já que o índice terapêutico é menor com os fármacos dessa natureza.
Quando pensamos em anestésicos locais, imaginamos um fármaco que gere bloqueio eficiente da condução nervosa, durante um tempo adequado, e que proporcione a menor toxicidade possível durante a realização de um procedimento, certo? Para isso é fundamental conhecer bem, além das características farmacológicas do fármaco, doses, presença de vasoconstritor e as maneiras de controlar sua passagem para a corrente sanguínea a partir do local de administração. Vamos a esses tópicos, então:
Quanto mais vascularizado for o local, maior será a absorção e, consequentemente, maior será o nível plasmático esperado.
A dose a ser administrada deverá obedecer a critérios que vão variar de indivíduo para indivíduo, tais como: peso, altura e possíveis interações medicamentosas. Observando-se esses critérios, a chance de erros na determinação da dose é diminuída.
A administração de vasoconstritor juntamente com o fármaco anestésico deve sempre ser considerada, principalmente se o local a ser anestesiado for muito vascularizado. A associação anestésico/vasoconstritor minimiza a passagem do anestésico para o plasma, diminuindo assim as chances de toxicidade do organismo pela droga. Além disso, aumenta o tempo de duração da anestesia no local e traz maior segurança e eficácia durante o procedimento. Essa associação, mesmo que vantajosa em muitos casos, é contraindicada para pacientes com problemas cardíacos, tais como: angina, arritmias cardíacas e insuficiência cardíaca congestiva, por exemplo.
A maior dúvida que fica é:
Por que não se deve utilizar preparações com vasoconstritores
em regiões com pouca circulação sanguínea?
A literatura aponta que a ação de substâncias vasoconstritoras, como a adrenalina, uma amina simpaticomimética, pode estar relacionada com a diminuição da cicatrização de feridas, edemas dos tecidos e necrose. Isso porque essas moléculas aumentam o consumo de oxigênio nesses locais; logo, o uso de fármacos anestésicos associados a vasoconstritores nesses casos pode levar à hipóxia e lesão tecidual local.
A duração da anestesia está diretamente relacionada com o tempo de permanência do anestésico em contato com o nervo. São comuns formulações anestésicas que já contenham vasoconstritores, sendo um dos mais usados a epinefrina. O fato de esses fármacos proporcionarem menor taxa de absorção por uma retenção do anestésico no local desejado traz um equilíbrio entre o processo de metabolização e a taxa com que ele é absorvido para a circulação.

Características farmacológicas do fármaco
Distribuição
A lipossolubilidade e sua capacidade vasodilatadora são importantes características que determinam o efeito dos fármacos anestésicos locais. Quanto mais lipofílica for a molécula, maior é sua capacidade de distribuição, inclusive aumentando seu tropismo pelo tecido adiposo, onde tende a ficar depositada. Devido a isso, uma concentração baixa de anestésico com alta lipossolubilidade será absorvida pelo componente vascular.
Saiba mais
Alguns anestésicos apresentam, em baixa concentração, ação vasodilatadora. Essa propriedade está relacionada com o aumento de sua absorção sistêmica. Uma vez na corrente sanguínea, o risco de toxicidade pelos anestésicos e seus metabólitos aumenta.
Quando atingem a corrente sanguínea, os anestésicos podem se ligar às proteínas plasmáticas e ser distribuídos para os tecidos a fim de se ligarem com receptores específicos. Cada fármaco apresenta uma taxa específica de ligação a proteínas plasmáticas, independentemente se pertence ao grupo das amidas ou dos ésteres.
Dentre as proteínas plasmáticas, boa parte dos anestésicos locais se ligam à proteína alfa globulina. Quanto maior sua afinidade por essa proteína, mais tempo o fármaco permanece no organismo do paciente.
Essa ligação tende a diminuir à medida que sua concentração plasmática aumenta. Observa-se que os anestésicos com alta afinidade com as proteínas tendem a aumentar consideravelmente sua fração livre quando ocorre redução de proteínas no plasma. São essas frações livres do fármaco que irão desempenhar o papel farmacológico ao se ligarem aos seus respectivos receptores, e que também poderão determinar seus efeitos tóxicos.
Metabolização e excreção
A eliminação do anestésico no organismo depende de alguns fatores, como: tempo de meia-vida, depuração e volume de distribuição. Aqueles anestésicos que apresentam um tempo de meia-vida alto tendem a ficar por mais tempo no organismo do paciente e podem levar à intoxicação sistêmica no caso de doses subsequentes. Quanto maior for a depuração renal, menor a possibilidade de intoxicação, e quanto maior o volume de distribuição, maior dificuldade na eliminação da droga anestésica.
Saiba mais
Se pudéssemos definir qual tipo de anestésico tende a ser metabolizado mais rapidamente e, em consequência, com o menor tempo de meia vida, seriam os anestésicos do tipo éster, por serem biotransformados já no plasma, não dependendo das enzimas hepáticas.
Quanto ao tempo de eliminação, também existem diferenças entre os anestésicos dos tipos amida e éster relacionados ao tipo de metabolização, seja por ação das esterases plasmáticas ou das enzimas microssomais hepáticas. Além disso, podemos observar que dentro do mesmo grupo de anestésicos os mecanismos de metabolização também variam. Temos o exemplo da prilocaína, anestésico do tipo amida que sofre uma metabolização rápida pelo fígado comparada com a lidocaína, que ocorre de forma lenta e extremamente complexa. Porém, dentre os anestésicos do grupo das amidas, a etidocaína, a bupivacaína e a ropivacaína são os fármacos que apresentam metabolização mais lenta.
Mecanismo de ação dos anestésicos locais
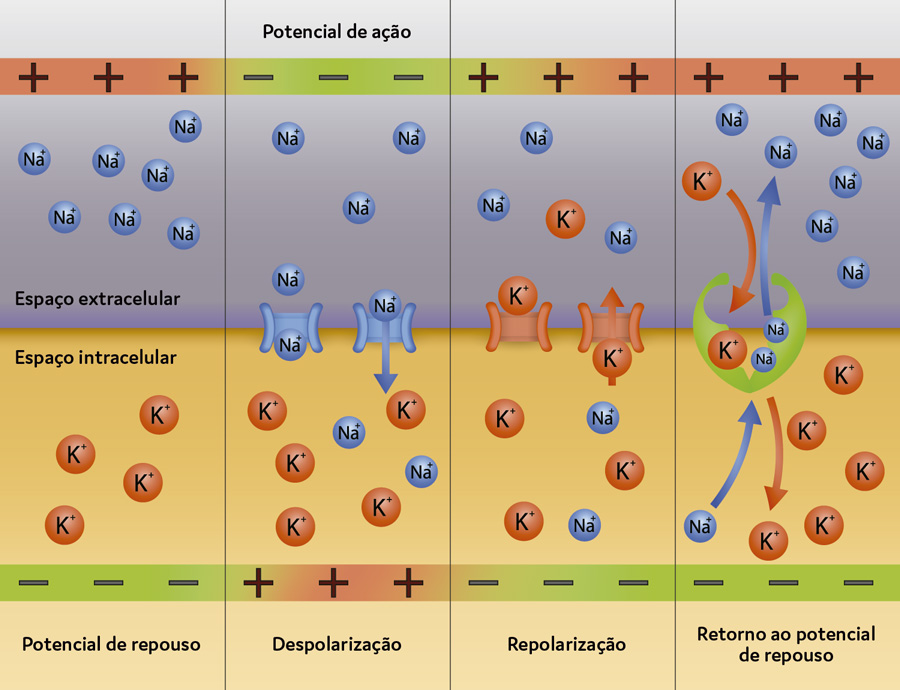
A dor surge por um mecanismo no qual um potencial de ação é gerado em uma fibra nervosa. A propagação ocorre por diferenças nas concentrações de eletrólitos nos meios intracelular e extracelular, o que leva a uma alteração no estado de repouso da fibra.
No repouso, o meio intracelular se mostra rico em potássio; já o meio extracelular, em sódio. Tal diferença de concentração faz com que, nesse estado, o meio extracelular fique carregado mais positivamente, enquanto o meio intracelular se mantém menos positivo. Esse gradiente iônico é mantido por uma bomba conhecida como bomba de sódio potássio ATPase (Na+ K+ ATPase).
Ao gerar um estímulo nervoso, aumenta-se a permeabilidade de sódio pela membrana; logo, as cargas serão invertidas, ou seja, a membrana externa do nervo ficará com carga mais negativa enquanto a membrana interna ficará com carga mais positiva.
O acúmulo de sódio dentro da célula e a consequente inversão na polaridade da membrana levam a um processo de despolarização, dando origem a um potencial de ação. O estado de repouso retorna após o processo de despolarização, que ocorre por mudança da permeabilidade da membrana ao sódio.
Os anestésicos locais são fármacos que têm afinidade reversível a um receptor específico presente nos canais de sódio dos nervos. Ao se ligarem, alteram a conformação do canal, ocasionando um bloqueio no transporte dos íons e não permitindo a entrada dessas espécies no meio intracelular. Assim, os anestésicos inibem a despolarização da membrana e, consequentemente, impedem a condução do impulso nervoso.
Saiba mais
Já se sabe que os canais de Na+ apresentam sítios de ação que podem ser inibidos por diversos fármacos. No caso dos anestésicos locais, essa inibição ocorre na face interna da membrana. A entrada do anestésico ocorre não pelo canal iônico; eles atravessam a bicamada fosfolipídica da membrana, por isso a necessidade de o fármaco apresentar um certo grau de lipofilicidade.
Existe também outra hipótese, dessa vez não específica, para o mecanismo de ação dos anestésicos locais. A hipótese do lipídeo descreve uma interação desses fármacos com os componentes lipídicos da membrana fundamental para o fechamento dos canais de sódio.
Essa nova hipótese passou a ser levantada visto que alguns anestésicos provocariam alterações na estrutura e na dinâmica da matriz lipídica, gerando consequentemente uma mudança conformacional no canal de sódio, justificando sua inativação. De acordo com diversas literaturas, ao observar a fase lipídica da membrana, foram percebidos efeitos de expansão da bicamada e uma queda na temperatura de transição da fase principal, levando a um aumento na fluidez e na permeabilidade da membrana.
Uso de anestésico em tecido
inflamado
estudo de caso
A especialista Cristiane Paiva Coelho Soares aborda o uso de anestésicos em tecido inflamado.
Verificando o aprendizado
ATENÇÃO!
Para desbloquear o próximo módulo, é necessário que você responda corretamente a uma das seguintes questões:
O conteúdo ainda não acabou.
Clique aqui e retorne para saber como desbloquear.
MÓDULO 2
Distinguir as características, indicações, possíveis eventos adversos e contra indicações dos anestésicos locais utilizados na prática clínica
Introdução
Como vimos no módulo anterior, os anestésicos podem ser classificados quanto à função química (amida e éster) da molécula. É importante observar algumas variáveis nos anestésicos, como, por exemplo: a maior estabilidade das amidas, que não sofrem metabolização rápida no plasma pelas pseudocolinesterases em comparação com os ésteres e a não geração de metabólitos, que são os responsáveis pelas reações de hipersensibilidade.
Fatores de interferência na ação dos anestésicos locais
Além das características intrínsecas dos anestésicos, já discutidas, vejamos outros fatores que interferem na ação local desses fármacos, como: pH do meio, pKa da molécula, tamanho da molécula, solubilidade lipídica e tipos de fibras bloqueadas.
pH do meio e pKa da molécula
Os anestésicos locais são bases fracas e pouco solúveis em água e, por isso, podem apresentar duas formas de ionização, dependendo do pH do meio em que se encontram:
Uma forma protonada
(em meio
ácido)
Uma forma não protonada
(em meio
básico)
O que, de fato, irá definir o grau de ionização das moléculas é o seu pKa e o pH do meio no qual se encontram. Resumidamente, podemos dizer que se o pH do meio for maior do que o pKa da substância, a forma predominante será a não protonada. Por outro lado, se o pH do meio for menor que o pKa da molécula, a quantidade de moléculas protonadas será maior. No caso dos anestésicos locais, uma base fraca, temos:
pKa
Parâmetro químico que quantifica a acidez e a basicidade dos compostos.
A forma não protonada é
neutra
(não
ionizada)
A forma protonada é carregada positivamente (ionizada)
Normalmente, o pH dos tecidos difere do pKa do fármaco; logo, haverá maior concentração de uma das formas (ionizada ou não ionizada). Se a molécula estiver na forma ionizada haverá maior dificuldade para entrar no ambiente celular e gerar o efeito anestésico; já na forma não ionizada, o fármaco tende a entrar com maior facilidade.
Podemos concluir, então, que os anestésicos exercem sua ação de forma mais rápida e com menor latência quando o pH do meio em que se encontram é mais elevado que o seu pKa (meio alcalino). Isso porque a maior parte das moléculas estará na forma não ionizada.
Você deve estar pensando que, seguindo essa lógica, os anestésicos atingiriam a sua ação máxima em pH extremamente alto. Mas isso não é bem uma verdade: pH excessivamente altos podem levar à precipitação do fármaco, uma vez que as formas não ionizáveis são também menos solúveis em água. Essa é uma das razões pelas quais toda preparação anestésica comercial se encontra na forma levemente ácida, uma vez que nessas condições o fármaco encontra-se solubilizado em solução aquosa.
Vamos a um exemplo prático.
Exemplo
Foi injetado, em um paciente, anestésico local cujo pKa é 7,9 que chegou ao interstício de um tecido que se encontra com pH fisiológico de 7,4. Como o pKa > pH do meio, observa-se que 75% das moléculas ficaram ionizadas. Os outros 25%, que se encontram na forma molecular (não ionizada), são capazes de atravessar a dupla camada fosfolipídica. Entretanto, no interior da célula, o pH do meio também é menor que o pKa do fármaco. Sendo assim, as moléculas que alcançaram o meio intracelular sofrerão um novo equilíbrio, no qual algumas delas permanecerão não ionizadas e poderão atravessar novamente a membrana plasmática, em direção ao meio extracelular. As demais moléculas passarão para a forma ionizada e, por isso, ficarão “presas” no meio intracelular. São elas que, “retidas” no interior da célula e ligadas aos receptores, de fato exercem o efeito anestésico.
Uma estratégia para aumentar a estabilidade da formulação é a adição de bicarbonato de sódio à solução anestésica imediatamente antes de sua aplicação, para obter um deslocamento do equilíbrio favorecendo maior concentração do fármaco na forma não ionizada.
Saiba mais
Muitas pessoas questionam: “É verdade que a anestesia não funciona quando o meio em questão está muito inflamado?” Um tecido inflamado tem pH baixo, ou seja, ácido. E o pH ácido do meio leva à ionização das moléculas de anestésico, dificultando a passagem do fármaco através da membrana celular e o seu efeito de bloqueio da condução nervosa. Por isso, muitos odontologistas recomendam o tratamento da infecção previamente para só então realizar procedimento que dependa de anestesia local.
Tamanho da molécula
O peso molecular tem relação direta com a taxa de dissociação dos fármacos aos seus receptores. Moléculas de baixo peso molecular conseguem se desprender com maior facilidade. Essa informação é de extrema importância quando discutimos o tempo de despolarização da célula.
Células nervosas se despolarizam rapidamente.
Logo, os anestésicos locais se ligam durante a geração do potencial de ação, no processo de despolarização, e dissociam-se durante o período em que ocorre a repolarização, para que a célula retorne ao seu estado de repouso.
Sua ligação rápida durante o período em que ocorre o potencial de ação é responsável por seu efeito.
Solubilidade lipídica
A solubilidade lipídica está diretamente relacionada à latência anestésica, ou seja, ao tempo de início da ação farmacológica. Moléculas mais lipofílicas tendem a proporcionar efeito anestésico mais rapidamente, uma vez que conseguem atravessar com mais facilidade a membrana do nervo e promover o bloqueio do canal iônico.
Tipos de fibras bloqueadas
As fibras nervosas apresentam sensibilidades diferentes aos anestésicos locais. As fibras menores são mais sensíveis aos anestésicos comparadas às maiores. Quanto à presença de bainha de mielina, as fibras mielinizadas são bloqueadas mais rapidamente do que as não mielinizadas, mesmo apresentando o mesmo diâmetro. O bloqueio das fibras pelos anestésicos ocorre de maneira gradativa, pela perda da sensibilidade à dor, posteriormente à temperatura, ao tato e à compressão profunda e, por último, pela perda da função motora. Desse modo, justifica-se, em muitos casos, o fato de o paciente sentir o toque, sem sentir dor.

Anestésicos locais do grupo das amidas
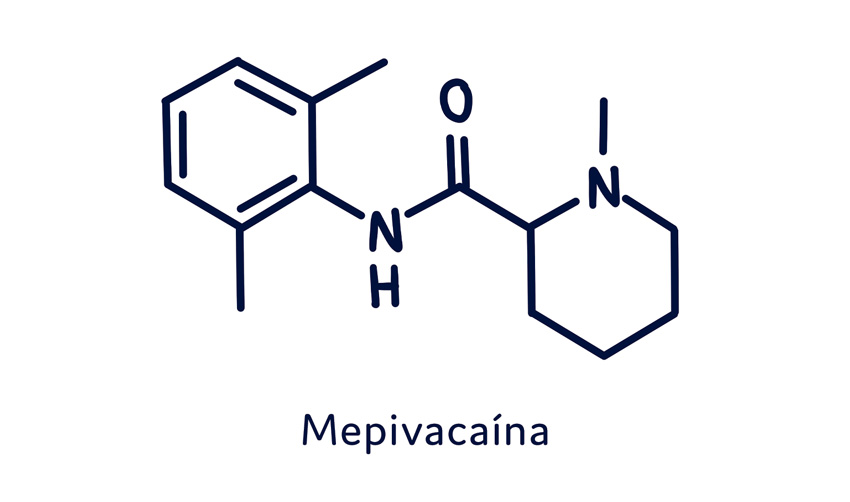
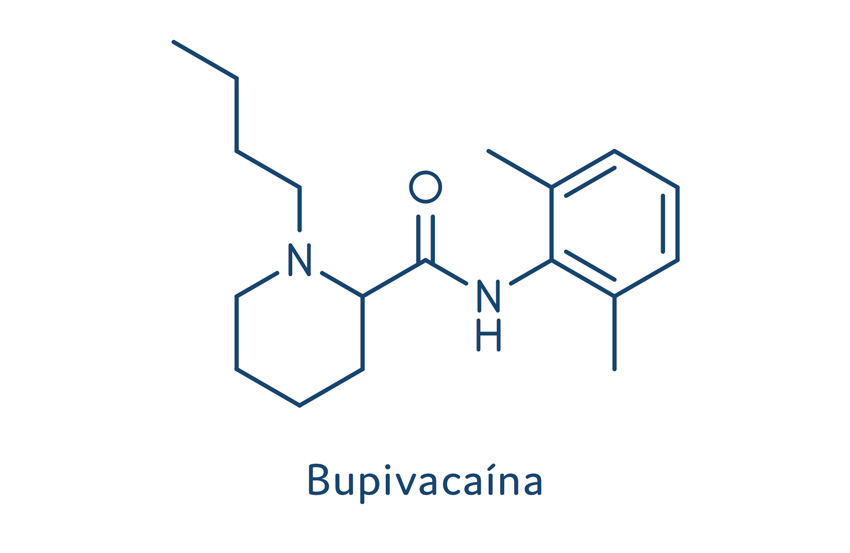
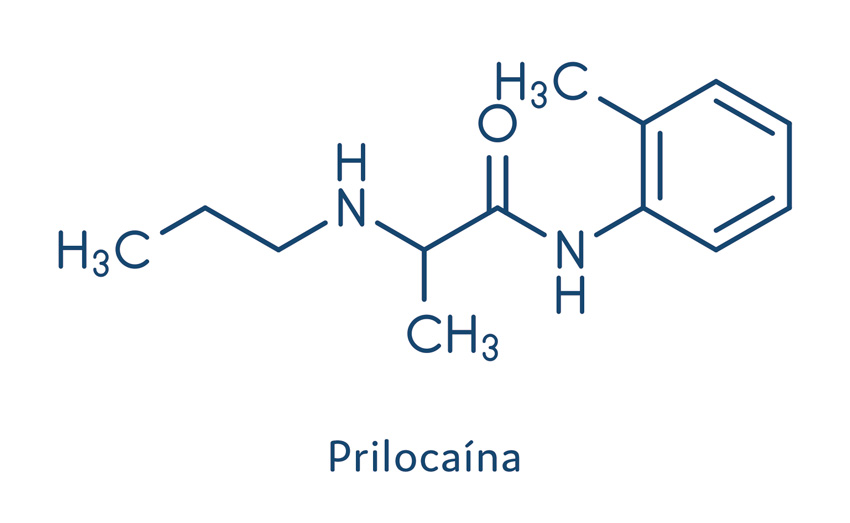
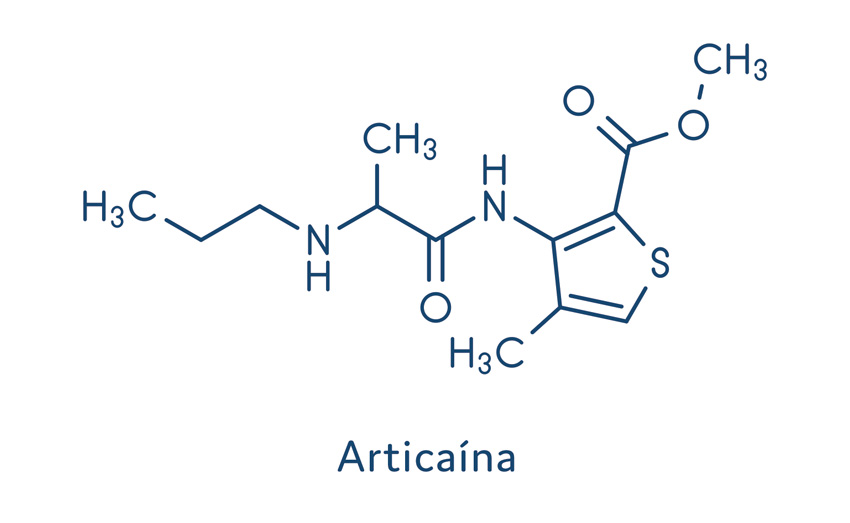
Os anestésicos locais do tipo amida são os mais utilizados na anestesia local, visto que os do tipo éster estão caindo em desuso devido ao seu alto potencial alergênico. Os fármacos do tipo amida mais utilizados são: lidocaína, mepivacaína, bupivacaína, prilocaína e articaína.
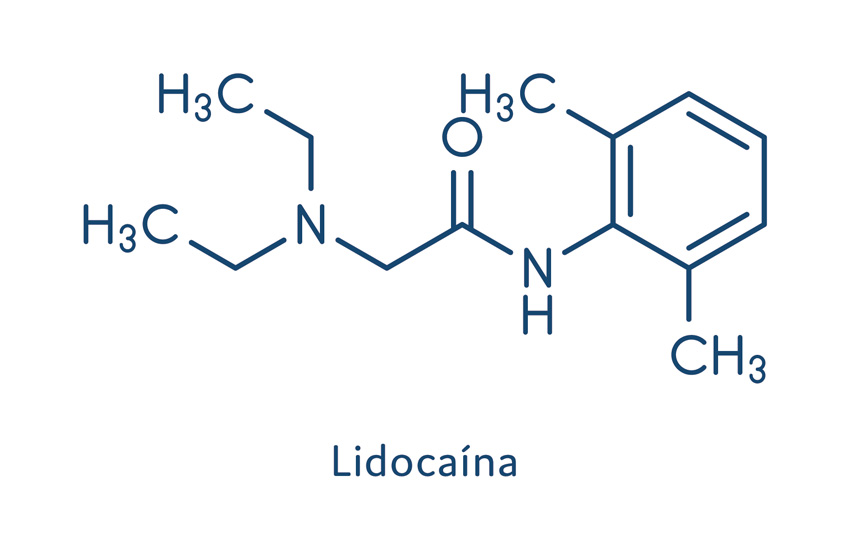
Lidocaína
A lidocaína é um anestésico local lançado em 1947 que proporciona importante bloqueio motor reversível. Indicado para o alívio de dor temporária associada a pequenos cortes com duração intermediária, apresenta vasta utilização na Odontologia; no alívio da dor durante a realização de exames, como proctoscopia, cistoscopia, intubação endotraqueal; nas dores associadas a queimaduras leves e abrasões da pele. Também pode ser utilizada como agente antiarrítmico, por suprimir as arritmias ventriculares pela diminuição da automaticidade. Promove proteção cardíaca por apresentar atividade antiarrítmica, devido ao seu efeito vasodilatador. Esse efeito pode limitar a ação da anestesia local, além de levar a um aumento de sua concentração na corrente sanguínea e, por isso, aumentar os riscos de reações adversas.
Proctoscopia
Procedimento médico que tem por objetivo examinar a cavidade anal, o reto ou o cólon sigmoide com a utilização de um instrumento, chamado de proctoscópio.
Cistoscopia
Procedimento médico que analisa os segmentos uretrais e da bexiga com a utilização de um instrumento chamado de cistoscópio.
É muito comum a apresentação de lidocaína associada a vasoconstritor, como felipressina, epinefrina, adrenalina, noradrenalina e fenilefrina, com a intenção de retardar o processo de absorção para a corrente sanguínea, prolongando a duração do efeito do anestésico no local do procedimento.
O uso da lidocaína deve ocorrer com cautela em pacientes cardiopatas, já que os vasoconstritores adrenérgicos podem levar a manifestações clínicas, como elevação da pressão arterial acompanhada de taquicardia ou bradicardia de natureza compensatória. Caso o paciente apresente apenas hipertensão e a pressão esteja bem controlada, poderá haver a utilização de lidocaína com vasoconstritor adrenérgico.
Em idosos, o uso deve ocorrer com cautela, visto que esses pacientes podem apresentar comorbidades, muitas vezes cardiovasculares. Caso não haja qualquer tipo de comorbidade, o uso de lidocaína é indicado em associação com vasoconstritores, no intuito de aumentar a potência e compensar o efeito vasodilatador do anestésico da musculatura esquelética.
Outro grupo de pacientes para quem é indicado o uso de lidocaína são as gestantes. Tal fármaco apresenta alto grau de segurança quando associado à adrenalina na concentração de 1:100.000, com a utilização de, no máximo, dois tubetes por atendimento.
O início da ação da lidocaína é rápido, sua duração média vai de uma a duas horas e apresenta potência analgésica moderada. Tem um valor relativamente baixo de pKa, e uma grande fração do fármaco encontra-se presente na forma não ionizada em pH fisiológico; por isso seu rápido início de ação.
Na Odontologia, as apresentações mais utilizadas são: lidocaína + epinefrina ou lidocaína + adrenalina.
Comorbidades
Paciente que apresenta duas ou mais doenças etiologicamente relacionadas.
Mepivacaína
A mepivacaína é um anestésico local que começou a ser comercializado nos Estados Unidos na década de 1960. Apresenta uma ação semelhante à da lidocaína, porém com efeito menos vasodilatador. Exerce sua ação por bloqueio de nervo ou por infiltração, na concentração de 2% com vasoconstritor e de 3% sem vasoconstritor. Não tem indicação clínica na obstetrícia por mostrar alta toxicidade aos recém-nascidos relacionada à sua retenção iônica devido ao pH mais baixo do sangue desses pacientes e ao pKa do fármaco. Sua duração anestésica sem vasoconstritor é alta em comparação à lidocaína – em torno de 20-40 minutos –, porém está entre os anestésicos mais tóxicos. Ao associar a mepivacaína com vasoconstritor, neste caso a epinefrina, obtém-se uma hemostasia desejável durante todo o procedimento.
Pacientes que sejam contraindicados ao uso de vasoconstritor podem se beneficiar desse anestésico, pelo fato de a mepivacaína apresentar menor poder vasodilatador.
Quanto aos parâmetros farmacocinéticos, a mepivacaína é bem semelhante à lidocaína, ou seja, apresenta um pKa relativamente baixo, em torno de 7,6, quando comparada a outros anestésicos. Esses fármacos diferenciam-se quanto ao volume de distribuição e magnitude nos níveis plasmáticos alcançados. Seu uso está limitado aos pacientes que utilizam medicamentos que levem a alterações na pressão arterial, como antidepressivos tricíclicos, inibidores da monoaminoxidase.
Quanto ao uso tópico, não é indicado, pois por essa via a mepivacaína apresenta eficácia apenas em doses muito altas.
Bupivacaína
A bupivacaína é um anestésico local com ação dose dependente. Sua rápida ação está diretamente relacionada com o local de administração a um bloqueio mais sensorial do que motor. Logo, esse fármaco apresenta larga utilização no trabalho de parto ou até em período pós-operatório, no intuito de prolongar a analgesia. Quando empregado na raquianestesia, apresenta uma rápida resposta de bloqueio dos canais de sódio e de média à longa duração.
Esse anestésico apresenta um pKa de 8,1, mais alto quando comparado ao da lidocaína e ao da mepivacaína. A duração de seu efeito varia entre duas e três horas.
A bupivacaína tem um enantiômero – a levobupivacaína –, que oferece maior segurança e menos efeitos cardiotóxicos, porém não apresenta uma rápida instalação no bloqueio quando comparada à bupivacaína.
Seus efeitos adversos estão relacionados com a cardiotoxicidade, podendo levar a arritmias ventriculares e depressão miocárdica grave. Essa cardiotoxicidade está pautada pela dissociação lenta do fármaco nos canais de sódio durante o processo de diástole.
Enantiômeros
Moléculas que são como imagens no espelho uma da outra, e não são sobreponíveis.
Prilocaína
Muito empregada na Odontologia, a prilocaína é um anestésico local de ação intermediária, com pKa de 7,89. Apresenta como propriedade farmacológica menor potência do que a lidocaína e, por isso, é utilizada em concentrações de 4%, comparada aos 2% da lidocaína. Por apresentar rápida metabolização hepática, esse fármaco é um anestésico sistemicamente menos tóxico, quando comparado a outros do tipo amida com potência equivalente. A prilocaína apresenta um poder vasodilatador menor do que outros analgésicos, permitindo, assim, sua utilização de forma isolada. Entretanto, em apresentações farmacêuticas, encontra-se associada à felipressina, um vasoconstritor de baixa potência.
Cabe destacar que a prilocaína, após a biotransformação por enzimas hepáticas, gera um metabólito, a ortotoluidina, que leva à formação da metemoglobina. Essa molécula é extremamente nociva para indivíduos anêmicos, neonatos e gestantes, já que quando formada em grandes quantidades pode causar metemoglobinemia.
O vasoconstritor utilizado em formulações comerciais com a prilocaína é a felipressina, também conhecida como octapressim. Esse fármaco é análogo ao hormônio antidiurético, que é um vasoconstritor não adrenérgico, bem tolerado em pacientes cardiopatas, já que sua atuação no miocárdio não é clinicamente observada, mostrando constrição apenas na musculatura lisa vascular da microvasculatura venosa.
Metemoglobinemia
Quadro clínico causado pela transformação em excesso de hemoglobina em metemoglobina, que é incapaz de se ligar ao oxigênio e transportá-lo pela corrente sanguínea.
Articaína
A articaína é um anestésico local com pKa de 7,8, mais potente do que a lidocaína e com possibilidade de ser associado a vasoconstritor. Foi aprovado para uso no Brasil apenas em 1999. Apresenta uma estrutura química híbrida por ter uma porção éster e amida; logo, sua biotransformação não ocorre somente pelas enzimas hepáticas, mas também pelas pseudocolinesterases plasmáticas. Desse modo, esse fármaco apresenta um tempo de meia-vida plasmático bem inferior aos outros anestésicos locais do tipo amida, apresentando menor toxicidade sistêmica.
Uma peculiaridade da articaína é a presença de um grupo tiofeno ao invés de anel benzênico em sua estrutura, o que traz a essa molécula maior grau de lipossolubilidade. Esse fármaco também pode levar à metemoglobinemia.
Anestésicos locais do grupo dos ésteres
Os anestésicos locais do tipo éster são fármacos biotransformados no plasma por pseudocolinesterases, gerando metabólitos do tipo PABA, altamente alergênicos. Eles apresentam ligações químicas mais fáceis de serem quebradas; por esse motivo mostram-se mais instáveis quando comparados aos anestésicos do tipo amida. Devido à baixa estabilidade, não podem ser armazenados durante muito tempo.
Os fármacos do tipo éster mais utilizados na clínica são: benzocaína, tetracaína e procaína. Vejamos as características farmacológicas de cada um deles.
Benzocaína
Apresenta um pKa de 2,5; logo, em condições fisiológicas é encontrada somente na forma neutra. Seu efeito anestésico é de alta duração, devido à dificuldade em ser absorvida para a circulação sistêmica, permanecendo por mais tempo no local em que foi administrada. Inicia sua ação de maneira rápida, aproximadamente 15 segundos, quando aplicada sobre a mucosa bucal. Sua biotransformação é mediada por enzimas presentes no plasma sanguíneo e a excreção dos metabólitos e pequenas frações inalteradas é feita por via renal, sendo favorecida pela acidificação da urina.
A benzocaína apresenta uma boa utilização prévia em anestesia tópica na mucosa oral, seguida da anestesia infiltrativa. Pode ser encontrada nas seguintes apresentações:
Indicada para anestesia palatina em pacientes que necessitam fazer moldagens e apresentam dificuldade por causa do alto reflexo de vômito.
Administrada antes do uso de anestésicos infiltrativos locais, no intuito de minimizar o desconforto da agulha.
Indicadas em situações de úlceras aftosas e úlceras traumáticas.
Saiba mais
Esse fármaco está relacionado ao desenvolvimento de metemoglobinemia, assim como a prilocaína, logo não deve ser prescrito para pacientes com anemia falciforme, neonatos e gestantes. Os efeitos adversos mais comuns são: prurido, erupção cutânea, irritação local, vermelhidão na pele.
Tetracaína
A tetracaína é um anestésico local com pKa de 8,0 que apresenta alta lipofilicidade e elevada potência. Esse fármaco se liga por mais tempo ao sítio no canal de sódio, apresentando uma duração mais prolongada quando comparado à procaína e à lidocaína, devido à sua permanência no tecido. Mostra-se com início de ação mais lento e com alta probabilidade de efeitos tóxicos, pois demonstra ter uma metabolização mais lenta se comparado a outros anestésicos do tipo éster. Isso se deve ao fato de ser liberado gradativamente dos tecidos para a corrente sanguínea.
Indicada em anestesia espinhal, principalmente quando existe a necessidade de um fármaco com uma duração mais prolongada, a tetracaína também é empregada em cirurgias oftalmológicas, como retirada de corpos estranhos da conjuntiva, anestesia do globo ocular, dentre outros procedimentos.
Saiba mais
Seus principais efeitos adversos estão relacionados a alterações cutâneas, como eritema e prurido, por sofrer hidrólise na derme pelas esterases teciduais. Essa biotransformação se relaciona diretamente a possíveis processos alérgicos pela geração de metábolitos PABA (ácido paraminobenzoico).
Procaína
A procaína é um anestésico local com valor de pKa de 8,9. Apresenta tempo de início de ação estimado em cinco minutos e duração de 30-60 minutos. Esse curto tempo de ação se deve à rápida metabolização no plasma e à baixa afinidade com as proteínas plasmáticas, colaborando para o baixo tempo de atuação farmacológica.
Saiba mais
Quanto à farmacocinética, a procaína apresenta uma absorção diretamente relacionada à dose administrada, à via escolhida, à vascularização do local, ao grau de vasodilatação e ao estado fisiológico do paciente.
Usos e características farmacológicas dos vasoconstritores
Como já discutimos, a associação entre anestésicos locais e vasoconstritores nas formulações anestésicas comerciais é bastante importante. Vamos ver a seguir um resumo sobre a utilização dos vasoconstritores em associação com os anestésicos locais:
|
Objetivo |
Minimizar o efeito vasodilatador presente em boa parte dos anestésicos locais. |
|
Ação farmacológica |
Controlar a perfusão local, tendo como consequência a diminuição da absorção sistêmica dos anestésicos e o consequente aumento do tempo de resposta farmacológica no local. |
|
Vantagens |
Manter o campo cirúrgico mais “limpo”. Reduzir a perda sanguínea em casos de trauma. Promover efeito protetor, por aumentar a intensidade e a duração do efeito anestésico, diminuindo o risco de toxicidade sistêmica. |
|
Desvantagens |
Alterar a pressão arterial e a frequência cardíaca. |
Os vasoconstritores utilizados em formulações anestésicas são quimicamente idênticos ou semelhantes aos neurotransmissores ou neuro-hormônios adrenérgicos (noradrenalina e adrenalina, respectivamente). Os mais empregados são: adrenalina (epinefrina), noradrenalina (noraepinefrina) e felipressina (octapressin).
A adrenalina é um neuro-hormônio sintetizado pela porção medular das glândulas suprarrenais que tem atuação sobre receptores beta e alfa adrenérgicos. No sistema cardiovascular, leva a um aumento da pressão sistólica e da frequência cardíaca.
A noradrenalina é um neurotransmissor sintetizado pelos neurônios noradrenérgicos. Apresenta maior resposta sob os receptores alfa adrenérgicos, podendo agir em receptores beta adrenérgicos. Atua levando ao aumento da pressão sistólica e diastólica, sem alterar a frequência cardíaca. Muitos pesquisadores descrevem o uso da noradrenalina como perigoso, por induzir a uma potente vasoconstrição, levando dessa forma a danos teciduais significativos.
A felipressina é uma amina não simpaticomimética análoga sintética da vasopressina (hormônio sintetizado pela neuro-hipófise). Sua maior vantagem frente à utilização em formulações anestésicas está no fato de que não atua sobre os receptores cardíacos. Por outro lado, seu uso pode aumentar a pressão sistólica e diastólica, determinando queda na frequência cardíaca e podendo causar crises de angina.
Angina
Síndrome clínica que leva a um desconforto no paciente, como: sensação de aperto, pressão, peso ou dor no peito. Normalmente causada por patologias que provocam obstrução nas artérias.
Saiba mais
Muito anestésicos locais apresentam em sua formulação bicarbonato de sódio. Esse sal, composto por íons bicarbonato e íons sódio, leva a um aumento do pH do meio e faz com que a concentração do fármaco na forma não ionizada seja maior, aumentando a velocidade da resposta farmacológica, ou seja, diminuindo o período de latência.
A escolha do anestésico local depende do tipo de procedimento e as doses máximas recomendadas para cada fármaco devem estar de acordo com o peso corporal do paciente e altura. O quadro a seguir compara os principais procedimentos anestésicos frente aos principais fármacos recomendados, de acordo com a prática clínica.
|
Procedimento anestésico |
Anestésico local |
Observação |
|---|---|---|
|
Anestesia tópica |
Lidocaína e tetracaína |
Em caso de nebulização, a lidocaína é feita com frequência em anestesia superficial da via aérea superior e inferior antes do procedimento de laringoscopia e/ou broncoscopia. Na forma de creme, existe uma mistura eutética de lidocaína e prilocaína. Essa mistura, conhecida como EMLA (Eutetic Mixture of Local Anesthetics), permite altas concentrações dos anestésicos sem trazer irritação local, absorção irregular ou toxicidade sistêmica. A anestesia tópica é indicada para a inserção de agulhas para introdução de cateteres venosos e procedimentos cirúrgicos superficiais, por exemplo. |
|
Anestesia local por infiltração |
Lidocaína |
Quando associada a um vasoconstritor (epinefrina), o tempo de ação poderá ser dobrado. Não deve ser administrada epinefrina na via intracutânea ou em tecidos pouco vascularizados, pois isso pode provocar vasoconstrição severa, levando a uma isquemia e trazendo como consequência uma necrose tissular. |
|
Anestesia por bloqueio de nervos periféricos |
Lidocaína e bupivacaína |
A duração desse tipo de anestesia irá depender da concentração do anestésico, do seu grau de solubilidade lipídica, da interação com as proteínas plasmáticas e do uso concomitante de um vasoconstritor. |
|
Anestesia peridural |
Lidocaína, bupivacaína, levobupivacaína e ropivacaína |
Esses fármacos estão associados a um menor risco de toxicidade cardíaca. |
|
Anestesia espinhal – raquianestesia |
Tetracaína, lidocaína, bupivacaína e ropivacaína |
A dose do anestésico irá variar com o procedimento a ser realizado, de acordo com a altura do paciente, que determina o volume do espaço subaracnoide; nível segmentar desejado de anestesia e duração anestésica desejada. |
Eutética
Mistura eutética: é uma mistura de substâncias químicas que não sofrem interação para a formação de um composto novo. Em certas proporções, porém, podem inibir o processo de cristalização um do outro, resultando em um sistema com ponto de fusão inferior ao dos componentes.
Uma abordagem dos principais
anestésicos locais.
Caso clínico com uso de prilocaína e felipressina
A especialista Cristiane Paiva Coelho Soares fala sobre a diferença entre os principais anestésicos do tipo amida e éster, indicando um caso clínico e discutindo o uso de prilocaína e felipressina na prática odontológica em pacientes cardiopatas.
Verificando o aprendizado
ATENÇÃO!
Para desbloquear o próximo módulo, é necessário que você responda corretamente a uma das seguintes questões:
O conteúdo ainda não acabou.
Clique aqui e retorne para saber como desbloquear.
Conclusão
Considerações Finais
Conhecer a farmacocinética e a farmacodinâmica dos anestésicos locais é de suma importância para a escolha do melhor fármaco para cada procedimento, ajudando a estimar a potência anestésica, a velocidade de início da ação, duração e, consequentemente, oferecendo segurança para o paciente. Os anestésicos locais têm uma vasta indicação clínica porque seu bloqueio ocorre de forma temporária e não provocam alteração do nível de consciência. Para ser considerado um bom anestésico local, o fármaco deverá apresentar baixa toxicidade, não ser irritativo aos tecidos e não trazer qualquer lesão às estruturas nervosas.
Como discutimos ao longo do estudo deste tema, os anestésicos locais são divididos em dois grupos, amida e éster. Os fármacos pertencentes ao grupo amida apresentam menor toxicidade, alta eficácia e são menos alergênicos, comparados aos ésteres.
Conhecer cada anestésico, sua indicação clínica e contraindicações, é essencial para se evitar possíveis eventos adversos e garantir a segurança do paciente. Isso quer dizer que, quando cuidadosamente administrados e respeitando os limites de dosagem terapêutica recomendada, esses fármacos apresentam um elevado índice de segurança.
Podcast
Agora, a especialista Cristiane Paiva Coelho Soares encerra o tema respondendo algumas perguntas sobre os dois módulos.
CONQUISTAS
Você atingiu os seguintes objetivos:
Compreendeu conceitos gerais dos anestésicos locais e dos vasoconstritores, e seu comportamento farmacocinético e farmacodinâmico
Ut enim ad minim veniam, quis nostrud exercitation ullamco
Distinguiu as características, indicações, possíveis eventos adversos e contra indicações dos anestésicos locais utilizados na prática clínica.